DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
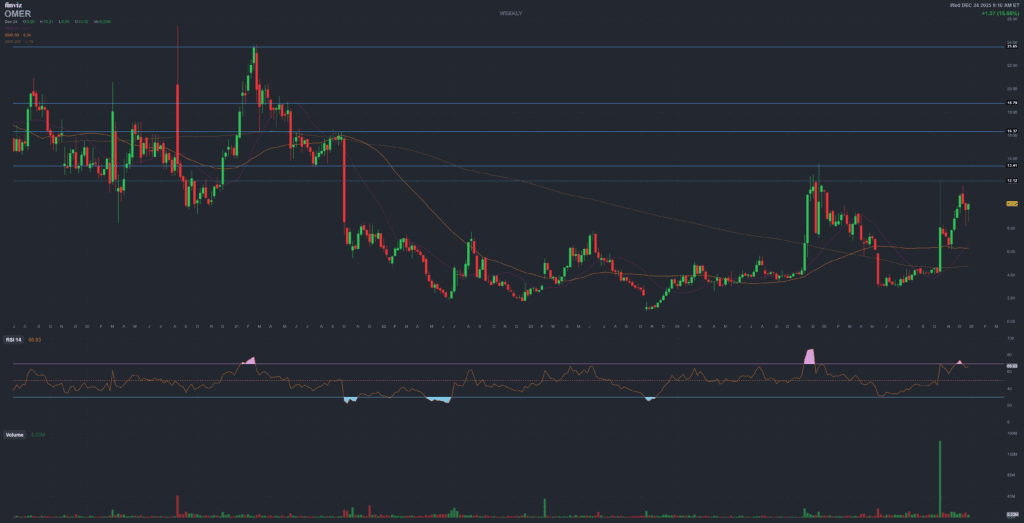
Omeros Corporation – NASDAQ: OMER
YARTEMLEA FDA approval: first-ever TA-TMA therapy and a new chapter for Omeros
The FDA has approved YARTEMLEA (narsoplimab-wuug) as the first and only treatment for transplant-associated thrombotic microangiopathy (TA-TMA) in adults and children ≥2 years. Here is what the label, data package, launch setup and Novo Nordisk deal really mean for the story.
Last price (approx.)
~9–10 USD per share
Fast-moving session around approval.
Market cap (range)
~650–700M USD
Small-mid cap, high volatility.
Status
FDA approved – TA-TMA
US launch planned Jan 2026.
Data points are indicative snapshots around the approval date and will move with the market.
News of the day – FDA approval
The FDA has approved YARTEMLEA (narsoplimab-wuug) for treatment of hematopoietic stem cell transplant-associated thrombotic microangiopathy (TA-TMA) in adults and children 2 years and older. YARTEMLEA is the first and only approved inhibitor of the lectin complement pathway and the only FDA-approved therapy for TA-TMA.
Approval is based on a single-arm, open-label adult TA-TMA study (N=28) plus data from a global expanded-access program (EAP; N=221), showing complete response rates of about 61–68% and 100-day survival around 73–74% in a uniformly high-risk population. The safety profile is consistent with transplant patients in general but serious infections and sepsis remain central risks and are highlighted in the label.
Executive summary – how the narrative just changed
With YARTEMLEA’s approval, Omeros exits the “all-or-nothing PDUFA” limbo and finally becomes a commercial-stage complement company again. The label is broad for such a rare and catastrophic condition: adults and children ≥2 years, no black-box, and efficacy supported by both pivotal trial and real-world expanded-access data.
The approval lands on top of a transformative up-to-2.1B USD transaction with Novo Nordisk on MASP-3 inhibitor zaltenibart (OMS906), which has already delivered a 240M upfront payment and allowed Omeros to repay its term loan and clean up the balance sheet. Together, the Novo cash and YARTEMLEA launch remove much of the existential risk that had haunted the story since the 2021 CRL.
This does not mean the stock suddenly becomes low-risk. YARTEMLEA is targeting an ultra-orphan, hospital-based complication that depends on transplant volumes, payer behavior and real-world uptake. Omeros remains a loss-making, high-beta micro/small-cap, and the path from “first approval” to “durable cash-generating franchise” is still long.
First and only TA-TMA therapy
Lectin pathway first-in-class mechanism
Ultra-orphan hospital market
Infection / sepsis risk
History of heavy cash burn and dilution
1. What exactly did the FDA approve?
1.1 The indication and label
YARTEMLEA is approved for treatment of hematopoietic stem cell transplant-associated thrombotic microangiopathy (TA-TMA) in adults and children aged two years and older. It is a fully human monoclonal antibody that selectively inhibits MASP-2, shutting down lectin-pathway activation while sparing classical and alternative complement pathways, which are important for host defense.
This is crucial: unlike broad C3/C5 blockade, MASP-2 targeting aims to reduce thrombotic microangiopathy and endothelial damage without fully disarming the complement system. The FDA label recognizes YARTEMLEA as the first and only approved lectin-pathway inhibitor and, more importantly, the only approved therapy for TA-TMA at all.
1.2 The data package behind approval
The approval rests primarily on:
- A single-arm, open-label adult TA-TMA study (“TA-TMA Study”, N=28), in which all patients met stringent high-risk criteria.
- Additional data from a global expanded-access program (EAP) including 221 adult and pediatric patients with TA-TMA; 19 patients (13 adult, 6 pediatric) had evaluable patient-level response data.
The primary efficacy endpoint was complete response (CR), defined as improvement in key TMA lab markers (platelets and LDH) together with either organ-function improvement or transfusion independence. YARTEMLEA achieved:
- 17/28 CRs (61%) in the adult TA-TMA study.
- 13/19 CRs (68%) among evaluable EAP patients.
Survival was equally important. Across the pivotal trial and the EAP, 100-day survival from TMA diagnosis reached roughly 73–74% in a population where severe TA-TMA historically can exceed 90% mortality. Peer-reviewed analyses comparing YARTEMLEA-treated patients to external control cohorts reported a three- to four-fold reduction in mortality risk, with one-year survival around 50% even in patients refractory to prior complement inhibitors or defibrotide, versus historical rates below 20%.
1.3 Safety and warnings
As expected in this population, the safety profile is dominated by infection and transplant-related complications rather than drug-specific toxicities:
- Serious infections occurred in roughly one-third of patients receiving YARTEMLEA, including sepsis, pneumonia, bacteremia, fungal infections and viral illnesses.
- The most common adverse reactions (≥20%) were viral infections, sepsis, hemorrhage, diarrhea, vomiting, nausea, neutropenia, pyrexia, fatigue and hypokalemia.
- Serious adverse reactions were reported in about 61% of patients, and fatal adverse reactions in about 7%, primarily neutropenic sepsis and septic shock.
Crucially for commercial positioning, the label does not introduce unexpected black-box warnings beyond what transplant teams already manage daily. Instead, it formalizes the need for vigilant infection monitoring and rapid treatment in this extremely fragile population.
2. TA-TMA and the size of the opportunity
Hematopoietic stem cell transplant-associated thrombotic microangiopathy is one of those complications every transplant center fears. It arises from systemic endothelial injury driven by conditioning regimens, calcineurin inhibitors, graft-versus-host disease, infections and other transplant stressors. The lectin complement pathway plays a central role in this cascade, with MASP-2 acting as a key effector enzyme.
Several points define the commercial opportunity:
- Roughly 30,000 allogeneic stem-cell transplants are performed each year across the U.S. and Europe.
- Recent studies suggest TA-TMA may develop in up to 50–56% of allogeneic recipients, although only a subset meets strict high-risk criteria.
- Severe high-risk TA-TMA carries historical mortality that can exceed 90%, with survivors frequently left with chronic renal damage or dialysis dependence.
Until now, there was no established, on-label therapy. Physicians juggled:
- Supportive measures (altering calcineurin inhibitors, managing GVHD and infections).
- Off-label use of complement inhibitors (mainly C5 blockers) with limited evidence.
- Occasional defibrotide use in some centers.
YARTEMLEA enters as the only approved, reimbursable option with dedicated ICD-10 and CPT codes. The company also expects a Medicare New Technology Add-On Payment (NTAP), which would help hospitals cover the cost in the DRG system. In practice, this means that once TA-TMA is recognized, there is now a clear, codified treatment pathway instead of a patchwork of off-label improvisation.
3. Launch setup: how ready is Omeros?
3.1 Commercial infrastructure
Well before approval, Omeros built out a launch-ready U.S. commercial organization:
- A first wave of sales specialists with deep experience in hematology and transplant centers.
- Ongoing pre-approval information exchanges with KOLs, transplant program directors and payers, which management describes as “consistently encouraging”.
- Clear branding: narsoplimab is now officially YARTEMLEA in the TA-TMA setting.
3.2 Reimbursement and codes
A key part of the story is that YARTEMLEA does not arrive alone but with its reimbursement plumbing largely pre-installed:
- ICD-10-CM code M31.11 – specific for HSCT-associated TA-TMA.
- ICD-10-PCS procedure codes XW03357 / XW04357 – for peripheral and central vein administration of the monoclonal antibody.
- An NTAP application under Medicare to help hospitals bridge the gap between DRG payment and actual drug cost.
On top of this, Omeros will run a dedicated patient-support program, YARTEMLEAssist, to help with benefits verification, prior authorizations and potential financial assistance.
3.3 Europe and rest-of-world
The TA-TMA story is not purely American. A Marketing Authorization Application (MAA) for YARTEMLEA is under review at the EMA, with an opinion expected around mid-2026. A positive CHMP opinion would open up a second major geography of transplant centers across the EU, where transplant volumes and TA-TMA incidence are substantial.
For now, the focus is squarely on the U.S. launch in January 2026. Investors will be watching:
- The number of transplant centers actively treating TA-TMA with YARTEMLEA.
- The balance between first-line and salvage use after other complement agents.
- Speed of payer coverage decisions and any access frictions.
Because the label is ultra-orphan and hospital-centric, even a relatively small number of centers adopting YARTEMLEA as de-facto standard could translate into meaningful revenue. But the ramp will likely be lumpy, with case numbers too small to smooth quarter-to-quarter noise.
4. Pipeline beyond YARTEMLEA and the Novo Nordisk deal
4.1 MASP-2 franchise – YARTEMLEA and OMS1029
YARTEMLEA is only the first MASP-2-targeting asset to hit the market. Behind it sits OMS1029, a long-acting MASP-2 inhibitor that has completed Phase 1 and is being positioned as a second-generation lectin-pathway backbone for future indications.
Combined, YARTEMLEA and OMS1029 give Omeros a platform in lectin-pathway complement disorders that could eventually extend beyond TA-TMA into nephrology, autoimmune disease and possibly certain inflammatory settings, depending on emerging data.
4.2 MASP-3 and Novo Nordisk: zaltenibart (OMS906)
On the other side of the complement system, Omeros has effectively outsourced the heavy lifting on MASP-3 to one of the world’s largest pharma players. Under the asset purchase and license agreement with Novo Nordisk:
- Omeros receives 240M USD in upfront cash (already paid) plus up to 100M USD in near-term milestones.
- Total potential milestones reach 2.1B USD, including 410M USD in development and approval milestones and 1.3B USD in sales-based milestones, plus tiered royalties on net sales.
- Novo obtains global rights to zaltenibart (OMS906), a MASP-3 inhibitor in late-stage development for PNH and in mid-stage trials for C3 glomerulopathy and other alternative pathway disorders.
Importantly, Omeros used the upfront cash to repay its 67.1M USD senior secured term loan and to prepare for redemption of remaining 2026 convertible notes, effectively removing a covenant-heavy debt overhang and extending runway beyond 12 months including the launch of YARTEMLEA.
From an equity-holder perspective, zaltenibart moves off the company’s direct spend line but remains a source of potential non-dilutive upside over the next decade, depending on Novo’s development success in PNH and kidney diseases.
4.3 Other programs – OMS527 and oncology
Beyond complement, Omeros runs a small but interesting set of programs:
- OMS527 (PDE7 inhibitor), in development for cocaine use disorder and funded by a multi-year grant from the U.S. National Institute on Drug Abuse. Preclinical interaction studies with cocaine have been completed, and an in-patient clinical study is targeted for 2026.
- An OncotoX platform focused initially on acute myeloid leukemia (AML), where early in vivo and non-human primate data suggest activity across multiple mutational subtypes.
- A T-CAT (targeted complement-activating therapy) program aimed at multi-drug resistant pathogens (bacteria, fungi, viruses), leveraging complement to directly kill pathogens.
None of these are near-term revenue sources, but they matter for the “what’s left after TA-TMA” question if YARTEMLEA becomes a durable cash engine.
5. Financial position and dilution history
Omeros’ balance sheet has been a constant source of stress for years. The combination of the Novo Nordisk deal and YARTEMLEA approval does not magically erase the past, but it does materially change the risk profile.
5.1 Q3 2025 snapshot
- Net loss Q3 2025: 30.9M USD (0.47 USD per share), versus 32.2M USD a year earlier.
- Non-GAAP adjusted net loss: 22.1M USD, excluding derivative fair-value changes.
- Cash + short-term investments: 36.1M USD as of Sept 30, 2025.
- Quarterly cash burn: ~22M USD (excluding financing).
- OMIDRIA royalties: ~9.2M USD in the quarter on 30.5M USD U.S. net sales (royalties largely monetized to DRI via escrow).
5.2 Equity raises and Novo cash
To bridge themselves to the PDUFA decision and the Novo transaction, Omeros resorted to both premium private placements and at-the-market issuance:
- July 2025: 5.37M shares sold to Polar Asset Management at 4.10 USD, a 14% premium to market, raising 20.3M USD net.
- Additional ~2.3M shares sold via ATM during Q3, bringing in another 9M USD, plus further ATM use after quarter-end.
These moves diluted existing holders but were effectively the price of survival while waiting for regulatory clarity. The Novo Nordisk upfront payment then allowed Omeros to repay its term loan at closing, release restrictive covenants and set up a cleaner runway into 2026.
5.3 Post-approval picture
After the YARTEMLEA approval and loan repayment, the financial story looks roughly like this:
- A cash balance substantially higher than the Q3 level once the 240M USD Novo upfront is fully reflected, minus debt repayment and transaction costs.
- Ongoing GAAP net losses until YARTEMLEA revenue and any additional milestones can offset R&D and SG&A.
- Still significant financing risk if launch uptake is slower than hoped or if broader macro conditions tighten – but far less existential than in 2021–2023.
For a TA-TMA-only scenario, Omeros can plausibly become a niche but self-funding company if U.S. and EU adoption reach critical mass. For a broader platform scenario (additional indications, OMS1029, oncology), they will likely continue to rely on selective partnerships and possibly further equity.
6. Analyst and retail sentiment
Sentiment sources considered here include analyst notes, Reddit discussion threads, Stocktwits streams,
X/Twitter commentary and user comments on finance portals. These are communities of non-professional traders:
noisy by design, useful only as a mood thermometer and never as investment research.
6.1 Street positioning
Ahead of the approval, Street research on Omeros had gradually migrated from outright skepticism to a more “option-like” framing: a small-cap biotech where value depended almost entirely on three conditions being met at the same time – YARTEMLEA approval, a label that transplant centers would actually use, and at least one sizeable business-development transaction.
With the FDA green light and the Novo Nordisk deal in hand, that triangle is now in place. What has not changed is the risk profile: analysts still describe OMER as a high-volatility name where quarterly numbers may swing with just a few dozen TA-TMA cases more or less, and where the quality of execution at hospital level matters as much as the headline label.
Price targets on main data aggregators remain all over the map. Some models assume that YARTEMLEA approaches functional “standard of care” status in TA-TMA and that MASP-2/3 become multi-indication platforms; others assume slower uptake, conservatively capped peak sales and a more limited contribution from pipeline assets. None of these scenarios is “the truth” – they simply illustrate how sensitive the equity value is to a thin layer of assumptions on incidence, diagnosis rates and real-world penetration.
6.2 What traders talk about (Reddit, Stocktwits, X)
In retail channels the conversation looks very different from formal research. In the weeks leading up to approval, OMER spent days among the most discussed biotech tickers on Stocktwits and Reddit. The key talking points were remarkably consistent:
- The “binary” nature of the event, with posts openly framing the trade as “approval and multi-bagger squeeze” versus “CRL and slow bleed”.
- The combination of small float, high historical short interest and long memory of the 2021 CRL, which created a narrative of “long-suffering longs finally getting their moment”.
- Comparisons with other orphan, hospital-based launches – some users citing examples where launch numbers surprised to the upside, others warning about overly optimistic case-count expectations.
After approval, the tone split into two camps. Enthusiastic longs emphasise the first-in-class mechanism, lack of direct competitors in TA-TMA and the presence of Novo as an external validation of the complement science. More cautious voices point out that TA-TMA is still underdiagnosed, that hospital economics can be slow to adapt, and that execution in a small ultra-orphan niche is very different from selling a broad chronic therapy.
Across Reddit and X there is also a subset of posts that barely mention TA-TMA at all and focus instead on intraday charts, options flow and short-term squeezes. That content can move price in the very short term but adds almost nothing to fundamental understanding of the story.
6.3 Sentiment takeaway
Putting it together, the sentiment picture is a bit paradoxical. On one hand, OMER has just delivered exactly what bulls had been waiting for: an approval in a setting with catastrophic unmet need plus a big-pharma deal that removes much of the financing overhang. On the other, a large portion of the retail audience is still treating the stock primarily as a vehicle for short-term volatility rather than as a long-duration complement platform.
Over the next 12–24 months, it would not be surprising to see the shareholder base slowly re-balance: fewer binary-event traders, more specialist funds watching centre-by-centre adoption, EMA timelines and the trajectory of the Novo-led MASP-3 program. For anyone following the name, separating that slow structural shift from the daily noise on social networks is likely to be more useful than tracking every chat-room spike.
7. Scenarios: what could the next 12–24 months look like?
Bull scenario
TA-TMA standard of care + EU tailwind
YARTEMLEA rapidly becomes de-facto standard in high-risk TA-TMA across major U.S. transplant centers, with strong adoption both first-line and as salvage after prior complement agents. NTAP and commercial payers support broad access. EMA grants approval on a label similar to the U.S., adding a second major region. YARTEMLEA generates meaningful, growing cash flows and Omeros can fund OMS1029 and key pipeline assets without aggressive dilution.
Base-case flavor
Gradual ramp, execution grind
Adoption is solid but not explosive; some centers move quickly, others wait for local protocols, real-world data and internal economic reviews. Reimbursement is available but administrative friction slows use in borderline cases. EMA approval arrives but launches are staggered across countries. YARTEMLEA provides meaningful revenue yet the company remains sensitive to trial timelines, payer decisions and macro liquidity.
Bear risks
Limited uptake or safety concerns
TA-TMA is recognized less frequently than expected, or centers rely heavily on alternative off-label strategies. Real-world outcomes diverge from trial data, or new safety signals emerge in broader practice, pressuring the label. EMA is less receptive than FDA or delays its decision. In this scenario, YARTEMLEA remains a scientifically important but commercially modest asset, and Omeros may eventually need more aggressive financing or further asset sales.
Disclosure: At the time of writing, the author holds a very small long position in Omeros (OMER). This position may be increased, reduced or fully closed at any time without notice and this article is not a recommendation to buy or sell the stock.
Other Merlintrader articles on Omeros:
Important disclaimer – informational only
This article is an independent editorial analysis based on public information (SEC filings, official company press releases, regulatory communications and reputable news outlets). It is intended solely for educational and informational purposes and does not constitute investment advice, solicitation, recommendation or invitation to buy or sell any financial instrument.
The issuer discussed here is a small/mid-cap biotechnology company with a high-risk profile: revenues are concentrated, the business is loss-making, clinical and regulatory setbacks are common and the stock price can be extremely volatile. Any investment decision should be taken independently, ideally with the support of a qualified financial advisor, and considering your own risk tolerance and objectives.
Nothing in this report should be interpreted as a guarantee of future performance or as a forecast. Regulatory environments (including FDA, EMA, CONSOB and SEC frameworks), clinical practice standards and market conditions can change quickly and materially.
Some external links may refer to partners or tools with which Merlintrader trading Blog may have referral or affiliate agreements (for example Finviz, Seeking Alpha, Stocktwits and similar platforms). If you subscribe or purchase services through those links, the site may receive a commission; this never changes your price as an end user.
Omeros Corporation – NASDAQ: OMER
YARTEMLEA approvato dalla FDA: prima terapia per la TA-TMA e nuovo capitolo per Omeros
La FDA ha approvato YARTEMLEA (narsoplimab-wuug) come prima e unica terapia per la trombotica microangiopatia associata a trapianto di cellule staminali (TA-TMA) negli adulti e nei bambini dai 2 anni in su. Qui analizziamo che cosa dice davvero la label, quali dati la sostengono, come è impostato il lancio e che impatto ha il deal con Novo Nordisk.
Prezzo recente (indicativo)
~9–10 USD per azione
Seduta molto volatile intorno all’annuncio.
Market cap (range)
~650–700M USD
Small/mid cap ad alta beta.
Stato
FDA approvato – TA-TMA
Lancio USA previsto per gennaio 2026.
I numeri sono uno snapshot approssimativo intorno alla data di approvazione e possono cambiare rapidamente con il mercato.
News del giorno – approvazione FDA
La FDA ha approvato YARTEMLEA (narsoplimab-wuug) per il trattamento della trombotica microangiopatia associata a trapianto di cellule staminali ematopoietiche (TA-TMA) negli adulti e nei bambini di età pari o superiore a 2 anni. YARTEMLEA è il primo e unico inibitore approvato della via lectinica del complemento e, soprattutto, la prima terapia approvata per la TA-TMA.
L’approvazione si basa su uno studio pivotale open-label a braccio singolo in adulti con TA-TMA (N=28) e sui dati del programma di uso compassionevole globale (EAP; N=221), con tassi di risposta completa intorno al 61–68% e sopravvivenza a 100 giorni intorno al 73–74% in una popolazione uniformemente ad altissimo rischio. Il profilo di sicurezza è coerente con quello dei pazienti trapiantati in generale, ma infezioni gravi e sepsi restano rischi centrali e sono ben evidenziati nella scheda tecnica.
Executive summary – che cosa cambia davvero per OMER
Con l’approvazione di YARTEMLEA, Omeros esce dal limbo del “tutto o niente al PDUFA” e torna ad essere, di fatto, una società con un prodotto complement approvato e lanciabile. La label è ampia per un’indicazione così rara e severa: adulti e bambini ≥2 anni, nessun black-box inatteso e dati di efficacia supportati sia dal trial pivotale sia dall’esperienza real-world dell’EAP.
L’ok della FDA si aggiunge a un accordo fino a 2,1 miliardi di dollari con Novo Nordisk sull’inibitore MASP-3 zaltenibart (OMS906), che ha già portato 240M USD di upfront, consentendo a Omeros di rimborsare il term loan e alleggerire in modo deciso il bilancio. Insieme, cash da Novo e lancio di YARTEMLEA spostano il caso da “rischio esistenziale” a “storia di esecuzione ad alto beta”.
Questo non rende OMER improvvisamente “sicura”: YARTEMLEA vive in un mercato ultra-orphan, ospedaliero, che dipende da volumi di trapianto, protocolli interni dei centri, scelte dei payers e andamento dei casi reali. La società è ancora in perdita, il flottante è relativamente contenuto e la volatilità resta strutturalmente elevata.
Prima terapia approvata per TA-TMA
Meccanismo lectin pathway first-in-class
Mercato ultra-orphan ospedaliero
Rischio infezioni/sepsi importante
Storico di burn e diluizione aggressiva
1. Cosa ha approvato esattamente la FDA?
1.1 Indicazione e scheda tecnica
YARTEMLEA è approvato per il trattamento della trombotica microangiopatia associata a trapianto di cellule staminali ematopoietiche (TA-TMA) negli adulti e nei bambini dai 2 anni in su. Si tratta di un anticorpo monoclonale umano che inibisce selettivamente MASP-2, l’enzima effettore della via lectinica del complemento, bloccando l’attivazione della via lectinica e preservando le vie classica e alternativa.
Questo è il punto chiave: a differenza degli inibitori C3/C5, l’inibizione di MASP-2 mira a ridurre la TMA e il danno endoteliale senza spegnere completamente il sistema del complemento. La label riconosce YARTEMLEA come primo e unico inibitore approvato della via lectinica e unica terapia approvata per TA-TMA.
1.2 Il pacchetto dati
L’approvazione poggia su:
- Uno studio pivotale open-label a braccio singolo in adulti con TA-TMA ad alto rischio (N=28).
- Dati aggiuntivi dal programma di uso compassionevole (EAP), che ha arruolato 221 pazienti adulti e pediatrici; 19 di questi (13 adulti, 6 pediatrici) avevano dati di risposta valutabili.
L’endpoint primario era la risposta completa (CR), definita come miglioramento dei marker di TMA (piastrine e LDH) insieme a miglioramento della funzione d’organo o indipendenza dalle trasfusioni. YARTEMLEA ha ottenuto:
- 17/28 CR (61%) nello studio TA-TMA negli adulti.
- 13/19 CR (68%) tra i pazienti valutabili dell’EAP.
Sul fronte sopravvivenza, la sopravvivenza a 100 giorni dalla diagnosi di TMA è stata di circa 73–74% tra trial ed EAP, in una popolazione in cui la mortalità storica della TA-TMA severa può superare il 90%. Analisi pubblicate in peer-review hanno mostrato una riduzione del rischio di morte di 3–4 volte rispetto a coorti esterne trattate con terapia di supporto standard.
1.3 Sicurezza
Il profilo di sicurezza riflette più lo stato clinico dei pazienti trapiantati che il farmaco in sé:
- Infezioni gravi in circa un terzo dei pazienti, incluse sepsi, polmoniti, batteriemie, infezioni fungine e virali.
- Reazioni avverse più comuni (≥20%): infezioni virali, sepsi, emorragia, diarrea, vomito, nausea, neutropenia, febbre, affaticamento, ipokaliemia.
- Reazioni avverse gravi nel ~61% dei pazienti; reazioni fatali nel ~7% (principalmente sepsi neutropenica e shock settico).
Dal punto di vista commerciale è importante che la scheda tecnica non introduca warning “a sorpresa” rispetto a ciò che i centri trapianto già gestiscono quotidianamente, ma formalizzi l’esigenza di monitoraggio stretto delle infezioni in corso di trattamento.
2. TA-TMA e dimensione del mercato
La TA-TMA è una delle complicanze più temute del trapianto di cellule staminali. Origina da un danno endoteliale diffuso innescato da condizionamento, immunosoppressori, GVHD, infezioni e altri fattori legati al trapianto; la via lectinica del complemento e MASP-2 giocano un ruolo centrale nella cascata.
Gli elementi chiave per il mercato sono:
- Circa 30.000 trapianti allogenici all’anno tra USA ed Europa.
- Studi recenti stimano che la TA-TMA possa svilupparsi fino nel 50–56% dei trapiantati allogenici, se si considerano tutte le forme, anche se solo una quota ristretta rientra nei criteri ad alto rischio.
- Nelle forme severe ad alto rischio, la mortalità storica può superare il 90%, con molti sopravvissuti che rimangono con danno renale cronico o dialisi.
Fino a oggi non esisteva una terapia on-label. I centri si muovevano fra:
- Misure di supporto e modifica degli immunosoppressori.
- Uso off-label di inibitori del complemento, soprattutto C5-blocker.
- Defibrotide in alcuni contesti, senza standard condivisi.
YARTEMLEA arriva come unica opzione approvata e rimborsabile con codice ICD-10 e CPT dedicati. Questo, in pratica, crea un percorso terapeutico strutturato: se il centro riconosce una TA-TMA ad alto rischio, ha ora una terapia on-label con un razionale biologico forte e dati di sopravvivenza difficili da ignorare.
3. Preparazione al lancio
3.1 Organizzazione commerciale
Omeros ha costruito l’infrastruttura commerciale USA prima della decisione:
- Una prima ondata di specialisti con esperienza specifica in ematologia e centri trapianto.
- Scambi informativi pre-approval con KOL, direttori di programmi trapianto e payers, che la società descrive come “costantemente incoraggianti”.
- Brand definito: narsoplimab viene commercializzato come YARTEMLEA nella TA-TMA.
3.2 Rimborso
Il lancio parte con una base di rimborsabilità già predisposta:
- ICD-10-CM M31.11 per la TA-TMA post trapianto.
- Codici procedurali ICD-10-PCS XW03357/XW04357 per la somministrazione endovenosa dell’anticorpo.
- Richiesta di NTAP in ambito Medicare per aiutare gli ospedali a coprire il costo del farmaco rispetto al DRG.
Inoltre sarà attivo il programma di supporto YARTEMLEAssist, che si occuperà di verifiche assicurative, prior authorization e potenziale supporto economico ai pazienti.
3.3 Europa e oltre
In parallelo è in corso la revisione dell’MAA presso EMA, con opinione attesa intorno alla metà del 2026. Un parere positivo aprirebbe un secondo bacino importante di centri trapianto in Europa.
Nel breve il focus è il lancio USA di gennaio 2026. I numeri da seguire saranno:
- Quanti centri trapianto inseriscono YARTEMLEA nei protocolli TA-TMA.
- Percentuale di uso in prima linea vs salvataggio dopo altri complement agent.
- Velocità e qualità delle decisioni di rimborso di payers pubblici e privati.
4. Pipeline oltre YARTEMLEA e accordo con Novo Nordisk
4.1 Franchising MASP-2
YARTEMLEA è solo il primo tassello della piattaforma MASP-2. Alle sue spalle c’è OMS1029, inibitore MASP-2 long-acting che ha completato la fase 1 e che può diventare il “workhorse” per indicazioni aggiuntive a cavallo tra nefrologia e immunologia.
4.2 MASP-3 e zaltenibart (OMS906)
Con zaltenibart, Omeros ha scelto di monetizzare e de-rischiare. L’accordo con Novo prevede:
- 240M USD di upfront già incassati.
- Fino a 100M USD di milestone a breve termine.
- Un totale potenziale di 2,1 miliardi fra milestone di sviluppo/approvazione e di vendita.
- Royalties a scalini sulle vendite globali.
Il cash upfront è stato usato per rimborsare i 67,1M USD di term loan, chiudere il contratto di credito, rimuovere covenant stringenti e preparare il rimborso delle rimanenti convertibili 2026. Di fatto, gran parte del rischio “liquidità a breve” è stato trasferito su Novo in cambio di upside futuro sotto forma di milestone e royalty.
4.3 OMS527 e oncologia
Completano il quadro:
- OMS527 (PDE7) per disturbo da uso di cocaina, con grant NIDA che copre parte dei costi di sviluppo.
- Piattaforma OncotoX su leucemia mieloide acuta (AML) con dati preclinici incoraggianti e ingresso in clinica previsto tra 18–24 mesi.
- Programma T-CAT su patogeni multi-resistenti, ancora in fase preclinica ma in un’area di forte interesse regolatorio.
5. Situazione finanziaria e diluizione
5.1 Q3 2025
- Perdita netta: 30,9M USD (0,47 USD/azione).
- Perdita netta non-GAAP: 22,1M USD.
- Cassa + investimenti a breve: 36,1M USD.
- Cash burn: ~22M USD nel trimestre (esclusi flussi di finanziamento).
- Royalties OMIDRIA: ~9,2M USD nel trimestre, ma sostanzialmente monetizzate a DRI.
5.2 Aumenti di capitale e accordo Novo
Nel 2025 Omeros ha combinato:
- Un private placement a premio con Polar (5,37M azioni a 4,10 USD).
- Vendite ATM per circa 2,3M di azioni nel solo Q3.
- Il maxi-accordo con Novo da 240M USD upfront.
Il risultato è una base azionaria più diluita ma una struttura finanziaria meno fragile: niente più term loan con covenant minimi di cassa e un orizzonte di cassa post-closing superiore ai 12 mesi, incluso il lancio iniziale di YARTEMLEA.
5.3 Dopo l’approvazione
Dopo l’ok della FDA, il quadro è quello di una small/mid-cap biotech ancora in perdita ma con:
- Un asset approvato in un’area ultra-orphan con forte unmet need.
- Un deal strutturato con big pharma (Novo) che può generare flussi non diluitivi nel medio/lungo termine.
- Un rischio finanziario che dipende ora dalla velocità del ramp di YARTEMLEA e dalla disciplina sulla spesa, più che dalla mera sopravvivenza a breve.
6. Sentiment analisti e retail
Le considerazioni di questa sezione si basano su note degli analisti, thread su Reddit, flussi
di messaggi su Stocktwits, commenti su X/Twitter e sezioni commenti di alcuni portali finanziari.
Si tratta di comunità popolate in gran parte da trader non professionisti: sono utili come termometro
dell’umore, non come ricerca o analisi da seguire ciecamente.
6.1 Posizionamento della “Street”
Prima dell’approvazione il consensus degli analisti si era spostato da un pessimismo marcato a una lettura più “optionalità pura”: una small-cap biotech il cui valore dipendeva dal verificarsi di tre condizioni insieme – approvazione di YARTEMLEA, scheda tecnica davvero utilizzabile nei centri trapianto e almeno un accordo corposo di business development.
Con il via libera FDA e il deal con Novo, quel trittico ora esiste. La parte che non cambia è il profilo di rischio: molti commenti di ricerca continuano a descrivere OMER come titolo ad alta volatilità, dove basta che pochi casi TA-TMA in più o in meno si concentrino in un trimestre per alterare parecchio i numeri, e dove l’esecuzione pratica nei centri ospedalieri pesa quanto la label.
I target price sui principali data provider restano molto dispersi. Alcuni modelli assumono che YARTEMLEA sfiori lo status di “standard of care” in TA-TMA e che MASP-2/MASP-3 diventino piattaforme multi-indicazione; altri si fermano a scenari più prudenti con uptake graduale, picchi di vendita limitati e contributo modesto dagli asset più lontani in pipeline. Più che numeri da prendere come verità, sono griglie di lettura di quanto l’equity sia sensibile a variabili piccole (incidenza, diagnosi, penetrazione reale).
6.2 Cosa dicono i retail (Reddit, Stocktwits, X)
Sulle community retail il tono è molto più diretto. Nelle settimane pre-approvazione OMER è stato a lungo tra i biotech più discussi su Stocktwits e Reddit. I temi ricorrenti:
- La narrazione del “trade binario”, con post che parlano apertamente di scenario “approvazione + short squeeze” contro scenario “CRL e lento logoramento”.
- Il mix di flottante non enorme, storico di short interest elevato e memoria lunga della CRL 2021, che alimenta il racconto dei “long di vecchia data finalmente premiati”.
- I paragoni con altri lanci in ambito orphan ospedaliero: da un lato esempi di ramp migliori delle attese, dall’altro warning di chi ricorda casi in cui le proiezioni sulla numerosità dei pazienti erano chiaramente troppo ottimistiche.
Dopo l’approvazione il flusso si polarizza. Da una parte ci sono i post euforici che puntano sul fatto che si tratti della prima terapia approvata per TA-TMA, con un meccanismo molto specifico e un unmet need difficile da contestare. Dall’altra ci sono commenti più freddi che ricordano come TA-TMA sia ancora oggi sotto-diagnosticata, che molti centri potrebbero muoversi con prudenza e che la dinamica economica dei DRG ospedalieri è tutto tranne che lineare.
Su Reddit e X non mancano poi thread che quasi ignorano il quadro clinico e si concentrano solo su grafici intraday, flussi di opzioni e potenziale di squeeze. Utili per capire dove si accumula il trading a breve respiro, ma poco interessanti per chi prova a seguire la storia su orizzonti più lunghi.
6.3 Cosa ci dice davvero il sentiment
Nel complesso, il quadro è duplice. Dal punto di vista fondamentale, Omeros ha appena messo sul tavolo due tasselli che molti consideravano indispensabili per la sopravvivenza a medio termine: un’approvazione in un ambito ultra-orphan con dati solidi e un partner big pharma che ha già scritto un assegno importante.
Sul fronte del mood, però, una fetta consistente del pubblico continua a trattare OMER più come un veicolo di volatilità che come una “platform story” sul complemento. È probabile che nei prossimi 12–24 mesi la base azionaria si riassetti gradualmente: meno trader da evento binario, più fondi specialistici interessati a metriche come numero di centri attivi, andamento delle richieste di rimborso, newsflow EMA e progressi di Novo su zaltenibart.
Per chi segue il titolo, distinguere questo lento ribilanciamento di fondo dal rumore quotidiano sui social probabilmente conterà più che inseguire ogni spike intraday sul flusso dei commenti.
7. Possibili scenari a 12–24 mesi
Scenario positivo
Standard of care + Europa
YARTEMLEA diventa rapidamente standard di cura nei casi TA-TMA ad alto rischio nei grandi centri trapianto USA; il rimborso è ampio e relativamente fluido e l’EMA approva un’indicazione simile. In questo contesto il farmaco può generare flussi tali da rendere Omeros sostanzialmente autosufficiente e finanziare buona parte del resto della pipeline.
Scenario intermedio
Ramp graduale, execution story
Adozione buona ma non esplosiva, con centri “early adopter” e altri più lenti che attendono dati real-world e linee guida interne. Il rimborso c’è ma con burocrazia pesante in alcuni sistemi. EMA approva ma i lanci nazionali sono a macchia di leopardo. OMER resta un titolo sensibile ai numeri trimestrali e al newsflow regolatorio.
Scenario negativo
Uptake limitato o problemi di sicurezza
La TA-TMA viene diagnosticata meno del previsto, oppure i centri preferiscono continuare a usare off-label altri approcci. Dati real-world meno convincenti del trial o nuovi segnali di safety frenano la fiducia. L’EMA è più fredda o introduce restrizioni. In questo caso YARTEMLEA resta un progresso clinico importante ma con impatto economico limitato, e la società potrebbe dover tornare a finanziare la pipeline con ulteriore diluizione o nuove cessioni.
Disclosure: Al momento della pubblicazione l’autore detiene una posizione long molto piccola su Omeros (OMER). Tale posizione può essere aumentata, ridotta o chiusa in qualunque momento senza preavviso e questo articolo non costituisce in alcun modo un invito o consiglio a comprare o vendere il titolo.
Altri articoli Merlintrader dedicati a Omeros:
Disclaimer importante – nessun consiglio finanziario
Questo articolo è una sintesi editoriale indipendente basata su informazioni pubbliche (SEC filing, comunicati ufficiali della società, documenti regolatori e principali fonti news). È pensato esclusivamente a scopo informativo e didattico e non costituisce in alcun modo raccomandazione, consulenza o sollecitazione all’investimento.
Le small/mid-cap biotech sono per definizione titoli ad alto rischio: business in perdita, forte dipendenza da singoli studi e singole decisioni regolatorie, volatilità elevata e possibile perdita integrale del capitale investito. Ogni decisione operativa andrebbe presa in autonomia, idealmente con il supporto di un consulente abilitato e tenendo conto della propria situazione personale.
Alcuni link presenti nel testo possono rimandare a strumenti o piattaforme con cui Merlintrader trading Blog ha accordi di affiliazione (Finviz, Seeking Alpha, Stocktwits, ecc.). Se l’utente sottoscrive servizi tramite questi link, il sito può ricevere una commissione; per l’utente finale il prezzo non cambia.
Biotech Catalyst Calendar
Vuoi seguire in anticipo le prossime PDUFA, letture di fase 2/3 e date chiave come quella di YARTEMLEA? Nella pagina dedicata trovi il calendario aggiornato dei catalyst biotech curato da Merlintrader.
Disclosure (EN): At the time of writing, the author holds a very small long position in Omeros (OMER). This position may be increased, reduced or fully closed at any time without notice and this article is not a recommendation to buy or sell the stock.
Disclosure (IT): Al momento della pubblicazione l’autore detiene una posizione long molto piccola su Omeros (OMER). Tale posizione può essere aumentata, ridotta o chiusa in qualunque momento senza preavviso e questo articolo non costituisce in alcun modo un invito o consiglio a comprare o vendere il titolo.
Other Merlintrader articles on Omeros:
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


