DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
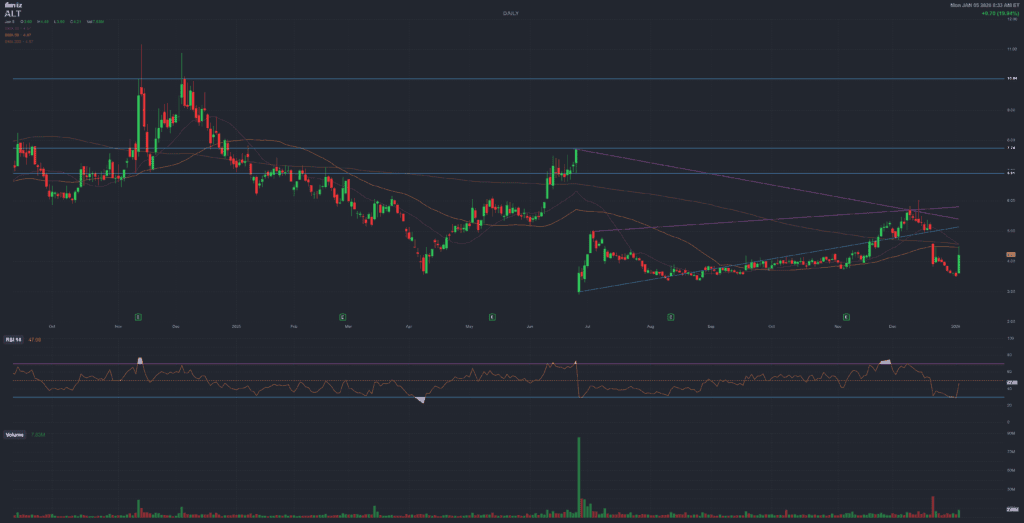
Altimmune (ALT) – Pemvidutide gets Breakthrough Therapy in MASH
Post–FDA news update (Breakthrough Therapy Designation) and impact on Altimmune’s equity story.
Key message: the FDA has granted Breakthrough Therapy Designation (BTD) to pemvidutide for the treatment of MASH, based on 24-week data from the Phase 2b IMPACT trial (company press release, Jan 5 2026 and IMPACT publication).
The stock immediately reacts with an intraday move around +15–20% (as reported by outlets like Seeking Alpha and Investing.com). This is not a random bounce, it is a repricing of regulatory risk.
1. Executive summary – ALT moves up a league
Today Altimmune’s story makes a real step up, not a cosmetic one.
- The FDA grants Breakthrough Therapy Designation to pemvidutide in MASH (BTD PR).
- The designation is based on the 24-week IMPACT Phase 2b data, where pemvidutide showed:
- resolution of MASH with no worsening of fibrosis,
- strong reductions in liver fat,
- improvements in non-invasive markers of inflammation and fibrosis (Lancet IMPACT paper and Altimmune IR).
- Altimmune also confirms a positive end-of-phase 2 meeting with the FDA and alignment on a registrational design (EoP2 PR):
- alignment on a 52-week registrational Phase 3,
- patients with F2–F3 fibrosis,
- biopsy-based endpoints supported by the AIM-MASH AI Assist system (described as the first FDA-qualified AI pathology tool for MASH trials in the BTD release and follow-up coverage, ad es. BTD PR, StockTitan summary).
From “interesting but debated program” after the 48-week data, we move to a program that the FDA explicitly decides to handle in fast-track mode. That is a category change.
2. What Breakthrough Therapy Designation really means
Breakthrough Therapy Designation is not a cosmetic label. It is one of the strongest regulatory tools the FDA has (FDA guidance).
- It is reserved for drugs that treat serious diseases and show preliminary clinical evidence of substantial improvement over available therapies on clinically meaningful endpoints.
- It includes:
- all the benefits of Fast Track,
- direct involvement of senior FDA management,
- higher probability of priority review and accelerated approval pathways, if the data support it (Friends of Cancer Research report).
On timelines, an FDA-sponsored analysis found that BTD programs show roughly a 30% reduction in late-stage development time compared to non-BTD drugs (HHS / ASPE analysis).
Concrete implications for pemvidutide:
- Time – late-stage development (EoP2 → approval) is statistically faster for BTD drugs.
- Quality of FDA interactions – intensive, structured guidance instead of a “normal” hands-off process.
- Perceived risk – the question “does the FDA really care about this asset?” goes down a notch in importance.
It does not mean approval is guaranteed, but it does mean that the clinical and regulatory potential has been formally recognized.
3. MASH timeline – from 24 weeks to BTD
3.1 IMPACT Phase 2b – 24 weeks
In the IMPACT Phase 2b trial in MASH patients, at 24 weeks pemvidutide delivered (Altimmune IR, Lancet paper):
- MASH resolution with no worsening of fibrosis in a clearly higher proportion of patients versus placebo, with strong statistical significance.
- Clear improvements in non-invasive tests:
- reduction in liver fat content (MRI-PDFF),
- declines in ELF, LSM and other NITs of inflammation/fibrosis,
- a favorable overall tolerability profile.
- For biopsy-based fibrosis (≥1 stage improvement) the signal was present but not yet statistically clean versus placebo at 24 weeks.
These 24-week data are explicitly cited in the BTD press release as the basis for granting Breakthrough Therapy Designation (BTD PR).
3.2 IMPACT – 48 weeks and market reaction
On 19 December 2025 Altimmune released the 48-week IMPACT data (48-week PR):
- further improvements in NITs (ELF, LSM, cT1, ALT),
- additional weight loss, particularly at the 1.8 mg dose,
- safety and tolerability remaining overall acceptable.
The market, however, punished the stock with a roughly −20% drawdown because:
- no new long-term fibrosis biopsy data were provided at that time,
- there was limited public detail on end-of-phase 2 outcomes,
- no partnership headline arrived to offset the disappointment.
3.3 5 January 2026 – Breakthrough and Phase 3 alignment
Today’s news closes that loop:
- the FDA grants Breakthrough Therapy Designation for MASH, explicitly citing the 24-week IMPACT data (BTD PR),
- Altimmune states it has received the official end-of-phase 2 meeting minutes and is aligned on:
- a 52-week registrational Phase 3,
- patients with F2–F3 fibrosis,
- biopsy-based endpoints using AIM-MASH AI Assist as AI pathology support (48-week PR, StockTitan).
The pemvidutide MASH program moves from “interesting but uncertain” to a program explicitly recognized by the FDA as worthy of an accelerated, high-touch pathway.
4. Scientific profile – beyond weight loss
4.1 Mechanism of action: dual GLP-1 / glucagon 1:1
Pemvidutide is a dual GLP-1 / glucagon receptor agonist with a balanced 1:1 activity ratio. The company summarizes this clearly in its R&D updates (May 13 2025 corporate update, pipeline page):
- GLP-1:
- reduces appetite,
- slows gastric emptying,
- improves glycemic control.
- Glucagon:
- increases fatty-acid oxidation,
- acts directly on hepatic fat metabolism,
- may improve triglycerides, LDL and fibrotic pathways.
The goal is not just weight loss, but to attack liver disease at its core, combining systemic metabolic effects with a direct hepatic effect.
4.2 Obesity data – MOMENTUM
In the MOMENTUM obesity trial, pemvidutide delivered robust results (MOMENTUM 48-week PR, topline PDF):
- mean weight loss of around 15.6% at the 2.4 mg dose at Week 48,
- good lean-mass preservation,
- reductions in triglycerides, LDL, liver fat and blood pressure.
This supports the idea of a single asset connecting obesity and MASH, which is strategically attractive.
4.3 MASH data – what we really have
In short:
- 24 weeks:
- MASH resolution as primary endpoint clearly hit,
- strong improvements in NITs,
- fibrosis signal present but not yet statistically clean in biopsy.
- 48 weeks:
- reinforcement of ELF, LSM, cT1 and inflammation markers,
- additional liver-fat reduction,
- continued weight loss, especially at 1.8 mg,
- tolerability essentially preserved (48-week PR).
- Regulatory status:
- Fast Track for MASH (granted in 2025, corporate update and Fast Track PR),
- Fast Track also for AUD, and now Breakthrough Therapy Designation for MASH (BTD PR).
The combined message is clear: the totality of efficacy + safety + NIT data is strong enough for the FDA to justify an accelerated pathway.
5. Competitive positioning in MASH
The MASH landscape is extremely competitive:
- Rezdiffra (resmetirom, Madrigal):
- first drug approved for NASH/MASH with F2–F3 fibrosis in March 2024 (FDA PR, Madrigal IR).
- Wegovy (semaglutide, Novo Nordisk):
- GLP-1 agonist with accelerated approval for MASH with moderate-to-advanced fibrosis granted in August 2025 (FDA MASH Wegovy page, Biochempeg summary, Nature Biotechnology note).
- Other pipelines:
- GLP-1 / GIP combos (tirzepatide, VK2735, etc.),
- FGF21 analogs (e.g. pegozafermin),
- other hepatic and metabolic mechanisms, as tracked in recent MASH-pipeline reviews.
Where can pemvidutide fit?
- Combined mechanism: weight plus direct hepatic effect via glucagon.
- Dual MASH + obesity positioning: attractive for overweight MASH patients needing both systemic and liver-specific benefit.
- BTD + Fast Track: in such a crowded field, having Breakthrough status places pemvidutide in the shortlist of FDA-prioritized programs.
MASH is not a “winner takes all” market. The patient pool is huge, with heterogeneous comorbidities. For a dual GLP-1/glucagon with strong liver signals and competitive weight loss, there is clearly room, and today’s BTD is the FDA’s way of saying this program is worth that race.
6. Financial structure – cash, burn, dilution risk
6.1 Cash and balance sheet
From the latest quarterly disclosures:
- Altimmune reported approximately $210.8 million in cash, cash equivalents, restricted cash and short-term investments as of September 30, 2025 (Q3 2025 financial results PR, Q3 10-Q).
- The company remains in a net cash position, with total liabilities materially below cash and short-term investments in recent balance sheets (see 10-Q and prior quarter filings such as the Q1 2025 10-Q excerpt here).
6.2 Cash burn and runway
An AI-assisted analysis on Fintel, based on the Q3 2025 10-Q, estimates:
- operating cash burn of roughly $11.9M for Q3 2025 (derived from the nine-month cash flow data in the 10-Q),
- a theoretical cash runway of around 4.4 years if that quarterly burn rate persisted unchanged (Fintel AI+ note).
Realistically, Phase 3 in MASH plus AUD/ALD and obesity work will drive burn higher, so actual runway is likely shorter than the “straight-line 4.4 years” scenario—but the starting point is clearly multi-year, not a six-month cash crunch.
6.3 Equity raise risk
The less pleasant side of the bull case is dilution risk:
- a significant shelf registration is already in place (see SEC filings on S-3 and ATM structures in the 10-K/10-Q stack),
- with BTD in hand and very positive news, management has a clear incentive to fund Phase 3 from a position of strength,
- a sharp rally like today is a classic window for potential equity offerings.
The qualitative value of today’s news does not change, but investors should keep the likelihood of further equity issuance in mind.
7. Ownership – insiders, institutions, retail
7.1 Shareholder structure
Aggregated ownership data (e.g. Simply Wall St, Fintel and others) show a familiar pattern:
- Insiders: low single-digit percentage of shares.
- Institutions: meaningful, but not controlling stake (dozens of funds and asset managers in 13F filings).
- Public/retail: the majority of the register, consistent with trading volumes and Stocktwits/Reddit traffic around ALT.
This is consistent with what you see on Yahoo Finance, Nasdaq and various ownership dashboards.
In practice, that mix means:
- high volatility,
- sharp reactions to data and headlines,
- strong sensitivity to short-term sentiment.
7.2 Insider activity
Recent ownership snapshots and insider-transactions digests (SEC Form 4, summarized on services like Fintel or MarketBeat) show more insider buying than selling over the last few months, from a low base. It is not a 20–30% insider fortress, but in a volatile period post-48w, insider net buying is a directionally positive signal.
8. Sell-side analysts – where consensus stands
Across public sources, analyst consensus is clearly positive:
- average rating in the “Buy” / “Strong Buy” range,
- median price targets:
- around $17–18 in some aggregators (e.g. Investing.com consensus),
- well above pre-news levels even after today’s move, in line with upside scenarios published on various platforms (TipRanks, MarketBeat, etc.).
- several notes after the 48-week read-out already argued that:
- the data were scientifically coherent and strong,
- the main issue was a disconnected market reaction, not the intrinsic quality of the program.
Today’s BTD essentially validates that reading: the dataset did not change; the regulatory validation did.
9. Retail sentiment – Stocktwits, Reddit and the crowd
9.1 Stocktwits – a “hot” ticker for months
On Stocktwits and related sentiment trackers (sentiment page), ALT has been one of the high-buzz names in the MASH/obesity complex for months:
- 24-week IMPACT and obesity data spikes drove “extremely bullish” sentiment scores and heavy message volume.
- post-48w, sentiment turned noisy as the stock sold off despite positive NITs.
- with BTD, the feed is again dominated by “validation from FDA”, “BTD + Fast Track = AA path” type narratives.
9.2 Reddit – scientific DD and funding risk
On r/Altimmune and related threads you see:
- deep dives on GLP-1/glucagon biology and IMPACT data (e.g. posts discussing the Lancet paper and IMPACT publication links),
- scenario modeling for MASH commercialization with Phase 3 start in 2026, 52-week duration and AA vs full-approval timelines (commercialization scenarios thread),
- funding/dilution threads explicitly noting the 210.8M cash figure and the BTD inflection (“Funding” thread).
The more serious Reddit crowd is broadly aligned on this thesis:
“Pemvidutide has strong MASH resolution, competitive weight loss, fibrosis signals in the making and a MASH + obesity + AUD/ALD axis. The key issue was alignment with the FDA. With BTD and a defined Phase 3, the inflection point is real.”
10. Main risks (without downgrading today’s news)
Even in a bull-toned piece, risks are real:
- Phase 3 execution:
- long, costly, complex trial (52 weeks, biopsies, AI pathology, F2–F3 population),
- recruitment, safety or endpoint issues can generate severe drawdowns.
- Competition:
- Rezdiffra and Wegovy are already on the market with growing real-world datasets and guideline presence,
- pemvidutide must show clear added value (efficacy, tolerability, combo potential, subgroups) to earn its place.
- Funding and dilution:
- solid, but not infinite cash (see Q3 10-Q and Fintel runway analysis),
- Phase 3 + multiple programs are expensive,
- large shelf means dilution risk is structural.
- Retail-driven volatility:
- retail-heavy ownership structure,
- high sensitivity to newsflow and social sentiment,
- history of overshooting both ways.
These risks were there yesterday and will be there tomorrow. What changes today is that a major chunk of regulatory uncertainty has been reduced.
11. Final take – why BTD is a true bull turning point for ALT
Putting data, regulatory, financials and sentiment together:
- Clinical data:
- 24 weeks: strong MASH resolution, favorable NITs, good safety,
- 48 weeks: reinforced antifibrotic signals and weight-loss profile.
- Regulatory:
- Fast Track already in place for MASH and AUD,
- now Breakthrough Therapy in MASH,
- 52-week registrational Phase 3 agreed with biopsy endpoints and AI pathology.
- Financials:
- net-cash company (~210.8M cash + investments at Q3 2025),
- multi-year runway on current burn, even before any potential raise,
- room to raise capital from a stronger position if sentiment stays constructive.
- Ownership & sentiment:
- retail majority with meaningful institutional base,
- ALT has been one of the flagship names in the MASH/obesity theme,
- BTD shifts perception from “controversial story” to “asset with a strong FDA stamp”.
In practical terms:
The FDA just put an official stamp on pemvidutide in MASH. That raises the quality of the story, removes a meaningful chunk of regulatory risk and redraws the potential trajectory for the stock.
Today’s double-digit move is not a random pump. It is a logical re-valuation as the perceived probability of regulatory success moves higher than it was yesterday.
Other Altimmune (ALT) articles on Merlintrader trading Blog
For readers who want the full pemvidutide/ALT history, here are all the related pieces published so far:
- ALT Altimmune, Inc. – Pemvidutide Late-Stage Clinical Biotech (main deep dive)
- ALT Altimmune Update Dec 3 – Pivotal phase and converging drivers
- ALT Altimmune Update Dec 12 – 48-week countdown, CEO change and GLP-1 context
- ALT Altimmune Inc 22 Dec Update – IMPACT 48w post-mortem (−20% after data)
- Anti-obesity Drugs And Weight-loss Therapies – GLP-1 / dual-agonist overview (pemvidutide section)
Altimmune (ALT) – Pemvidutide ottiene la Breakthrough Therapy in MASH
Aggiornamento post–news FDA (Breakthrough Therapy Designation) e impatto sulla equity story di Altimmune.
Messaggio chiave: la FDA ha concesso a pemvidutide la Breakthrough Therapy Designation (BTD) per il trattamento della MASH, sulla base dei dati a 24 settimane dello studio di Phase 2b IMPACT (comunicato ufficiale BTD e pubblicazione IMPACT).
Il titolo reagisce subito con un movimento intraday nell’ordine di +15–20% (come riportato da fonti come Seeking Alpha e Investing.com). Non è un rimbalzo casuale: è una ri-valutazione del rischio regolatorio.
1. Executive summary – ALT cambia livello
Oggi la storia di Altimmune fa uno scatto in avanti reale, non cosmetico.
- La FDA concede la Breakthrough Therapy Designation a pemvidutide per la MASH (PR BTD).
- La designazione arriva sulla base dei dati a 24 settimane dello studio IMPACT di Phase 2b, dove pemvidutide ha mostrato:
- risoluzione di MASH senza peggioramento della fibrosi,
- riduzione marcata del grasso epatico,
- miglioramenti dei marker non invasivi di infiammazione e fibrosi (articolo sul Lancet e IR Altimmune).
- Altimmune conferma anche un end-of-phase 2 meeting positivo con la FDA e l’allineamento su un disegno registrativo (PR EoP2):
- Phase 3 registrativo di 52 settimane,
- pazienti con fibrosi F2–F3,
- endpoint bioptici supportati dal sistema AIM-MASH AI Assist, indicato nei comunicati come primo strumento di patologia AI qualificato dalla FDA per trial MASH (PR 48w, StockTitan).
Da “programma interessante ma discusso” dopo i 48w, si passa a un programma che la FDA decide di gestire con approccio accelerato e ad alta interazione. È un cambio di categoria.
2. Cosa significa davvero la Breakthrough Therapy Designation
La Breakthrough Therapy Designation non è un semplice bollino estetico: è uno degli strumenti regolatori più forti che la FDA ha a disposizione (guidance FDA).
- È riservata a farmaci che trattano malattie gravi e che mostrano evidenza clinica preliminare di miglioramento sostanziale rispetto alle terapie esistenti, su endpoint clinicamente rilevanti.
- Include:
- tutti i benefici del Fast Track,
- coinvolgimento diretto del senior management della FDA,
- maggiore probabilità di priority review e di percorsi di approvazione accelerata, se i dati lo giustificano (report Friends of Cancer Research).
Su tempi e velocità: un’analisi supportata dalla stessa FDA mostra che i programmi con BTD hanno in media una riduzione di circa il 30% del tempo di sviluppo in late-stage rispetto ai farmaci senza BTD (studio HHS / ASPE).
Impatti concreti per pemvidutide:
- Tempo – in media, lo sviluppo tra end-of-Phase 2 e approvazione è più rapido per i farmaci con BTD.
- Qualità del dialogo con la FDA – guidance intensiva, non un processo “lasciato andare” in automatico.
- Percezione di rischio – il grande punto interrogativo “la FDA crede davvero in questo asset?” scende di peso.
Non significa che l’approvazione sia garantita, ma significa che il potenziale clinico e regolatorio è stato riconosciuto in modo formale.
3. Timeline MASH – dai 24w alla BTD
3.1 IMPACT Phase 2b – 24 settimane
Nel trial IMPACT di Phase 2b in pazienti con MASH, a 24 settimane pemvidutide ha mostrato (PR Altimmune, paper Lancet):
- risoluzione di MASH senza peggioramento della fibrosi in una quota nettamente superiore rispetto al placebo, con forte significatività statistica.
- Miglioramento marcato dei test non invasivi:
- riduzione del contenuto di grasso epatico (MRI-PDFF),
- calo di ELF, LSM e altri NIT di infiammazione/fibrosi,
- profilo di tollerabilità complessivamente favorevole.
- Per la fibrosi bioptica (≥1 stadio di miglioramento) il segnale era presente ma non ancora statisticamente “pulito” rispetto al placebo a 24 settimane.
È esattamente su questi dati a 24 settimane che la FDA concede ora la BTD, come indicato nel comunicato ufficiale (PR BTD).
3.2 IMPACT – 48 settimane e reazione del mercato
Il 19 dicembre 2025 Altimmune pubblica i dati a 48 settimane (PR 48w):
- ulteriore miglioramento dei NIT (ELF, LSM, cT1, ALT),
- weight loss aggiuntivo, soprattutto alla dose da 1,8 mg,
- safety e tollerabilità che restano globalmente buone.
Il mercato però punisce il titolo con un drawdown nell’ordine del −20%, perché:
- non emergono nuovi dati istologici forti sulla fibrosi di lungo periodo,
- le informazioni sull’end-of-Phase 2 sono limitate in pubblico,
- non c’è una partnership da mostrare per compensare la delusione.
3.3 5 gennaio 2026 – Breakthrough e Phase 3 definito
La news di oggi chiude il cerchio:
- la FDA concede la Breakthrough Therapy Designation per la MASH, basata sui dati a 24 settimane (PR BTD),
- Altimmune comunica di aver ricevuto i minutes ufficiali dell’end-of-phase 2 e di essere allineata su:
- un Phase 3 registrativo di 52 settimane,
- pazienti con fibrosi F2–F3,
- endpoint bioptici supportati dal sistema AIM-MASH AI Assist (richiamato sia nel PR 48w sia nelle sintesi su AIM-MASH come tool AI qualificato: PR 48w, StockTitan).
Il programma MASH di pemvidutide passa da “interessante ma incerto” a programma riconosciuto esplicitamente dalla FDA come meritevole di una corsia preferenziale.
4. Profilo scientifico – oltre il semplice dimagrimento
4.1 Meccanismo d’azione: dual GLP-1 / glucagon 1:1
Pemvidutide è un dual agonist GLP-1 / glucagon con rapporto di attività bilanciato 1:1. Questa impostazione è descritta chiaramente nei documenti societari (corporate update 13 maggio 2025, pagina pipeline):
- GLP-1:
- riduce l’appetito,
- rallenta lo svuotamento gastrico,
- migliora il profilo glicemico.
- Glucagon:
- incrementa l’ossidazione degli acidi grassi,
- agisce direttamente sul metabolismo del grasso epatico,
- può migliorare trigliceridi, LDL e percorsi fibrotici.
L’obiettivo non è solo far perdere peso, ma colpire la malattia epatica alla radice, combinando effetto metabolico sistemico ed effetto diretto sul fegato.
4.2 Dati in obesità – MOMENTUM
Nel trial di obesità MOMENTUM, pemvidutide ha mostrato (PR 48 settimane MOMENTUM, PDF topline):
- perdita di peso media intorno al 15,6% alla dose da 2,4 mg a Week 48,
- buona preservazione della massa magra,
- riduzione di trigliceridi, LDL, grasso epatico e pressione arteriosa.
Questo rende credibile l’idea di un singolo asset che collega obesità e MASH nella stessa storia terapeutica.
4.3 Dati in MASH – cosa abbiamo davvero
In sintesi:
- 24 settimane:
- MASH resolution centrata come endpoint primario,
- NIT fortemente migliorati,
- segnale di fibrosi presente ma non ancora statisticamente “pulito” in biopsia.
- 48 settimane:
- rafforzamento dei segnali su ELF, LSM, cT1 e parametri di infiammazione,
- ulteriore riduzione del grasso epatico,
- weight loss che continua, soprattutto alla dose da 1,8 mg,
- safety sostanzialmente confermata (PR 48w).
- Stato regolatorio:
- Fast Track per MASH (confermato nel corporate update del 2025 e nel PR Fast Track),
- Fast Track per AUD,
- Breakthrough Therapy Designation in MASH (PR BTD).
Il messaggio combinato è chiaro: il pacchetto completo efficacia + safety + NIT è ritenuto dalla FDA abbastanza forte da giustificare un percorso accelerato.
5. Posizionamento competitivo in MASH
Il contesto MASH è estremamente competitivo:
- Rezdiffra (resmetirom, Madrigal):
- primo farmaco approvato per NASH/MASH con fibrosi F2–F3 nel marzo 2024 (PR FDA, PR Madrigal).
- Wegovy (semaglutide, Novo Nordisk):
- GLP-1 puro, con approvazione accelerata per MASH con fibrosi moderata-avanzata ad agosto 2025 (pagina FDA Wegovy-MASH, analisi Biochempeg, nota Nature Biotechnology).
- Altra pipeline in arrivo:
- combo GLP-1 / GIP (tirzepatide, VK2735, ecc.),
- analoghi FGF21 (es. pegozafermin),
- altri meccanismi epatici e metabolici coperti dalle review di settore più recenti.
Dove si inserisce pemvidutide?
- Meccanismo combinato: peso + effetto diretto sul fegato via glucagon.
- Doppio asse MASH + obesità: interessante per pazienti MASH obesi che hanno bisogno sia di beneficio metabolico sia epatico.
- BTD + Fast Track: in un campo così affollato, avere la Breakthrough ti mette nel gruppo ristretto dei programmi prioritari per la FDA.
MASH non è un mercato “winner takes all”. Il bacino di pazienti è enorme e molto eterogeneo. Per un dual GLP-1/glucagon con segnali epatici convincenti e weight loss competitivo, spazio potenziale c’è, e la BTD di oggi è il modo in cui la FDA dice che questo programma merita quella corsa.
6. Struttura finanziaria – cassa, burn, diluizione
6.1 Cassa e bilancio
Dalle ultime comunicazioni societarie:
- Altimmune riporta circa 210,8 milioni USD tra cassa, equivalenti, cassa vincolata e investimenti a breve al 30 settembre 2025 (PR risultati Q3 2025, 10-Q Q3 2025).
- L’azienda si trova in posizione di net cash, con passività totali nettamente inferiori alla somma di cassa e investimenti di breve (vedi 10-Q e, per esempio, la struttura del bilancio nel Q1 2025 qui).
6.2 Cash burn e runway
Un’analisi AI+ su Fintel, basata sui dati della 10-Q Q3 2025, stima che (nota Fintel):
- il burn operativo del Q3 2025 sia nell’ordine di ~11,9M USD, ricavato dai flussi di cassa dei 9 mesi,
- la runway teorica, mantenendo quel burn, sia di circa 4,4 anni (210,8M / 11,9M a trimestre).
Nella pratica, con l’avvio del Phase 3 MASH e i programmi in AUD/ALD e obesità, il burn tenderà a salire, quindi la runway reale sarà più corta della stima lineare. Ma il punto chiave è che si parte comunque da una situazione multi-annuale, non da un’emergenza di 6 mesi.
6.3 Rischio aumento di capitale
Il lato meno piacevole del bull case è la diluizione:
- esiste una shelf registration importante già in essere (documentata nei filing SEC su S-3/ATM),
- con BTD e news positive, il management ha un incentivo evidente a finanziare il Phase 3 da posizione di forza,
- un rally violento come quello di oggi è una finestra naturale per eventuali offerte azionarie.
Il valore qualitativo della news non cambia, ma sul piano del rischio va tenuta in conto la probabilità di ulteriori emissioni azionarie.
7. Ownership – insider, istituzionali, retail
7.1 Struttura azionaria
Dai dati aggregati (Simply Wall St, Fintel, piattaforme tipo Yahoo Finance e Nasdaq) emerge un quadro tipico da small/mid cap biotech:
- Insider: quota di possesso bassa (low single-digit %).
- Istituzionali: presenza significativa ma non dominante (decine di fondi e gestori nei 13F).
- Pubblico retail: maggioranza del float, coerente con volumi e attività social.
È esattamente quello che vedi da Yahoo Finance, Nasdaq e simili.
In pratica, questa struttura significa:
- volatilità elevata,
- reazioni violente a dati e news,
- forte sensibilità al sentiment di breve periodo.
7.2 Attività insider
Le sintesi di transazioni insider (Form 4, riassunte da Fintel, MarketBeat, ecc.) indicano, negli ultimi mesi, più acquisti che vendite da parte del management, seppur su volumi assoluti contenuti. Non è un “insider fortress” con il 20–30% del capitale, ma in una fase post-48w volatile vedere insider comprare sulla debolezza è un segnale direzionalmente positivo.
8. Analisti sell-side – dove sta il consenso
Incrociando diverse fonti pubbliche, il consenso degli analisti è chiaramente positivo:
- rating medio “Buy” / “Strong Buy”,
- price target medi:
- nell’area ~17–18 USD su alcune piattaforme (ad es. Investing.com consensus),
- comunque molto sopra i livelli pre-news, anche dopo il movimento odierno.
- molte note post-48w sottolineavano già che:
- i dati erano coerenti e solidi dal punto di vista scientifico,
- il vero problema era la reazione emotiva del mercato, non la qualità del programma.
La BTD di oggi tende a confermare quella lettura: non è cambiato il dataset, è cambiata la validazione regolatoria.
9. Sentiment retail – Stocktwits, Reddit e crowd
9.1 Stocktwits – ticker “caldo” da mesi
Sui tracker di sentiment di Stocktwits e in particolare sulla pagina ALT/sentiment, ALT è da mesi uno dei nomi più “carichi” del filone MASH/obesità:
- le letture di 24w IMPACT e i dati in obesità hanno portato il sentiment su livelli “extremely bullish”, con volume messaggi molto elevato,
- dopo i 48w il sentiment si è spaccato: parte della community ha venduto su −20%, altri hanno fatto DD approfondite a supporto,
- con la BTD, il feed torna a focalizzarsi su “validation from FDA”, “BTD + Fast Track = percorso AA”, “shorts in trouble”.
9.2 Reddit – DD scientifiche e rischio funding
Su r/Altimmune e thread collegati emergono:
- DD scientifiche sul binomio GLP-1 / glucagon e sui dati IMPACT (spesso linkando direttamente PR e paper),
- modelli di scenario per la commercializzazione MASH con avvio Phase 3 nel 2026, durata 52 settimane e timeline AA vs full approval (thread “Commercialization scenarios”),
- discussioni sul funding e sulla shelf da 400M che citano la cifra di 210,8M di cassa e i dati 24w/48w come punto di inflessione (thread “Funding”).
La parte più lucida della community è, in sostanza, allineata su questa tesi:
“Pemvidutide ha una MASH resolution forte, un weight loss competitivo, segnali di fibrosi in costruzione e un asse MASH + obesità + AUD/ALD. Il problema chiave era l’allineamento con la FDA. Con BTD e Phase 3 definito, l’inflection point è reale.”
10. Rischi principali (senza ridimensionare la news)
In un pezzo a tono bull i rischi restano comunque sul tavolo:
- Esecuzione del Phase 3:
- trial lungo, costoso e complesso (52 settimane, biopsie, AI pathology, popolazione F2–F3),
- eventuali problemi di arruolamento, safety o lettura degli endpoint possono generare drawdown importanti.
- Concorrenza:
- Rezdiffra e Wegovy sono già sul mercato con dataset real-world in espansione,
- pemvidutide dovrà dimostrare un valore aggiunto chiaro (efficacia, tollerabilità, potenziale combinazione, sottogruppi) per ritagliarsi spazio reale.
- Finanziamento e diluizione:
- cassa solida ma non infinita (vedi 10-Q Q3 e analisi Fintel),
- Phase 3 + pipeline multipla costano,
- shelf ampia = rischio diluizione strutturale.
- Volatilità guidata dal retail:
- struttura di proprietà dominata dal retail,
- alta sensibilità a news e sentiment social,
- storico di overshoot in entrambe le direzioni.
Questi rischi c’erano ieri e ci saranno domani. Quello che cambia oggi è che una parte importante dell’incertezza regolatoria è stata ridotta.
11. Sintesi finale – perché la BTD è un vero turning point bull per ALT
Mettendo insieme dati, regolatorio, finanza e sentiment:
- Dati clinici:
- 24 settimane: MASH resolution forte, NIT favorevoli, safety buona,
- 48 settimane: segnali antifibrotici rafforzati e profilo di weight loss interessante.
- Regolatorio:
- Fast Track già in tasca per MASH e AUD,
- ora Breakthrough Therapy in MASH,
- Phase 3 registrativo a 52 settimane definito con endpoint bioptici e AI pathology.
- Finanza:
- azienda net cash (~210,8M USD di cassa + investimenti al Q3 2025),
- runway multi-annuale sul burn attuale,
- spazio per rafforzare il bilancio da posizione di maggiore forza se il sentiment resta costruttivo.
- Ownership & sentiment:
- maggioranza retail con presenza istituzionale significativa,
- ALT è da mesi uno dei nomi di riferimento nel tema MASH/obesità,
- la BTD sposta la percezione da “storia controversa” ad “asset con timbro forte della FDA”.
In pratica:
La FDA ha appena messo un timbro ufficiale su pemvidutide in MASH. Questo alza la qualità della storia, riduce una fetta importante di rischio regolatorio e ridisegna la traiettoria potenziale del titolo.
Il movimento di oggi a doppia cifra non è un pump casuale: è una ri-valutazione logica in uno scenario in cui la probabilità percepita di successo regolatorio è più alta rispetto a ieri.
Altri articoli su Altimmune (ALT) su Merlintrader trading Blog
Per chi vuole ricostruire l’intera storia di pemvidutide e dell’evoluzione del caso ALT, ecco tutti i contenuti pubblicati finora sul sito:
- ALT Altimmune, Inc. – Pemvidutide Late-Stage Clinical Biotech (deep dive principale)
- ALT Altimmune Update Dec 3 – Phase pivotale e driver convergenti
- ALT Altimmune Update Dec 12 – 48-week countdown, cambio CEO e contesto GLP-1
- ALT Altimmune Inc 22 Dec Update – Post-mortem IMPACT 48w (−20% dopo i dati)
- Anti-obesity Drugs And Weight-loss Therapies – panoramica GLP-1 / dual agonist (sezione su pemvidutide)
Scanner for active traders
Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


