DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
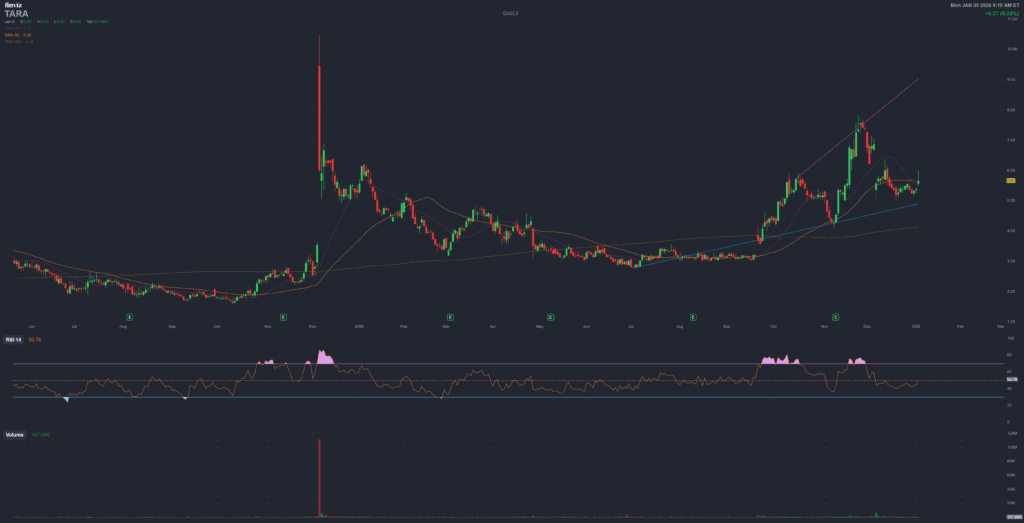
Protara Therapeutics (TARA) – TARA-002 Gets Breakthrough & Fast Track in Pediatric Lymphatic Malformations
Deep dive on TARA-002’s dual FDA designations in pediatric lymphatic malformations, disease context, valuation, ownership and retail sentiment.
Key message: the FDA has granted Breakthrough Therapy and Fast Track designations to TARA-002 for the treatment of pediatric macrocystic and mixed cystic lymphatic malformations (LMs), on top of the existing Rare Pediatric Disease designation and inclusion in the FDA’s CMC Development and Readiness Pilot program.
This turns TARA-002 into a rare triple-designation asset in a high-need pediatric space, and gives Protara a clearly accelerated regulatory lane while the stock is still trading in single digits.
1. Executive summary – a small cap with a very “big cap” style regulatory profile
Protara Therapeutics is now sitting on one of the more interesting small-cap setups in rare pediatric disease:
- TARA-002, a cell-based immunopotentiator derived from the same master cell bank as OK-432 (Picibanil), is being developed for:
- pediatric lymphatic malformations (LMs) – current focus of today’s news,
- BCG-unresponsive and BCG-naïve NMIBC (non–muscle invasive bladder cancer),
- and backed up by a separate IV choline chloride program in IFALD.
- For pediatric LMs, TARA-002 now carries:
- Rare Pediatric Disease (RPD) designation,
- Breakthrough Therapy designation,
- Fast Track designation,
- and selection into the FDA’s CMC Development and Readiness Pilot alongside only a handful of other products.
- The company had roughly $133–134M cash & investments as of 30 Sep 2025 and just raised a further $75M in a December 2025 public offering at $5.75, extending cash runway into mid-2027 by management’s guidance.
- Analyst consensus sits at an average price target around $25 (range $21–30) with **Buy / Strong Buy** ratings from 5–6 covering analysts, implying several hundred percent upside from the current ~$5–6 trading range.
Net-net: a clinical-stage small cap with triple FDA designations in a pediatric ultra-rare indication, a second important program in NMIBC, solid cash runway and a sell-side view that’s aggressively bullish vs current price.
2. What the new designations actually say
On January 5, 2026, Protara announced that the U.S. FDA has granted:
- Breakthrough Therapy Designation for TARA-002 in pediatric patients with macrocystic and mixed cystic LMs,
- Fast Track Designation for the same indication,
- and confirmed that TARA-002 is one of a small number of products selected for participation in the FDA’s Chemistry, Manufacturing, and Controls (CMC) Development and Readiness Pilot.
This is on top of the previously granted Rare Pediatric Disease (RPD) designation for TARA-002 in LMs.
Practically this means:
- BTD → intensive guidance, senior FDA involvement and the possibility of using a smaller dataset for approval if the effect is large and clinically meaningful.
- Fast Track → rolling review, more frequent meetings and flexibility on submission components.
- RPD → potential for a Priority Review Voucher (PRV) if TARA-002 ultimately gets approved in the pediatric indication, which itself can be sold to other companies for substantial sums.
- CMC pilot → the agency works with Protara to streamline and de-risk manufacturing and quality packages ahead of submission, which is especially critical for a biologic/immunopotentiator product like TARA-002.
In one shot, the regulatory risk around “does the FDA buy into this program?” drops significantly; the new questions become timing, execution and competition, not whether the agency is interested.
3. Disease context – pediatric lymphatic malformations (LMs)
Lymphatic malformations are congenital, benign but potentially disfiguring and morbid malformations of the lymphatic system:
- Incidence in the literature is estimated around 1 in 6,000–16,000 live births, generally classified as rare disease.
- Most cases are diagnosed at or shortly after birth, and the vast majority are identified before age 2–3.
- They are classified morphologically into:
- macrocystic (large cysts),
- microcystic (small vesicles, often cutaneous),
- mixed forms (features of both).
- Clinically, these lesions can cause:
- cosmetic deformity (especially in head/neck),
- pain, recurrent infections, bleeding, lymphorrhea, malodor, functional impairment,
- and in some cases life-threatening complications due to compression of airways or vital structures.
There is **no FDA-approved drug therapy** for pediatric lymphatic malformations today; management is a combination of surgery, interventional procedures (sclerotherapy) and repeated interventions, with recurrence and incomplete responses common in the literature.
That background explains why a drug that can be injected into the lesion and deliver sustained, clinically meaningful responses has a strong case for expedited regulatory treatment.
4. TARA-002 – mechanism and clinical signal in LMs
4.1 What TARA-002 is
TARA-002 is an investigational cell-based immunopotentiator developed from the same master cell bank of genetically distinct Streptococcus pyogenes as **OK-432 (Picibanil®)**, a broad immunostimulant used in Japan and Taiwan for various indications, including macrocystic LMs.
Protara has run comparability work to show that TARA-002 is manufacturing-compatible with OK-432, but produced under a modern, scalable process suitable for U.S. and EU regulatory standards.
Mechanism (in company language): when injected into the cyst, TARA-002 activates local innate and adaptive immune cells, triggering a pro-inflammatory response (TNF-α, IFN-γ, IL-6, IL-10, IL-12) that ultimately leads to:
- shrinkage and remodeling of the lymphatic malformation,
- direct killing of target cells,
- and induction of immunogenic cell death that reinforces the response.
4.2 STARBORN-1 Phase 2 – early pediatric LM data
TARA-002 is being evaluated in the open-label STARBORN-1 Phase 2 trial in pediatric patients with macrocystic and mixed cystic LMs. So far Protara has reported:
- completion of the first safety cohort with “promising results” and good tolerability,
- ongoing enrollment with interim data expected (and now partially shared) covering:
- radiologic response (volume reduction),
- clinical response (symptoms, function, appearance),
- safety signals post-injection.
- enough signal for the FDA to grant Rare Pediatric Disease, Breakthrough and Fast Track designations in the LM indication.
While the detailed STARBORN-1 data set is still emerging, the combination of:
- clear clinical benefit in early cohorts,
- alignment with historical OK-432 case series,
- and strong unmet need
is clearly considered sufficient by the FDA to justify high-priority regulatory treatment.
5. Broader pipeline – NMIBC and IV choline chloride
For context on the equity story, TARA-002 is not a single-asset in a single indication:
- TARA-002 in NMIBC:
- Being studied in high-risk BCG-unresponsive and BCG-naïve NMIBC in the ADVANCED-2 Phase 2 trial.
- Recent interim updates (Dec 2025) showed “robust responses” in BCG-naïve patients, fueling part of the rally that preceded the December equity raise.
- IV choline chloride in IFALD:
- Program THRIVE-3, a seamless Phase 2b/3 trial, targets **intestinal failure–associated liver disease** in patients dependent on parenteral nutrition.
- IV choline chloride has its own Fast Track designation and could become an important, differentiated asset if data are positive.
So the story is not “one narrow pediatric niche only”; TARA-002 plus IV choline give Protara a multi-asset, multi-indication rare disease and oncology profile, with LMs and NMIBC as the current spearheads.
6. Financial profile – cash, burn, and recent financing
6.1 Cash and runway
According to the Q3 2025 financial update, as of 30 September 2025 Protara had:
- $133.6M in unrestricted cash, cash equivalents and marketable debt securities,
- with management guiding that this cash was expected to fund operations into mid-2027.
Q3 2025 numbers:
- R&D expenses: $9.6M for the quarter,
- G&A expenses: $5.2M,
- Net loss: $13.3M for the quarter (versus $11.2M in Q3 2024).
6.2 December 2025 $75M public offering
On 4 December 2025, Protara priced a $75M underwritten public offering at $5.75 per share, for 13,043,479 shares plus a 30-day greenshoe option for 1.96M extra shares.
The offering closed on 8 December 2025; all shares were primary, and proceeds are earmarked primarily to:
- fund clinical development of TARA-002 (LMs and NMIBC),
- support IV choline chloride and other programs,
- general corporate and working-capital needs.
Net effect: despite clear dilution, the company emerges with **>200M USD total liquidity** and a runway that, barring major spend escalation, is **comfortably multi-year**.
7. Ownership structure – insiders vs institutions vs retail
Ownership snapshots from several sources paint a consistent picture:
- According to Simply Wall St, the breakdown is roughly:
- Individual insiders: ~1.8–2.8% of shares,
- General public (retail): ~48%,
- Institutions: ~50%.
- Fintel and other institutional-holders trackers show around 140–150 institutional owners holding roughly 27–28M shares, including Janus Henderson, Velan, BlackRock, Vanguard and others in the top-holder list.
- Some dashboards (e.g. StockTitan) list institutional ownership in the high-70% range and insiders around 2–3%, reflecting differences in float vs total shares calculations but still consistent with “institutionally anchored, retail-amplified” structure.
In practice:
- Institutions are clearly engaged and own a substantial chunk of the stock.
- Retail still matters – especially around catalysts and financings – but the register is not purely retail-driven.
- Recent filings show some institutions (e.g. Velan Capital) increasing stakes ahead of recent data/BTD, which fits the bull side of the story.
8. Analyst coverage – “Strong Buy” with high targets
Across sell-side aggregators, the message is very directionally aligned:
- Number of covering analysts: 5–6, depending on the source (MarketScreener, Investing.com, TipRanks, MarketBeat).
- Consensus rating: “Buy” to “Strong Buy”.
- Average 12-month price target:
- around $25 on Investing.com and MarketScreener (range $21–30),
- around $19.5 in some other aggregators depending on snapshot and included analysts.
- Implied upside: typically **+250–350%** vs current ~$5–6 spot in the consensus snapshots.
The common thesis across notes is:
- TARA-002 in LMs + NMIBC and IV choline in IFALD represent a **multi-asset upside** opportunity.
- The dual BTD/Fast Track + RPD designations materially de-risk the LM program.
- Recent financings remove the near-term cash overhang, even if they are dilutive.
9. Retail sentiment – Stocktwits, Reddit, and the financing overhang
9.1 Stocktwits picture
On Stocktwits, TARA is not among the hyper-traded meme names, but it shows the usual biotech pattern:
- Spikes in message volume and watchers around:
- positive NMIBC updates,
- November 2025 interim LM data,
- December 2025 $75M offering (many threads complaining about dilution and timing),
- today’s BTD/Fast Track press release.
- Sentiment readouts on third-party scrapers (where visible) generally show:
- bullish bias over multi-month periods,
- short-term dips into neutral/bearish immediately after the December offering.
9.2 Reddit
On Reddit, TARA compare threads (especially in r/biotech_stocks) tendono a concentrarsi su:
- il mix “grande potenziale vs diluizioni ripetute”,
- valutazioni pre e post-offering, con commenti che notano come il prezzo di 5,75$ fosse sotto i massimi recenti ma comunque dopo un rally >100%,
- il fatto che la cassa ora copra fino a metà 2027, ma al costo di un bel po’ di carta nuova in giro.
Detto in sintesi retail: c’è una base di **true believers** sulla combo LMs + NMIBC che usa i drop da offering come entry/add, e una fascia speculativa che gioca solo i movimenti su news.
10. Main risks – cosa può andare storto anche con BTD/Fast Track
BTD e Fast Track non annullano i rischi; li ridisegnano.
- Rischio esecuzione clinica:
- STARBORN-1 è ancora una Phase 2, aperta e relativamente piccola.
- Servono dati più ampi, follow-up e un programma ben strutturato per il registrational trial.
- FDA può essere flessibile, ma numeri e safety devono reggere nel tempo.
- Rischio CMC / manufacturing:
- TARA-002 è un prodotto complesso tipo biologico; da qui l’ingresso nel CMC pilot.
- Questo riduce il rischio regolatorio CMC ma non lo azzera: scaling e consistenza restano critici.
- Rischio concorrenza e adozione:
- Trattamenti attuali (scleroterapia, chirurgia) hanno comunque una lunga storia, con risultati discreti in una parte dei pazienti.
- Bisognerà dimostrare che TARA-002 offre un miglioramento chiaro su:
- numero di procedure,
- necessità di anestesia,
- esiti estetici/funzionali,
- e qualità di vita.
- Rischio diluizione futura:
- Nonostante la cassa post-offering sia forte, l’azienda è ancora in piena fase di sviluppo e potrebbe usare ulteriore equity più avanti, soprattutto se ampliando gli studi.
- Rischio esecuzione commerciale:
- Lanciare un prodotto in malattia rara pediatrica richiede:
- centri di riferimento ben serviti,
- logistica complessa,
- pricing sensibile (pazienti pediatrici, payor attenti).
- Lanciare un prodotto in malattia rara pediatrica richiede:
11. Final take – come si presenta oggi il “bull case” su TARA
In versione sintetica:
- Asset: TARA-002, immunopotentiator con storia reale (OK-432) e segnale clinico in LMs e NMIBC.
- Regolatorio: tripla combinazione Rare Pediatric Disease + Breakthrough Therapy + Fast Track in pediatric LMs, più CMC pilot – pacchetto rarissimo per una small cap.
- Pipeline: oltre alle LMs, NMIBC con dati interim robusti e IV choline in IFALD – non è un “one-trick pony”.
- Finanza: circa 133–134M di cassa/investimenti al Q3 2025 + 75M raccolti a dicembre → runway guidata fino a metà 2027.
- Mercato: LMs pediatriche = rare ma con huge unmet need e nessun farmaco approvato; NMIBC = indicazione ampia e molto “valutata” dal mercato.
- Equity story: registri con istituzionali importanti a bordo, forte base retail biotech, analisti su target 20–30$ con rating Buy/Strong Buy.
La notizia di oggi non è una chicca cosmetica: è un timbro forte della FDA su un programma pediatrico raro con meccanismo e dati coerenti. Per un titolo che gira ancora in area 5–6$, in uno scenario di cassa lunga e di endorsement multipli (RPD, BTD, Fast Track, CMC pilot), il setup resta dichiaratamente da bull case – fermo restando il rischio biotech intrinseco, alto per definizione.
Key official sources and further reading
A selection of primary sources used for this analysis (FDA, SEC, company IR and major data aggregators):
- Protara – BTD & Fast Track press release (Jan 5, 2026)
- Q3 2025 financial results & business update
- $75M public offering pricing press release (Dec 4, 2025)
- Company LM pipeline page – STARBORN-1 trial
- Scientific overview – lymphatic malformations epidemiology & treatment (example)
- MarketScreener – analyst consensus & targets for TARA
- Simply Wall St – ownership breakdown
- Fintel – institutional holders and short interest
Protara Therapeutics (TARA) – TARA-002 ottiene Breakthrough & Fast Track nelle Lymphatic Malformations pediatriche
Deep dive su TARA-002: tripla designazione FDA in LMs pediatriche, contesto clinico, numeri finanziari, ownership, analisti e sentiment retail.
Messaggio chiave: la FDA ha concesso a TARA-002 la Breakthrough Therapy Designation e la Fast Track Designation per il trattamento delle lymphatic malformations (LMs) macrocistiche e miste in pazienti pediatrici, oltre alla già esistente Rare Pediatric Disease Designation e alla partecipazione al programma pilota FDA sui CMC.
In pratica, TARA-002 diventa un asset con un profilo regolatorio “da big cap” all’interno di una small cap, in un setting pediatrico raro con forte unmet need e nessun farmaco approvato.
1. Executive summary – small cap, ma con timbro regolatorio pesante
Protara Therapeutics oggi è una delle small cap più interessanti in area rare disease/oncologia:
- TARA-002, immunopotentiator derivato dalla stessa master cell bank di OK-432 (Picibanil), viene sviluppato per:
- lymphatic malformations pediatriche (focus della news),
- NMIBC (non–muscle invasive bladder cancer) in setting BCG-naïve e BCG-unresponsive,
- mentre un altro asset (IV choline chloride) copre IFALD.
- Per le LMs pediatriche oggi TARA-002 ha:
- Rare Pediatric Disease designation,
- Breakthrough Therapy designation,
- Fast Track designation,
- selezione nel CMC Development and Readiness Pilot della FDA.
- A livello cassa:
- circa 133–134M USD di cash + investimenti al 30/09/2025,
- offerta pubblica da 75M USD a 5,75$ a dicembre 2025,
- guidance di runway fino a metà 2027.
- Analisti:
- consensus Buy / Strong Buy,
- target price medio intorno ai 25$ (range 21–30$), con upside teorico di varie centinaia di punti percentuali rispetto agli attuali ~5–6$.
Tradotto: small cap in perdita, sì, ma con tripletta regolatoria in un pediatrico raro, seconda gamba importante in NMIBC, cassa lunga e sell-side decisamente più ottimista del prezzo corrente.
2. Cosa dicono davvero le nuove designazioni
Il comunicato del 5 gennaio 2026 conferma che la FDA ha concesso a TARA-002 in LMs pediatriche:
- Breakthrough Therapy Designation,
- Fast Track Designation,
- conferma della pre-esistente Rare Pediatric Disease Designation,
- e partecipazione al CMC Development and Readiness Pilot (programma pilota per ottimizzare e “anticipare” la parte CMC).
In pratica:
- BTD → interazione ravvicinata con FDA, possibilità di percorsi di approvazione accelerata su dataset più “compatti” se l’effetto clinico è molto marcato.
- Fast Track → rolling review, più flessibilità su submission e interazioni frequenti.
- RPD → possibilità di ottenere un Priority Review Voucher pediatrico in caso di approvazione, che può essere venduto a terzi per cifre molto significative.
- CMC pilot → la FDA aiuta a “pulire” in anticipo tutta la parte chimico-farmaceutica, particolarmente delicata per un prodotto di tipo biologico/cell-based.
La domanda “la FDA ci crede?” passa in secondo piano; il focus si sposta su execution clinico/regolatoria, tempi e concorrenza.
3. Contesto clinico – lymphatic malformations pediatriche
Le LMs sono malformazioni congenite lente del sistema linfatico:
- incidenza nella letteratura: circa 1 su 6.000–16.000 nati vivi, quindi rare disease;
- la grande maggioranza dei casi viene diagnosticata alla nascita o nei primi 2–3 anni di vita;
- classificazione morfologica:
- macrocistiche,
- microcistiche,
- miste.
- le sedi più frequenti sono testa/collo, ma possono coinvolgere praticamente qualsiasi distretto (torace, addome, arti, ecc.);
- possono causare:
- deformità estetica importante,
- dolore, infezioni ricorrenti, sanguinamento, linforrea, cattivo odore,
- complicanze anche gravi per compressione di vie aeree o strutture vitali.
Ad oggi non esiste nessun farmaco approvato dalla FDA specifico per le LMs pediatriche: lo standard è scleroterapia, chirurgia, e gestione caso per caso, con risultati buoni in una parte dei pazienti ma recidive frequenti e un carico di procedure tutt’altro che banale.
In questo contesto, un prodotto iniettato direttamente nella lesione che possa ridurre dimensioni e sintomi in modo sostenuto è candidabile in modo naturale a percorsi accelerati.
4. TARA-002 – meccanismo e segnale clinico nelle LMs
4.1 Cos’è TARA-002
TARA-002 è un immunopotentiator cell-based sviluppato a partire dalla stessa master cell bank di OK-432 (Picibanil®), immunoterapico utilizzato in Giappone/Taiwan anche nelle LMs macrocistiche.
Protara ha lavorato sulla comparabilità per dimostrare che TARA-002 è sostanzialmente simile ad OK-432, ma prodotto con un processo moderno e scalabile, compatibile con gli standard regolatori USA/EU.
Il meccanismo ipotizzato: una volta iniettato nel cisto, TARA-002 attiva cellule immuni innate e adattative localmente, induce una risposta pro-infiammatoria (TNF-α, IFN-γ, IL-6, IL-10, IL-12), con:
- remodeling e riduzione del volume della malformazione,
- morte cellulare immunogena e risposta immune secondaria,
- parallelismo con quanto già visto in decenni di uso “off-US” di OK-432.
4.2 STARBORN-1 – dati iniziali in pediatria
STARBORN-1 è uno studio di Phase 2 open-label in pazienti pediatrici con LMs macrocistiche e miste. Ad oggi Protara ha comunicato che:
- la prima coorte di sicurezza è stata completata con risultati promettenti e buona tollerabilità,
- è in corso l’arruolamento, con obiettivo di:
- valutare riduzioni volumetriche radiologiche,
- miglioramenti clinici (sintomi, funzione, estetica),
- profilo di safety post-iniezione.
- il segnale complessivo è stato giudicato sufficiente dalla FDA per concedere RPD + BTD + Fast Track nel contesto pediatrico.
È chiaro che serviranno dati più completi, ma la combinazione di: risposta osservata, storia di OK-432 e unmet need forte è bastata per far scattare la corsia preferenziale regolatoria.
5. Pipeline più ampia – NMIBC e IV choline chloride
Per capire la equity story, TARA-002 non è solo LMs:
- TARA-002 in NMIBC:
- ADVANCED-2 è uno studio di Phase 2 in pazienti ad alto rischio BCG-naïve e BCG-unresponsive.
- Gli aggiornamenti di dicembre 2025 parlano di risposte robuste in BCG-naïve, con attenzione particolare a complete response e durata.
- IV choline chloride in IFALD:
- THRIVE-3 è un trial seamless Phase 2b/3 in pazienti dipendenti da nutrizione parenterale.
- Anche IV choline chloride ha Fast Track e, se positivo, può diventare un asset unico in un setting rarissimo ma ad altissimo valore per paziente.
Quindi il caso Protara è multi-asset: LMs + NMIBC + IFALD, tutte aree in cui non mancano né bisogno né spazio di pricing.
6. Profilo finanziario – cassa, burn e ultima raccolta
6.1 Cassa e runway
Dal comunicato Q3 2025:
- cassa, equivalenti e investimenti in titoli di debito a breve: circa 133,6M USD al 30/09/2025,
- management stima che questa dotazione sia sufficiente a finanziare le operazioni fino a metà 2027.
Per il Q3 2025:
- R&D: 9,6M USD,
- G&A: 5,2M USD,
- perdita netta: 13,3M USD (vs 11,2M nel Q3 2024).
6.2 Offerta pubblica da 75M USD (dicembre 2025)
Il 4 dicembre 2025 Protara ha prezzato un’offerta pubblica da 75M USD a 5,75$ per azione, per 13.043.479 azioni più opzione greenshoe.
L’operazione è stata chiusa l’8 dicembre 2025; tutte azioni primarie, proventi destinati a:
- sviluppo clinico di TARA-002 (LMs + NMIBC),
- supporto agli altri programmi (IV choline, ecc.),
- capitale circolante e spese generali.
A livello equity è chiaramente diluitiva, ma combinata con i 133,6M esistenti porta la dotazione di cassa a livelli più che adeguati per portare avanti pipeline e registrational plan nel medio termine.
7. Ownership – insider, istituzionali, pubblico
I dati di ownership mostrano uno schema abbastanza equilibrato:
- Insider: nell’ordine del 2–3% delle azioni.
- Istituzionali: tra il 40% e il 70–80% a seconda della metrica (float vs total); Fintel cita oltre 140 investitori istituzionali con circa 27–28M di azioni.
- Pubblico retail: il resto del float, attorno al 40–50% nelle stime tipo Simply Wall St.
Tra i top holder risultano nomi come Janus Henderson, Velan Capital, BlackRock, Vanguard, ecc., quindi presenza istituzionale “vera”, non solo fondi piccoli o ETF marginali.
Il quadro finale è: titolo istituzionalmente ancorato ma con una componente retail attiva, che amplifica i movimenti sulle news (soprattutto su offerte e catalyst clinici).
8. Analisti – rating e target price
Tra i vari aggregatori (MarketScreener, Investing.com, TipRanks, MarketBeat):
- copertura da parte di 5–6 analisti,
- consensus tra Buy e Strong Buy,
- target price medio intorno ai 25$ (range 21–30$); in alcune snapshot appare un medio di ~19,5$ a seconda di quale sottoinsieme di analisti è incluso.
L’upside implicito rispetto ai ~5–6$ attuali resta comunque nell’ordine di +250–350%, con visione chiaramente positiva su LMs + NMIBC + IFALD e sul profilo cassa post-offerta.
9. Sentiment retail – Stocktwits, Reddit e overhang da funding
9.1 Stocktwits
Su Stocktwits TARA non è un meme, ma mostra pattern da classica biotech:
- picchi di messaggi e watchers:
- su dati NMIBC,
- sui primi update LMs,
- durante l’annuncio dell’offerta da 75M (con commenti negativi su diluizione e timing),
- e ora sulla news BTD + Fast Track.
- il bias di fondo è bullish nel medio periodo, con fasi di neutral/bearish immediatamente dopo i funding.
9.2 Reddit
Su Reddit (soprattutto r/biotech_stocks) i thread su TARA ruotano attorno a:
- mix tra forte potenziale e necessità di capitali ripetuti,
- discussioni sul fatto che il pricing dell’offerta a 5,75$ fosse sotto i massimi ma dopo un rally >100%,
- il conforto dato da cassa estesa a metà 2027, ma al prezzo di diluizione non triviale.
La base retail più “seria” tende a vedere TARA come bet a 2–3 anni sulla combinazione LMs + NMIBC + IFALD, non come trade intraday.
10. Rischi principali – oltre il timbro FDA
I rischi restano alti, in stile biotech:
- Esecuzione clinica: STARBORN-1 è ancora una Phase 2 open-label; servirà un disegno registrativo ben costruito e dati solidi su un campione più ampio.
- CMC/manifattura: il prodotto è complesso; il CMC pilot aiuta, ma la scalabilità e la consistenza restano punti sensibili.
- Concorrenza/adozione: chirurgia e scleroterapia hanno comunque una storia; il posizionamento dovrà essere chiaro (meno interventi? outcome migliori? minore morbidità?).
- Diluizione futura: anche con cassa lunga, nuove fasi di sviluppo o espansione di programmi possono richiedere ulteriore equity più avanti.
- Rischio esecuzione commerciale: lanciare un farmaco in malattia rara pediatrica non è banale (centri specializzati, logistica, pricing, payor).
11. Sintesi finale – com’è il bull case oggi su TARA
Riassumendo:
- Asset: TARA-002 con storia reale (OK-432), segnale in LMs e NMIBC, più IV choline in IFALD.
- Regolatorio: Rare Pediatric Disease + Breakthrough + Fast Track in LMs, più CMC pilot → pacchetto raro per una small cap.
- Finanza: ~133,6M di cassa/investimenti al Q3 2025 + 75M da offerta → runway fino a metà 2027.
- Mercato: LMs pediatriche = rare ma ad altissimo unmet need; NMIBC = enorme; IFALD = ultra-raro ma di valore.
- Equity: istituzionali importanti, retail attivo, analisti con target molto sopra il prezzo attuale.
La BTD/Fast Track di oggi è un vero turning point regolatorio, non un orpello: riduce il rischio “la FDA è tiepida” e sposta tutto su execution. Per chi guarda a 2–3 anni, l’accoppiata profilo regolatorio + cassa + pipeline mette TARA su una lista corta di small cap da seguire da vicino.
Fonti ufficiali e letture consigliate
Una selezione di link diretti alle fonti usate per questo report:
- PR Protara – BTD & Fast Track su TARA-002 in LMs pediatriche
- Protara – risultati finanziari Q3 2025 e business update
- PR – offerta pubblica da 75M USD (dicembre 2025)
- Pagina pipeline Protara – LMs & trial STARBORN-1
- MarketScreener – consensus analisti su TARA
- Simply Wall St – struttura proprietaria
- Fintel – holders istituzionali e short interest
- Stocktwits – stream TARA (sentiment e messaggi)
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


