DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
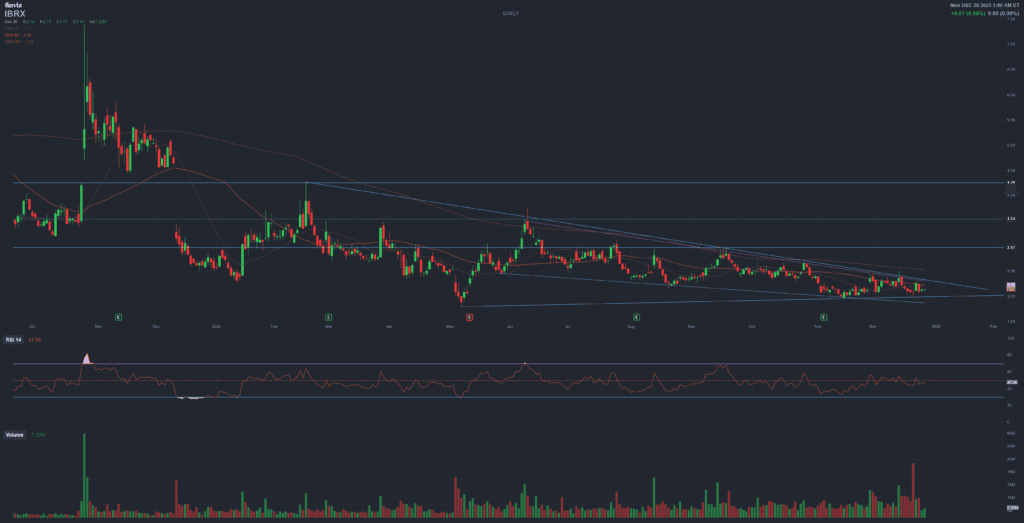
Ticker: IBRX (NASDAQ)
ImmunityBio (IBRX) – ANKTIVA, NMIBC and the long road from approval to a real business
Commercial-stage IL-15 / NK-cell immunotherapy story with a real product on the market, fast-growing revenue, a still-tight cash position and a very opinionated retail base.
News of the Day – Why IBRX is back on screens
Latest updatesThe IBRX story today is all about how far ANKTIVA can go in NMIBC – and whether the current balance sheet can carry the rest of the pipeline long enough.
1) EMA backs ANKTIVA in Europe (December 2025)
On December 12, 2025, the European Medicines Agency recommended granting a conditional marketing authorization for ANKTIVA (nogapendekin alfa inbakicept) in combination with BCG for adults with BCG-unresponsive non-muscle invasive bladder cancer (NMIBC) with CIS, with or without papillary tumors – effectively mirroring the U.S. label in the EU and leveraging the pivotal QUILT-3.032 data set.
2) Strengthening long-term data in papillary NMIBC
Just a few days later, ImmunityBio reported three-year outcomes from high-grade papillary-only NMIBC treated with ANKTIVA + BCG, highlighting 96% bladder cancer-specific survival at three years, durable disease-free survival and high cystectomy-free rates – important for the real-world positioning of ANKTIVA vs historical BCG alone or radical cystectomy.
3) Commercial ramp: revenue now meaningful, but not yet self-funding
Since U.S. FDA approval (April 22, 2024) for BCG-unresponsive NMIBC CIS with or without papillary tumors, ANKTIVA revenue has ramped quickly: ImmunityBio reported Q3 2025 revenue of about $32M and YTD ANKTIVA sales of roughly $75M, with unit volume up over 400% year-on-year. At the same time, operating cash burn remains heavy (over $230M YTD in operating outflows), so the ramp is real but not yet enough to make IBRX self-funded.
4) Stock still behaving like a high-beta biotech
Around late December 2025, IBRX trades roughly in the $2.10–2.20 range, with a 52-week range of about $1.83–4.27 and a market cap close to $2.1B. The stock remains volatile, very sensitive to regulatory headlines, cash runway discussions, and momentum flows from retail traders.
Quick data – IBRX at a glance
Snapshot (late Dec 2025)Ticker / ExchangeIBRX – Nasdaq
Share price≈ $2.14 (Dec 26, 2025)
52-week range$1.83 – $4.27
Market cap≈ $2.1B
SectorOncology / Immunotherapy
StageCommercial-stage biotech
Lead productANKTIVA (N-803, IL-15 superagonist)
Approved indicationBCG-unresponsive NMIBC CIS ± papillary (US)
EU statusEMA conditional MA recommended (Dec 2025)
Q3 2025 revenue~$32M (+400%+ YoY)
YTD ANKTIVA sales 2025~$75M
Cash + securities~$258M (Sep 30, 2025)
Operating cash burn YTD≈ $230M+
Analyst consensus“Strong Buy” (3rd-party analysts)
12-month PT (avg)~$9.7–10.4 (range $5–24)
Data compiled from ImmunityBio filings/PR, Nasdaq/Yahoo Finance, MarketBeat, StockAnalysis and Investing.com. Values rounded and for information only, not for trading decisions.
IL-15 superagonist + NK-cell platform
Bladder cancer (NMIBC)
High volatility
Cash-intensive pipeline
Executive Summary – What ImmunityBio is (and is not)
Context for non-specialistsImmunityBio is no longer a “pure story stock”: it now has an FDA-approved product on the market – ANKTIVA, an IL-15 receptor agonist used with BCG for BCG-unresponsive non-muscle invasive bladder cancer (NMIBC) with CIS. Revenue is growing fast from a low base, but the rest of the story still looks and trades like high-risk immuno-oncology.
- Clinical foundation: ANKTIVA showed a ~71% complete response in CIS patients and long median duration of response (>24 months) in the pivotal NMIBC trial, with robust bladder-preserving outcomes – now backed by extended three-year data and regulatory recognition across the US, UK and now the EU (conditional recommendation).
- Platform angle: ANKTIVA is the front face of a much broader platform: IL-15 superagonist combinations, engineered NK-92 / t-haNK cell therapies and adenovirus-based vaccines across multiple solid tumors and infectious diseases.
- Commercial reality: Q3 2025 shows ~$32M revenue with ANKTIVA unit volume +400%+ YoY, but the company still runs operating losses above $60M per quarter and yearly operating cash outflows above $200M. The current cash + marketable securities (~$258M) buy time, not comfort.
- Regulatory upside vs execution risk: key 2025–26 levers include EU formal approval and launch, papillary disease sBLA progress, broader adoption in real-world NMIBC, and maturation of lymphopenia / solid tumor programs. Each adds optionality, but also manufacturing, pricing and payer-access execution risk.
- Market expectations: 3rd-party analyst targets cluster around ~$9–10 per share on a 12-month view (with wide dispersion from $5 to $24), and many models embed multi-billion peak sales scenarios that are far from de-risked.
- Retail sentiment: Reddit, Stocktwits and X show a classic split: a vocal long-term bull camp versus skeptical traders focusing on dilution risk, management communication and media strategy. These are non-professional opinions and often emotionally driven.
The goal here is to lay out facts, scenarios and known risks so that readers can form their own view. It is explicitly not a recommendation to buy, sell or hold ImmunityBio or any other security.
1. Company & Platform – What is ImmunityBio actually building?
IL-15 + NK-cell + vaccine stackImmunityBio positions itself as a platform immunotherapy company built around three pillars: an IL-15 superagonist (ANKTIVA), engineered NK-92 / t-haNK cell therapies, and a next-generation adenovirus vaccine platform.
1.1 ANKTIVA (N-803) – IL-15 superagonist as the lead asset
ANKTIVA (nogapendekin alfa inbakicept-pmln, previously N-803) is an IL-15 superagonist complex that expands and activates NK and CD8+ T cells, enhancing anti-tumor immunity. The drug is delivered intravesically with BCG in NMIBC and is being tested systemically and intralesionally in several solid tumor settings.
1.2 NK-92 / t-haNK cell therapy platform
The NK-92 platform is a family of engineered NK cell lines (including high-affinity haNK and CAR-engineered t-haNK cells) targeting PD-L1, CD19 and other antigens. These cells are evaluated in multiple early- and mid-stage trials across difficult solid tumors such as pancreatic cancer, TNBC, GBM and head & neck cancers.
1.3 Adenovirus (hAd5) vaccines and NANT Cancer Vaccine concepts
ImmunityBio also owns an adenovirus-based vaccine platform (hAd5) used both in oncology and infectious disease, including COVID-19 vaccine candidates and tumor neoantigen vaccines. The concept is to orchestrate innate and adaptive immunity using coordinated combinations of:
- Checkpoint blockade
- IL-15 superagonist (ANKTIVA)
- NK-based cell therapies (haNK / t-haNK)
- Adenovirus-based vaccination
On paper, this is a powerful integrated platform. In practice, investors are watching one question first: can ANKTIVA in NMIBC become a durable, cash-generating franchise that pays for everything else?
2. ANKTIVA in NMIBC – From CRL to approval to EU entry
Pivotal asset, pivotal execution2.1 Regulatory journey
- 2023 – Complete Response Letter (CRL): the initial BLA for N-803 + BCG in BCG-unresponsive NMIBC CIS received a CRL in May 2023, driven primarily by manufacturing/inspection issues rather than clinical efficacy concerns.
- 2024 – FDA approval: after resubmission, the FDA approved ANKTIVA + BCG on April 22, 2024 for adult patients with BCG-unresponsive NMIBC CIS with or without papillary tumors.
- UK approval: in 2025, the UK MHRA also approved ANKTIVA + BCG for BCG-unresponsive NMIBC CIS, reinforcing the global credibility of the data.
- 2025 – EMA conditional recommendation: in December 2025, the EMA’s CHMP recommended conditional marketing authorization in the EU for ANKTIVA + BCG in BCG-unresponsive NMIBC CIS with or without papillary tumors.
2.2 Clinical efficacy: what the data say
The FDA Drug Trials Snapshot and QUILT-3.032 publication show that ANKTIVA + BCG achieved about 71% complete response (CR) in CIS patients with BCG-unresponsive high-risk NMIBC, with a median duration of response around 24.1 months. Long-term follow-up suggests durable bladder preservation and disease-specific survival benefits in both CIS and papillary-only cohorts, with the recent 96% three-year survival figure in high-grade papillary-only patients being particularly eye-catching.
2.3 Competitive landscape
In BCG-unresponsive NMIBC, ANKTIVA competes directly or indirectly with:
- Keytruda (pembrolizumab) – PD-1 inhibitor, systemic IV therapy with its own efficacy/safety profile.
- Intravesical chemo and other devices – e.g. mitomycin, gemcitabine–docetaxel regimens, device-assisted BCG, etc.
- Radical cystectomy – still the definitive option, but highly morbid and often poorly accepted by patients.
ANKTIVA’s main differentiation story is: local immunotherapy that amplifies BCG, with durable responses and meaningful cystectomy avoidance. Whether payers and urologists embrace that positioning at scale is one of the core commercial questions for the next 2–3 years.
3. Commercial ramp & financials – Revenue vs cash burn
Growing, but not yet comfortable3.1 Revenue trajectory
Since launch, ANKTIVA has shown a strong ramp in both volume and revenue:
- Q1 2025: net product revenue ~$16.5M, already up sharply vs late 2024.
- Q2 2025: revenue ~$26.4M (+60% vs Q1), with YTD sales ~$43M and unit volume +246% vs 2H 2024.
- Q3 2025: revenue around $32M, +400%+ YoY, continuing the growth trend and reflecting broader adoption.
3.2 Cash, burn and financing structure
As of September 30, 2025, ImmunityBio reported ~$257.8M in cash, cash equivalents and marketable securities, up from around $154M at the end of Q2 2025, partly thanks to external financing and revenue growth. However, operating cash outflows for 2025 remain above $200M, and the company continues to rely on structured financings and revenue interest obligations.
A key point stressed by more conservative investors is that the business is still in “scale-up mode” with significant execution risk: manufacturing scale-up, sales force build-out, real-world outcomes, payer access and potential label expansions all require capital before they pay off.
3.3 What this means for investors (in neutral terms)
- ANKTIVA revenue is becoming large enough to matter, not yet large enough to fund the full platform.
- Cash runway is improved but still finite; dilution or additional deals cannot be ruled out if the ramp slows or pipeline spend stays high.
- Any slowdown in ANKTIVA uptake, pricing pressure or payer friction would quickly feed back into the equity narrative.
These are not buy/sell signals – just the mechanical consequences of the current capital structure.
4. Pipeline & Catalysts – Beyond NMIBC
Optionality vs focus4.1 NMIBC label expansion (papillary disease)
In April 2025, ImmunityBio submitted an sBLA to the FDA to extend ANKTIVA + BCG to BCG-unresponsive NMIBC papillary disease beyond CIS alone. The process has been complicated: the company disclosed a Refusal-to-File (RTF) in May 2025 and requested an urgent Type A meeting to reconcile what it describes as contradictory regulatory guidance.
If resolved positively, this could:
- expand the eligible U.S. population;
- strengthen the economic base of ANKTIVA in bladder cancer;
- support a broader global label in the medium term.
4.2 Lymphopenia & Cancer BioShield platform
ANKTIVA also received FDA Expanded Access authorization in 2025 for treatment of lymphopenia in solid tumors, positioning it as a potential “immune restoration” therapy under the Cancer BioShield concept. This is early-stage commercially, but scientifically interesting: patients with chemotherapy-induced lymphopenia often lack good targeted options to rebuild immune surveillance.
Beyond the US program, in May 2025 ImmunityBio signed a strategic Memorandum of Understanding in Saudi Arabia to bring the Cancer BioShield™ platform to the Middle East. The agreement, announced during the Saudi–U.S. Investment Forum 2025 in Riyadh, involves the Saudi Ministry of Investment (MISA), King Faisal Specialist Hospital & Research Centre (KFSHRC) and King Abdullah International Medical Research Center (KAIMRC).
- Objectives: introduce immune-restorative therapies and localize biomanufacturing in line with the Saudi National Biotech Strategy.
- Planned activities: local clinical trials, technology and know-how transfer, training of healthcare staff and the potential creation of regional subsidiaries in the Middle East.
Strategically, this partnership positions ImmunityBio as an early immunotherapy player in the Middle Eastern market and may, over time, provide additional capital flows and infrastructure support that help partially offset the heavy cash burn described earlier in the report.
4.3 Solid tumor combinations (pancreatic, lung, TNBC, GBM)
Multiple trials evaluate ANKTIVA with checkpoint inhibitors, chemotherapy and NK-based therapies in:
- pancreatic cancer, TNBC and head & neck cancer, often as part of “NANT Cancer Vaccine” strategies;
- NSCLC and other solid tumors, using ANKTIVA to rescue lymphopenia and synergize with PD-L1 t-haNK cells;
- hematologic cancers (e.g. NHL) with CD19 t-haNK cell therapy.
For equity holders, these programs represent high-upside optionality but are still far from commercialization. Their role today is more about narrative and long-term optionality than near-term cash flow.
4.4 Upcoming catalysts & future milestones
There are no new “PDUFA-style” fixed dates on the calendar, but several forward-looking events can shape the IBRX story over the next 12–36 months:
- European Commission decision and EU launch: following the December 2025 CHMP positive opinion, the formal decision by the European Commission on ANKTIVA’s conditional marketing authorization is expected in early 2026. The speed and depth of the first EU launches will be closely watched.
- Regulatory clarity on papillary-only NMIBC: after the May 2025 RTF for the papillary sBLA, the outcome of the Type A meeting and any subsequent regulatory plan (new data package, potential randomized trial, resubmission) will be a key medium-term catalyst for the NMIBC franchise.
- ResQ201A Phase 3 in NSCLC: the registrational RESQ201A study in checkpoint-resistant NSCLC is now underway. Management has stated in multiple 2025 updates that it aims to file a BLA in 2025 for second- and third-line NSCLC after progression on checkpoint inhibitors, although the actual timing will ultimately depend on enrollment, data maturity and FDA feedback.
- Lymphopenia / Cancer BioShield program: expansion of the Expanded Access protocol into a more formal pivotal pathway, plus early real-world data in chemotherapy/radiation/checkpoint-treated patients, can gradually turn this from a “curiosity” into a more visible asset.
- Longer-term NMIBC data and health economics: additional 3- and 5-year follow-up in both CIS and papillary cohorts (bladder-sparing, survival, quality of life, cost offsets vs cystectomy) can influence guidelines, payer coverage and ultimately the size of the ANKTIVA opportunity in bladder cancer.
- Quarterly earnings and guidance: every set of quarterly results (starting with FY 2025 numbers) will act as a recurring catalyst, updating the ANKTIVA revenue ramp, gross-to-net behavior, operating expense trends and cash runway.
5. Analysts & Valuation – What the “Street” is modeling
External expectations (not recommendations)Several independent analyst platforms currently classify IBRX as a “Strong Buy”, with:
- Average 12-month price targets around $9.7–10.4 per share;
- Target range roughly from $5 (low) to $24 (high), implying very different views on execution and peak sales;
- Commentary highlighting ANKTIVA’s revenue momentum, EU/UK regulatory gains, but also cash needs and competitive risks.
These targets are built on explicit assumptions (NMIBC penetration, pricing, EU/UK uptake, pipeline success, cost of capital). None of them are guarantees, and even reputable analysts can be very wrong on both timing and magnitude.
How to read analyst targets
Price targets are best treated as scenarios, not promises. They tell you what would need to go right (or wrong) to justify a certain price, not what the price will actually be. For risk management, the shape of the assumptions matters more than the absolute target.
6. Sentiment – Reddit, Stocktwits and X
Non-professional trader viewsThe IBRX community is loud and split. Across Reddit, Stocktwits and X, you see recurring patterns:
6.1 Bullish themes
- “Star of 2026” style theses, arguing that ANKTIVA’s NMIBC revenue, EU entry and potential label expansions could eventually support multi-billion sales and rerating from small-cap to mid-cap valuations.
- Strong conviction that ANKTIVA is difficult to copy as a biologic and that it provides durable, chemo-free responses in bladder cancer.
- Frequent references to new data drops and positive PRs as catalysts for short squeezes or large percentage moves.
6.2 Bearish / skeptical themes
- Concerns that “media pumps never last” and that every spike eventually fades to lower lows if fundamentals and communication don’t improve.
- Focus on cash burn, financing structures and dilution risk – a recurring theme among more cautious posters.
- Criticism of management’s communication style and event execution (e.g. webcast quality, clarity of regulatory messaging).
All of these are opinions from non-professional traders/investors. They can be useful to understand crowd positioning and psychology, but they are not research and not a reliable decision tool on their own.
These links may include affiliate/referral components. They do not change our editorial view and are not endorsements of any specific service.
7. Key Risks & Red Flags
Where things can go wrong7.1 Clinical & regulatory risk
High ANKTIVA is approved in a specific NMIBC subset; label expansions (papillary, other tumors, new geographies) are not guaranteed. Past events like the BLA CRL and papillary sBLA RTF illustrate that regulatory paths can be bumpy even with strong efficacy.
7.2 Commercial execution & payer dynamics
Medium / execution-sensitive Adoption depends on:
- urologists’ comfort with ANKTIVA + BCG vs Keytruda or surgery;
- real-world safety and durability outside trial settings;
- pricing, reimbursement and formulary placement in the US and EU;
- capacity to scale manufacturing and distribution reliably.
7.3 Balance sheet & financing
High Even with revenue growth and improved cash, IBRX remains a company with substantial operating losses, heavy R&D and commercialization spend, and revenue interest/financing obligations. Future capital raises or deal structures are a real possibility if the ANKTIVA ramp or EU launch underperform.
7.4 Platform complexity
Medium The integrated IL-15 + NK-cell + vaccine vision is scientifically appealing but operationally complex. Combining multiple advanced modalities in late-stage pipelines increases both cost and execution risk.
7.5 Volatility & crowding
Medium–High IBRX is heavily traded by retail and momentum-oriented accounts. That means:
- sharp swings around news (both positive and negative);
- episodes of over-reaction in both directions;
- gaps between long-term fundamentals and short-term price moves.
8. Scenario Map – Neutral high-level view
Not a recommendation8.1 Constructive scenario (what would need to go right)
- Sustained ANKTIVA uptake in US NMIBC CIS, with broad payer coverage and good real-world outcomes.
- EMA conditional approval converts into a solid EU franchise with meaningful revenue contribution.
- Papillary label issues with the FDA are resolved in a way that expands the treatable population.
- Lymphopenia and one or two solid tumor programs generate convincing data and clear regulatory paths.
- Cash burn moderates as revenue grows, reducing the need for dilutive financings.
8.2 Cautious / downside scenario (what could break)
- US uptake plateaus below expectations or faces pricing/reimbursement pressure.
- EU launch is slower than hoped, with fragmented adoption across countries.
- Further regulatory friction around label expansions erodes confidence.
- Pipeline outside bladder cancer fails to show compelling risk/benefit.
- Additional financing on less-attractive terms leads to shareholder dilution and sentiment fatigue.
Again: these are scenarios, not forecasts. The goal is to outline the main paths, not to assign probabilities or make trade calls.
9. Sources & Further Reading
Clickable official references- EMA (EU): European Medicines Agency portal (news, CHMP opinions, EPAR when available): https://www.ema.europa.eu/en
- FDA (US): Drug Trials Snapshot hub (use search for “ANKTIVA / nogapendekin alfa inbakicept”): https://www.fda.gov/drugs/drug-trials-snapshots
- ImmunityBio official press releases (EU update, long-term NMIBC outcomes, Saudi MOU, quarterly results): https://ir.immunitybio.com/news-releases
- ImmunityBio SEC filings (10-Q, financial statements, cash flow, risk factors): https://www.sec.gov/edgar/browse/?CIK=0001326110
- UK (MHRA): official MHRA medicines and approvals portal (use search for “Anktiva”): https://www.gov.uk/government/organisations/medicines-and-healthcare-products-regulatory-agency
- Clinical trials (official registry): use search for “N-803”, “ANKTIVA”, “nogapendekin”, “ResQ201A”: https://clinicaltrials.gov/
- Company product page / prescribing information (if published): ImmunityBio ANKTIVA product hub: https://www.immunitybio.com/
- Community sentiment (non-professional): Stocktwits ticker feed: https://stocktwits.com/symbol/IBRX
Note: some regulatory / PR URLs can change over time. The links above point to the official portals where the exact documents and announcements can be searched by title/date.
Educational / legal disclaimer (EN)
This content is for informational purposes only. It is not, and must not be interpreted as, investment advice, a solicitation, or a recommendation to buy or sell any security or financial instrument. All data are based on public sources (FDA, EMA, company filings, press releases and major financial news/analysis platforms) believed to be reliable, but errors and omissions are always possible. Readers should independently verify all key figures (including dates, cash, revenue, indications and regulatory status) using primary documents such as SEC filings, official regulatory websites and company disclosures.
Any reference to analyst price targets, ratings or community comments reflects third-party opinions and not the view of Merlintrader trading Blog. These opinions may change without notice and may be wrong. Trading and investing in biotech, especially small and mid caps, involves a high risk of capital loss and may be unsuitable for many investors. Always consult a qualified financial professional and consider local regulations (including CONSOB and SEC rules) before making decisions.
This content is for informational purposes only. It is not, and must not be interpreted as, investment advice, a solicitation, or a recommendation to buy or sell any security or financial instrument. All data are based on public sources (FDA, EMA, company filings, press releases and major financial news/analysis platforms) believed to be reliable, but errors and omissions are always possible. Readers should independently verify all key figures (including dates, cash, revenue, indications and regulatory status) using primary documents such as SEC filings, official regulatory websites and company disclosures.
Any reference to analyst price targets, ratings or community comments reflects third-party opinions and not the view of Merlintrader trading Blog. These opinions may change without notice and may be wrong. Trading and investing in biotech, especially small and mid caps, involves a high risk of capital loss and may be unsuitable for many investors. Always consult a qualified financial professional and consider local regulations (including CONSOB and SEC rules) before making decisions.
Legal resources of Merlintrader trading Blog (full disclaimer and privacy / terms of use):
https://merlintrader.com/disclaimer/
https://merlintrader.com/condizioni-duso-e-info-privacy/
My tale (personal view, not a recommendation)
This final note is a personal, non-advisory take on the risk/reward around IBRX. In simple terms, IBRX offers a speculative bull case: if ANKTIVA keeps ramping, the EU launch gains real traction and at least one major pipeline program (for example NSCLC) delivers convincing data, the risk/reward can tilt to the upside over the next few years. At the same time, this remains a high-risk, cash-hungry biotech story, with very real dilution and execution risk if growth or access disappoint. This is my personal opinion only and not a recommendation to buy, sell or hold the stock.
Biotech Catalyst Calendar
For a broader view of upcoming biotech catalysts (PDUFA dates, trial readouts, key regulatory events) beyond IBRX, you can consult the dedicated Biotech Catalyst Calendar maintained on Merlintrader.
Ticker: IBRX (NASDAQ)
ImmunityBio (IBRX) – ANKTIVA, NMIBC e la sfida di trasformare l’approvazione in cassa reale
Storia di immunoterapia IL-15 / cellule NK con un prodotto reale sul mercato, ricavi in forte crescita, cassa ancora tirata e una base retail molto rumorosa.
News del giorno – Perché IBRX è di nuovo sul radar
Aggiornamenti recentiOggi la storia IBRX ruota intorno a quanto lontano potrà arrivare ANKTIVA in NMIBC – e se l’attuale bilancio basta davvero a sostenere il resto della pipeline.
1) EMA favorevole ad ANKTIVA in Europa (dicembre 2025)
Il 12 dicembre 2025 l’EMA ha raccomandato la concessione di un’ autorizzazione condizionata all’immissione in commercio per ANKTIVA (nogapendekin alfa inbakicept) in combinazione con BCG negli adulti con NMIBC ad alto rischio, BCG-unresponsive, con CIS con o senza malattia papillare – sostanzialmente allineando l’Europa all’etichetta USA e basandosi sui dati dello studio QUILT-3.032.
2) Dati a 3 anni nel papillary-only
Pochi giorni dopo, ImmunityBio ha diffuso i dati a tre anni nei pazienti con NMIBC papillare-solo ad alto grado trattati con ANKTIVA + BCG, evidenziando 96% di sopravvivenza specifica per il tumore vescicale a tre anni, buona disease-free survival e tassi elevati di evitamento della cistectomia – numeri importanti per il posizionamento reale di ANKTIVA rispetto a BCG e chirurgia radicale.
3) Ramp commerciale: ricavi ora significativi, non ancora “comodi”
Dall’approvazione FDA (22 aprile 2024) per NMIBC BCG-unresponsive con CIS con o senza papillare, i ricavi di ANKTIVA sono cresciuti rapidamente: nel Q3 2025 ImmunityBio ha riportato circa $32M di fatturato e vendite YTD di ANKTIVA intorno a $75M, con volumi unitari in forte crescita anno su anno. Allo stesso tempo il cash burn operativo resta elevato (oltre $230M di flussi negativi su base annua), quindi il ramp è reale ma non ancora sufficiente a rendere la società auto-finanziata.
4) Il titolo resta da biotech ad alta beta
A fine dicembre 2025 IBRX scambia grosso modo in area $2,10–2,20, con un range 52 settimane di circa $1,83–4,27 e una capitalizzazione intorno a $2,1 miliardi. Il titolo resta volatile e molto sensibile a news regolatorie, discussioni sulla cassa e flussi momentum dalla componente retail.
Dati rapidi – IBRX in una schermata
Snapshot (fine dic 2025)Ticker / MercatoIBRX – Nasdaq
Prezzo azione≈ $2,14 (26 dic 2025)
Range 52 settimane$1,83 – $4,27
Market cap≈ $2,1 mld
SettoreOncologia / Immunoterapia
StadioBiotech commerciale
Prodotto leaderANKTIVA (N-803, agonista IL-15)
Indicazione approvataNMIBC BCG-unresponsive con CIS ± papillare (USA)
Status UERaccomandazione EMA per AIC condizionata (dic 2025)
Ricavi Q3 2025~$32M (+400%+ a/a)
Vendite ANKTIVA 2025 YTD~$75M
Cassa + titoli~$258M (30 set 2025)
Cash burn operativo YTD≈ $230M+
Consenso analisti“Strong Buy” (analisti terzi)
PT 12 mesi (medio)~$9,7–10,4 (range $5–24)
Dati ricavati da comunicati/filing ImmunityBio, Nasdaq/Yahoo Finance, MarketBeat, StockAnalysis e Investing.com. Valori arrotondati e solo a fini informativi, non per decisioni operative.
Piattaforma IL-15 + cellule NK
Tumore vescicale NMIBC
Alta volatilità
Pipeline a forte consumo di cassa
Executive summary – Cosa è (e cosa non è) ImmunityBio
Contesto per chi non è specialistaImmunityBio non è più solo una “story stock”: oggi ha un prodotto approvato dalla FDA – ANKTIVA, agonista del recettore IL-15 usato con BCG nel NMIBC BCG-unresponsive con CIS. I ricavi stanno crescendo in modo significativo da una base bassa, ma il resto della storia assomiglia ancora molto a un’immuno-oncologia ad alto rischio.
- Fondamento clinico: ANKTIVA + BCG ha mostrato circa 71% di risposta completa nei pazienti con CIS e NMIBC BCG-unresponsive, con durata mediana di risposta intorno a 24 mesi e buoni tassi di preservazione della vescica, ora rafforzati da dati a lungo termine e riconoscimento regolatorio in USA, UK e (in forma condizionata) UE.
- Angolo piattaforma: ANKTIVA è la “punta dell’iceberg” di una piattaforma che comprende combinazioni IL-15, terapie cellulari NK-92 / t-haNK e vaccini adenovirali per diversi tumori solidi e malattie infettive.
- Realtà commerciale: il Q3 2025 mostra ~$32M di ricavi con volumi ANKTIVA in forte crescita, ma le perdite operative restano superiori a $60M a trimestre e il cash burn annuo oltre $200M. La cassa attuale (~$258M) dà tempo, non tranquillità piena.
- Upside regolatorio vs execution risk: i driver 2025–26 includono approvazione formale e lancio UE, gestione del dossier papillary (sBLA USA), adozione reale nel NMIBC e maturazione dei programmi su linfopenia e tumori solidi. Tutto questo aggiunge opzionalità ma anche rischio esecutivo (pricing, accesso, produzione).
- Aspettative di mercato: diversi analisti terzi vedono IBRX con rating “Strong Buy” e target medi intorno a $9–10 a 12 mesi (range $5–24), basati su scenari di picco ricavi molto superiori a quelli attuali e tutt’altro che pienamente deriskati.
- Sentiment retail: Reddit, Stocktwits e X mostrano una classica spaccatura: una componente molto bullish (“star del 2026”) versus trader più scettici focalizzati su rischio diluizione, comunicazione del management e strategia media. Si tratta di opinioni di trader non professionisti.
L’obiettivo è dare una fotografia completa di dati, scenari e rischi noti, in modo che il lettore possa farsi una propria idea. Non è in alcun modo una raccomandazione ad acquistare o vendere titoli.
1. Azienda e piattaforma – Cosa sta cercando di costruire ImmunityBio
Stack IL-15 + NK-cell + vacciniImmunityBio si presenta come una piattaforma di immunoterapia basata su tre pilastri: ANKTIVA (superagonista IL-15), cellule NK-92 / t-haNK ingegnerizzate e una piattaforma vaccinale adenovirale di nuova generazione.
1.1 ANKTIVA (N-803) – Superagonista IL-15 come asset principale
ANKTIVA (nogapendekin alfa inbakicept-pmln, ex N-803) è un complesso IL-15 superagonista che espande e attiva cellule NK e T CD8+, potenziando la risposta antitumorale. Nel NMIBC viene somministrato per via intravescicale con BCG, mentre in altri setting è testato per via sistemica o intralesionale.
1.2 Piattaforma NK-92 / t-haNK
La famiglia NK-92 comprende linee cellulari NK ad alta affinità (haNK) e CAR-NK (t-haNK) contro target come PD-L1 e CD19. Queste terapie sono in studi di fase iniziale e intermedia in tumori solidi difficili (pancreas, TNBC, glioblastoma, testa-collo) e in alcune neoplasie ematologiche.
1.3 Vaccini adenovirali (hAd5) e concetto NANT Cancer Vaccine
ImmunityBio possiede anche una piattaforma vaccinale hAd5, usata sia in oncologia sia in malattie infettive (es. candidati vaccini COVID-19 e vaccini neoantigenici). L’idea è combinare:
- checkpoint inhibitor,
- superagonista IL-15 (ANKTIVA),
- terapie cellulari NK (haNK / t-haNK),
- vaccini adenovirali,
per orchestrare una risposta sinergica del sistema immunitario contro il tumore.
Sulla carta la piattaforma è potente. Dal punto di vista azionario, però, la domanda chiave nel breve è: ANKTIVA nel NMIBC riuscirà a generare cassa sufficiente per sostenere tutto il resto?
2. ANKTIVA nel NMIBC – Dal CRL all’approvazione fino all’Europa
Asset chiave, execution chiave2.1 Percorso regolatorio
- 2023 – Complete Response Letter (CRL): la prima BLA per N-803 + BCG in NMIBC BCG-unresponsive con CIS riceve una CRL nel maggio 2023, legata soprattutto a ispezioni produttive, non a problemi di efficacia clinica.
- 2024 – Approvazione FDA: dopo la resubmission, la FDA approva ANKTIVA + BCG il 22 aprile 2024 per pazienti adulti con NMIBC BCG-unresponsive con CIS con o senza tumori papillari.
- Approvazione UK: nel 2025 l’MHRA britannica approva ANKTIVA + BCG nello stesso setting, consolidando il profilo regolatorio internazionale.
- 2025 – Raccomandazione condizionata EMA: a dicembre 2025 il CHMP raccomanda l’autorizzazione condizionata UE per ANKTIVA + BCG nel NMIBC BCG-unresponsive con CIS, con o senza papillare.
2.2 Efficacia clinica
La Drug Trials Snapshot FDA e i dati di QUILT-3.032 mostrano che ANKTIVA + BCG ha ottenuto circa 71% di risposta completa nei pazienti con CIS BCG-unresponsive, con durata mediana di risposta intorno a 24,1 mesi. Il follow-up a lungo termine suggerisce buona preservazione vescicale e sopravvivenza cancro-specifica favorevole, con il recente 96% a tre anni nel papillary-only che rafforza ulteriormente il profilo.
2.3 Scenario competitivo
Nel NMIBC BCG-unresponsive, ANKTIVA si confronta con:
- Keytruda (pembrolizumab) – terapia sistemica IV con suo profilo benefit/risk.
- Regimi intravescicali tradizionali (mitomicina, gemcitabina-docetaxel, ecc.).
- Cistectomia radicale – standard definitivo ma altamente impattante sulla qualità di vita.
Il posizionamento di ANKTIVA punta su: immunoterapia locale che potenzia il BCG, con risposte durature e riduzione della necessità di cistectomia. Quanto rapidamente urologi e payer sposeranno questo posizionamento sarà uno dei driver principali del caso IBRX.
3. Ramp commerciale e numeri – Ricavi vs consumo di cassa
Crescita reale, ma ancora fase di scale-up3.1 Traiettoria dei ricavi
Dalla disponibilità commerciale, ANKTIVA ha mostrato una crescita significativa:
- Q1 2025: ~$16,5M di ricavi, già in netto aumento rispetto alla fine del 2024.
- Q2 2025: ~$26,4M (+60% vs Q1), con vendite YTD ~$43M e volumi +246% vs 2H 2024.
- Q3 2025: ~$32M, oltre +400% anno su anno, a conferma di un’adozione in accelerazione.
3.2 Cassa, burn e struttura finanziaria
Al 30 settembre 2025 ImmunityBio riportava circa $257,8M di cassa, equivalenti e titoli, in crescita rispetto ai ~<$154M di fine Q2 2025, grazie a finanziamenti esterni e all’aumento dei ricavi. Il cash burn operativo annuo resta però superiore a $200M, con presenza di strutture di financing e revenue interest che aggiungono complessità.
Tradotto in termini neutri: l’azienda è in piena fase di scale-up, con execution risk elevato su produzione, rete commerciale, outcomes real world, accesso rimborsato e future estensioni di etichetta.
3.3 Implicazioni (non operative)
- ANKTIVA genera ormai ricavi materialmente rilevanti, ma non ancora sufficienti a “pagare il conto” dell’intera piattaforma.
- La runway è migliorata ma non infinita; in caso di ramp più lento del previsto o spese elevate, ulteriori operazioni di capitale non possono essere escluse.
- Eventuali intoppi su adozione, prezzo o rimborsi hanno impatto diretto e rapido sulla narrativa di mercato.
4. Pipeline e catalyst – Oltre il NMIBC
Opzionalità vs concentrazione4.1 Estensione di etichetta nel papillary
Nell’aprile 2025 ImmunityBio ha completato l’invio di una sBLA alla FDA per estendere ANKTIVA + BCG al NMIBC BCG-unresponsive papillare oltre il CIS, ma la domanda ha incontrato un Refusal-to-File (RTF) e la società ha chiesto un meeting di tipo A per chiarire le linee guida. Una risoluzione positiva amplierebbe la popolazione trattabile e rafforzerebbe l’economia del franchise bladder.
4.2 Linfopenia e Cancer BioShield
Nel 2025 ANKTIVA ha ricevuto anche un’Expanded Access authorization FDA per il trattamento della linfopenia in tumori solidi, nell’ambito del concetto Cancer BioShield. Non è un driver di ricavi nel breve, ma è un tassello interessante sul piano scientifico e di posizionamento.
Oltre al programma statunitense, a maggio 2025 ImmunityBio ha firmato un Memorandum of Understanding strategico in Arabia Saudita per portare la piattaforma Cancer BioShield in Medio Oriente. L’accordo, annunciato durante il Saudi–U.S. Investment Forum 2025 a Riad, coinvolge il Ministero dell’Investimento saudita (MISA), il King Faisal Specialist Hospital & Research Centre (KFSHRC) e il King Abdullah International Medical Research Center (KAIMRC).
- Obiettivi: introdurre terapie immuno-ristorative e localizzare la produzione biotecnologica in linea con la National Biotech Strategy saudita.
- Attività previste: conduzione di trial clinici in loco, trasferimento di know-how scientifico, formazione del personale sanitario e possibile creazione di sussidiarie regionali in Medio Oriente.
Dal punto di vista strategico, questo accordo posiziona ImmunityBio come attore precoce nel mercato mediorientale dell’immunoterapia e potrebbe, nel tempo, contribuire almeno in parte ad alleviare la pressione finanziaria legata all’elevato cash burn descritto nel report.
4.3 Tumori solidi (pancreas, polmone, TNBC, GBM…)
Diverse sperimentazioni valutano ANKTIVA in combinazione con checkpoint inhibitor, chemioterapia e terapie NK in:
- tumore pancreatico, TNBC e testa-collo (strategie tipo “NANT Cancer Vaccine”);
- NSCLC e altri solidi, con ANKTIVA per il “rescue” della linfopenia e combinazione con t-haNK PD-L1;
- NHL con cell therapy t-haNK CD19.
Per ora questi programmi valgono soprattutto come opzionalità di lungo periodo.
4.4 Prossimi catalyst e tappe future
Non ci sono più date formali in stile PDUFA, ma il mercato guarda alcune tappe piuttosto chiare nei prossimi 12–36 mesi:
- Decisione finale UE e lancio europeo: dopo l’opinione positiva del CHMP di dicembre 2025, la decisione della Commissione Europea sull’autorizzazione condizionata di ANKTIVA è attesa nella prima parte del 2026. Il ritmo di adozione nei primi paesi sarà un test importante.
- Chiarezza regolatoria sul papillary-only NMIBC: l’esito del Type A meeting richiesto dopo la RTF di maggio 2025 e l’eventuale nuovo piano (nuovi dati, possibile trial randomizzato, resubmission) sono un catalyst strutturale per la dimensione del franchise vesicale.
- ResQ201A (Phase 3 NSCLC): il trial registrazionale nei pazienti NSCLC resistenti al checkpoint è in corso; il management ha indicato in diversi aggiornamenti nel 2025 l’obiettivo di presentare una BLA nel 2025 per la seconda/terza linea NSCLC dopo fallimento del checkpoint, anche se la tempistica effettiva resta legata a enrollment, maturità dei dati e confronto con la FDA.
- Programma linfopenia / Cancer BioShield: l’evoluzione dall’Expanded Access a una potenziale via registrazionale più strutturata, insieme ai primi dati real world in pazienti sottoposti a chemio/radioterapia/checkpoint, può cambiare il peso percepito di questo asset.
- Dati long-term su NMIBC e health economics: ulteriori follow-up a 3 e 5 anni nei cohort CIS e papillare (preservazione vescica, sopravvivenza, qualità di vita, confronto economico vs cistectomia) possono influenzare linee guida e rimborsi.
- Trimestrali e guidance: ogni nuova trimestrale (a partire dai risultati FY 2025) è un catalyst ricorrente, perché aggiorna la traiettoria dei ricavi ANKTIVA, il profilo gross-to-net, l’andamento dei costi e la runway di cassa.
5. Analisti e valutazione – Cosa sta prezzando il “mercato istituzionale”
Aspettative esterne (non consigli)Diverse piattaforme riportano su IBRX un rating medio “Strong Buy” da parte di analisti terzi, con:
- target medi a 12 mesi intorno a $9,7–10,4 per azione;
- range ampio tra $5 (low) e $24 (high), che riflette opinioni molto diverse su execution e picco ricavi;
- commenti che evidenziano sia il momentum di ANKTIVA e le tappe regolatorie, sia la persistenza dei rischi di cassa e concorrenza.
Sono stime, non certezze. Anche analisti molto preparati possono sbagliare timing e numeri in modo significativo, soprattutto su storie biotech complesse come ImmunityBio.
Come usare (bene) i target
Ha senso trattare i target come scenari condizionati: indicano “cosa dovrebbe succedere” perché quel numero abbia senso, non dove andrà effettivamente il prezzo. Il valore sta nella logica sottostante (ipotesi su volumi, prezzi, margini, costi, rischio regolatorio), non nella cifra secca.
6. Sentiment – Reddit, Stocktwits e X
Opinioni di trader non professionistiLa community su IBRX è rumorosa e polarizzata. In sintesi:
6.1 Narrativa bullish
- Tesi tipo “potenziale star del 2026”, con aspettative di ricavi miliardari nel NMIBC, espansione UE/UK e multiple di valutazione in stile mid-cap in caso di execution riuscita.
- Enfasi sulla difficoltà di replicare ANKTIVA come biologico e sulla possibilità di risposte durature senza chemioterapia in vescicale.
- Forte attenzione ai nuovi dati e ai PR come possibili trigger di squeeze e movimenti percentuali a due cifre.
6.2 Narrativa scettica / bear
- Critiche ai “media pump” percepiti come temporanei, con l’idea che ogni spike si traduca poi in nuovi minimi se la comunicazione e i numeri non migliorano.
- Focus su cash burn, diluizione e strutture di finanziamento come rischio strutturale.
- Lamentele sulla qualità della comunicazione del management (eventi, webcast, chiarezza delle guidance).
Tutti questi sono commenti di utenti retail, non report di analisti registrati. Possono aiutare a capire il clima di mercato, ma non dovrebbero essere usati come base decisionale.
Questi link possono includere elementi di affiliazione. Non modificano in alcun modo il contenuto editoriale e non costituiscono un invito a usare servizi specifici.
7. Rischi principali e red flags
Dove la storia può incepparsi7.1 Rischio clinico/regolatorio
Alto ANKTIVA è approvata in un sottogruppo preciso di NMIBC; le estensioni di etichetta (papillary, altre indicazioni, ulteriori geografie) non sono garantite. Eventi come la CRL e la RTF sulla sBLA ricordano che il percorso può restare accidentato.
7.2 Esecuzione commerciale e payers
Medio / execution-driven Il successo dipende da:
- adozione da parte degli urologi rispetto a Keytruda o alle opzioni chirurgiche;
- dati real world e profilo di sicurezza nel tempo;
- prezzo, rimborsabilità e posizionamento in prontuario negli USA e in Europa;
- capacità produttiva e logistico-distributiva.
7.3 Struttura finanziaria
Alto Nonostante il ramp di ricavi e la migliore posizione di cassa, IBRX resta una società con forti perdite operative, spese R&D/commerciali elevate e obbligazioni finanziarie non banali. Nuovi aumenti di capitale o deal diluitivi sono scenari da tenere in conto se qualcosa nel ramp dovesse rallentare.
7.4 Complessità della piattaforma
Medio L’idea di combinare IL-15, NK-cell therapy e vaccini è affascinante ma operativamente complessa. Ogni livello aggiunge costi, rischi e punti di failure potenziali.
7.5 Volatilità e crowding
Medio–Alto Il titolo è fortemente presente su canali retail; questo si traduce in spike improvvisi, ritracciamento veloce e scostamenti frequenti tra fondamentali e prezzo nel breve.
8. Mappa scenari – Vista neutrale ad alto livello
Nessuna raccomandazione8.1 Scenario costruttivo (cosa dovrebbe andare bene)
- adozione sostenuta di ANKTIVA nel NMIBC CIS USA con buona copertura payer;
- ricavi significativi dall’Europa dopo l’autorizzazione condizionata EMA;
- risoluzione favorevole del dossier papillary;
- dati convincenti su linfopenia e almeno uno-due tumori solidi;
- riduzione progressiva del cash burn grazie alla crescita dei ricavi.
8.2 Scenario prudente / downside (cosa può rompersi)
- adozione più lenta del previsto o frizioni su prezzo/rimborsi;
- lancio UE in ordine sparso e meno impattante del previsto;
- ulteriore frizione regolatoria sulle estensioni di etichetta;
- pipeline extra-NMIBC che non produce dati abbastanza forti;
- nuova raccolta di capitale con impatto diluitivo significativo.
Anche qui, l’obiettivo è solo mappare i possibili percorsi, non assegnare probabilità o esprimere giudizi operativi.
9. Fonti e letture di approfondimento
Link cliccabili alle fonti ufficiali- EMA (UE): portale ufficiale EMA (news, opinioni CHMP, EPAR quando disponibile): https://www.ema.europa.eu/en
- FDA (USA): hub Drug Trials Snapshot (cerca “ANKTIVA / nogapendekin alfa inbakicept”): https://www.fda.gov/drugs/drug-trials-snapshots
- Press release ufficiali ImmunityBio (update UE, dati long-term, MOU Arabia Saudita, trimestrali): https://ir.immunitybio.com/news-releases
- Filing SEC (10-Q, cash flow, rischi): https://www.sec.gov/edgar/browse/?CIK=0001326110
- UK (MHRA): portale ufficiale MHRA (cerca “Anktiva”): https://www.gov.uk/government/organisations/medicines-and-healthcare-products-regulatory-agency
- Clinical trials (registro ufficiale): https://clinicaltrials.gov/
- Sito aziendale (overview prodotti e piattaforma): https://www.immunitybio.com/
- Sentiment community (non professionale): Stocktwits feed ticker: https://stocktwits.com/symbol/IBRX
Nota: alcuni URL di comunicati o pagine regolatorie possono cambiare nel tempo. I link sopra puntano ai portali ufficiali dove puoi trovare i documenti esatti cercando per titolo o data.
Disclaimer educativo / legale (IT)
Questo contenuto ha finalità esclusivamente informative ed editoriali. Non costituisce in alcun modo consulenza finanziaria, sollecitazione al pubblico risparmio, offerta o raccomandazione personalizzata di investimento, né sostituisce il giudizio autonomo del lettore.
I dati riportati sono tratti da fonti pubbliche (FDA, EMA, comunicati e filing ImmunityBio, principali piattaforme di dati e analisi). Nonostante l’attenzione nella verifica, sono sempre possibili errori od omissioni. Il lettore deve verificare in autonomia tutte le informazioni rilevanti (date, importi, stati regolatori, ecc.) su documenti ufficiali (SEC, siti regolatori, comunicati aziendali).
I riferimenti a target di prezzo, rating o commenti di community riflettono opinioni di terzi e non l’opinione di Merlintrader trading Blog. Il trading/investing in titoli biotech, in particolare small e mid cap, comporta un rischio elevato di perdita del capitale ed è spesso inadatto a molti investitori. Prima di qualsiasi decisione è opportuno rivolgersi a un consulente finanziario abilitato e considerare le normative applicabili (incluse quelle CONSOB e SEC).
Questo contenuto ha finalità esclusivamente informative ed editoriali. Non costituisce in alcun modo consulenza finanziaria, sollecitazione al pubblico risparmio, offerta o raccomandazione personalizzata di investimento, né sostituisce il giudizio autonomo del lettore.
I dati riportati sono tratti da fonti pubbliche (FDA, EMA, comunicati e filing ImmunityBio, principali piattaforme di dati e analisi). Nonostante l’attenzione nella verifica, sono sempre possibili errori od omissioni. Il lettore deve verificare in autonomia tutte le informazioni rilevanti (date, importi, stati regolatori, ecc.) su documenti ufficiali (SEC, siti regolatori, comunicati aziendali).
I riferimenti a target di prezzo, rating o commenti di community riflettono opinioni di terzi e non l’opinione di Merlintrader trading Blog. Il trading/investing in titoli biotech, in particolare small e mid cap, comporta un rischio elevato di perdita del capitale ed è spesso inadatto a molti investitori. Prima di qualsiasi decisione è opportuno rivolgersi a un consulente finanziario abilitato e considerare le normative applicabili (incluse quelle CONSOB e SEC).
Risorse legali Merlintrader trading Blog:
https://merlintrader.com/disclaimer/
https://merlintrader.com/condizioni-duso-e-info-privacy/
My tale (opinione personale, non raccomandazione)
Questa sezione è una mia lettura personale del profilo rischio/rendimento di IBRX, e non una raccomandazione operativa.
In sintesi vedo su IBRX un bull case speculativo: se il ramp di ANKTIVA prosegue, il lancio europeo prende davvero trazione
e almeno uno dei programmi chiave di pipeline (per esempio NSCLC) porta dati convincenti, il rapporto rischio/rendimento può spostarsi a favore dello scenario positivo
nel medio periodo.
Allo stesso tempo resta una storia ad alto rischio e forte consumo di cassa, con rischio di diluizione ed execution molto concreto
se crescita, accesso o pricing dovessero deludere. È una mia opinione personale, non una raccomandazione di acquisto, vendita
o mantenimento del titolo.
Biotech Catalyst Calendar
Per una panoramica più ampia delle prossime date chiave biotech (PDUFA, readout, eventi regolatori), puoi fare riferimento al Biotech Catalyst Calendar mantenuto su Merlintrader.
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.



