DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
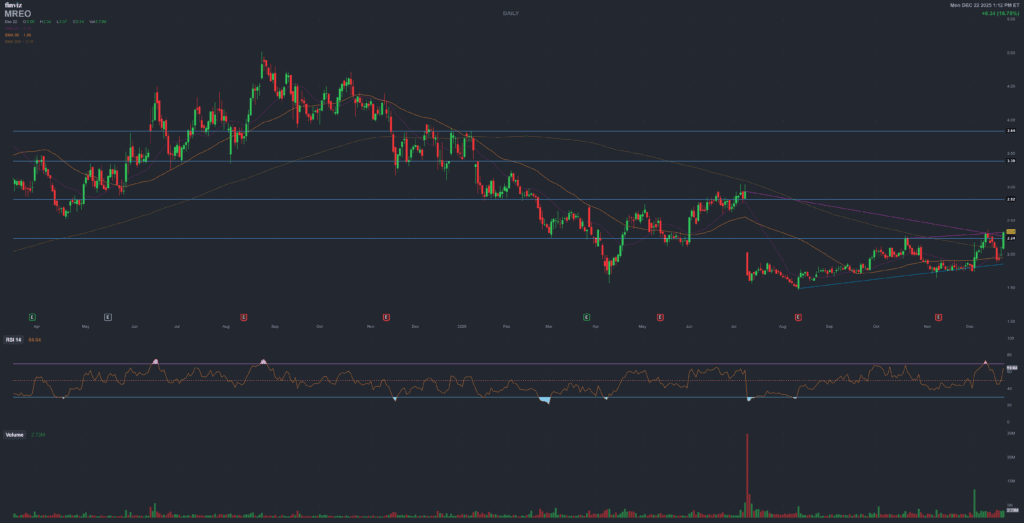
Mereo BioPharma (MREO) – Setrusumab in brittle bone disease and the rare disease pivot
Long-form, filings-based look at Mereo BioPharma at the end of 2025: the Phase 3 Orbit and Cosmic studies of setrusumab (UX143) in osteogenesis imperfecta, the alvelestat lung program, the new vantictumab partnership and how a once “forgotten” biotech is trying to become a focused rare-disease company.
MREO
Nasdaq | Mereo BioPharma Group plc
News of the day – 22 Dec 2025
Setrusumab: Phase 3 Orbit and Cosmic moving to final analysis after “no early stop” shock
In July 2025, Ultragenyx and Mereo announced that the second interim analysis of the Phase 3 Orbit study in osteogenesis imperfecta did not meet the high statistical bar required for early termination, so the trial is continuing to its planned final analysis in Q4 2025 – with data from both Orbit and Cosmic expected around year-end.
- The July announcement triggered a 25–40% sell-off in Ultragenyx and Mereo as investors had been hoping for an early stop on overwhelming efficacy; instead the Data Monitoring Committee recommended continuing as planned, citing acceptable safety.
- Subsequent quarterly updates from Mereo reiterated that both the Phase 3 Orbit and Phase 3 Cosmic studies of setrusumab remain on track for final analyses around the end of 2025, after at least 18 months of treatment. The p-value thresholds for success have been pre-specified (Orbit p<0.04, Cosmic p<0.05).
- Management continues to guide that, if final data are positive, the partners intend to move toward regulatory filings in the US and EU, with Mereo retaining commercial rights in Europe while Ultragenyx leads elsewhere.
Executive summary
Mereo BioPharma is now a concentrated bet on setrusumab (UX143), an anti-sclerostin monoclonal antibody partnered with Ultragenyx for osteogenesis imperfecta (OI), plus a back-up program in respiratory alpha-1 antitrypsin deficiency (alvelestat) and an earlier-stage bone asset (vantictumab) licensed to āshibio for autosomal dominant osteopetrosis type 2, where Mereo retains European commercial rights.
The investment narrative in 2025 has been dominated by the Phase 3 Orbit and Cosmic studies of setrusumab in OI: fully enrolled, on track for final analysis around year-end 2025 and explicitly described by management as a “major transition” point in the company’s evolution. The second interim analysis in mid-2025 failed to justify an early stop, triggering a sharp share-price correction, but did not reveal new safety concerns, and the trials are continuing as planned.
Financially, Mereo is a small-cap clinical-stage company with no product revenue, modest operating expenses by biotech standards, and a cash balance in the high-forty-million range as of Q3 2025, which management believes is sufficient to fund operations into 2027 – through the setrusumab Phase 3 readouts and the next steps for alvelestat partnering.
This deep dive focuses on: (1) what we actually know about setrusumab’s Phase 3 design, thresholds and timelines; (2) the strategic and financial position of Mereo going into those readouts; (3) the status and potential of alvelestat and vantictumab; and (4) how current sentiment frames the risk/reward – without trying to predict a specific share price outcome.
Company overview
Mereo BioPharma describes itself as a rare disease focused, clinical-stage biopharma. After spinning out and then shelving a series of oncology and endocrine assets, the company has concentrated its efforts on two main product candidates: setrusumab for osteogenesis imperfecta and alvelestat for severe alpha-1 antitrypsin deficiency-associated lung disease (AATD-LD). A newer partnered asset, vantictumab, adds another rare bone disease angle (autosomal dominant osteopetrosis type 2).
Strategically, the idea is simple: let Ultragenyx drive most of the global heavy lifting on setrusumab, while Mereo keeps European commercial rights and a meaningful share of the economics. In parallel, alvelestat is being positioned for a Phase 3 trial in AATD-LD, backed by Orphan Drug Designation and Fast Track in the US and positive orphan opinions in Europe. Management is actively seeking a partner to co-fund and eventually commercialise alvelestat.
The company’s own materials present 2025–2026 as a “milestone-rich period” centered on setrusumab’s Phase 3 data and alvelestat partnering. Everything else – valuation, deal options, and long-term independence – flows from how those two assets perform.
Pipeline snapshot: setrusumab, alvelestat and vantictumab
| Program | Indication | Partner / region | Stage |
|---|---|---|---|
| Setrusumab (UX143) | Osteogenesis imperfecta (OI), pediatric & young adult | Ultragenyx leads global development; Mereo retains European rights | Phase 3 Orbit (peds & young adults, 5–25 years) and Cosmic (2–<7 years), progressing toward final analyses around year-end 2025. |
| Alvelestat | Severe AATD-associated lung disease (AATD-LD) | Mereo (planning to partner for Phase 3 and commercialisation) | Phase 2 data support Phase 3 readiness; Orphan Drug Designation and Fast Track in US; positive EMA orphan opinion and expected EU Orphan Designation in 2025. |
| Vantictumab (anti-Wnt) | Autosomal dominant osteopetrosis type 2 (ADO2) | License to āshibio; Mereo retains European commercial rights | Preclinical/early clinical rare bone disease program; promising preclinical data presented at ASBMR 2025. |
Older oncology programs (such as navicixizumab) and endocrine assets have been effectively deprioritised or out-licensed; they no longer drive the core valuation. The entire equity story is increasingly concentrated on whether setrusumab can clear the Phase 3 bar and translate into a commercially viable OI therapy.
Catalyst and timeline overview (2025 – 2027)
Q1 2025
Orbit IA2 guidance and AATD orphan opinion
Mereo reiterates that the Phase 3 Orbit study in OI is on track either to read out at a second interim analysis in mid-2025 or at final analysis in Q4 2025. The company also announces that the EMA’s Committee for Orphan Medicinal Products has issued a positive opinion on European Orphan Designation for alvelestat in AATD-LD, with a formal Commission decision expected in early 2025.
Jul 2025
Orbit second interim: no early stop, sentiment hit
Ultragenyx and Mereo report that the second interim analysis of Orbit did not meet the high bar for early stopping on efficacy. The Data Monitoring Committee recommends continuing to final analysis with acceptable safety. The market reacts violently, with both RARE and MREO dropping 25–40% in a single session as investors reset expectations from “early stop” fantasy back to “wait for final data”.
Aug–Nov 2025
Q2/Q3 updates: year-end data and cash runway
In Q2 and Q3 financial updates, Mereo reiterates that data from the Phase 3 Orbit and Cosmic studies are expected around the end of 2025, with patients on therapy for at least 18 months. The company reports cash of USD 56.1M at 30 Jun and USD 48.7M at 30 Sep, and continues to guide that this should fund operations into 2027, including launch-readiness activities in Europe for setrusumab if the data are positive.
Year-end 2025 / early 2026
Final Orbit and Cosmic analyses
Final analyses of Orbit and Cosmic are expected once patients have completed at least 18 months of treatment. Success would likely mean a statistically significant reduction in fracture rates versus control in Orbit and a clear advantage over IV bisphosphonates in Cosmic. Failure or borderline results would materially damage the case for setrusumab as a future standard-of-care in OI.
2026–2027
Regulatory path and potential EU launch
Assuming positive Phase 3 results, Mereo and Ultragenyx have indicated that they would aim for regulatory submissions in US and EU, with a possible first launch in 2027. In Europe, Mereo is preparing to commercialise setrusumab directly (or via partners) in its retained territory, while Ultragenyx leads in the US and other regions.
Financial snapshot and capital position
In Q3 2025, Mereo reported cash and cash equivalents of USD 48.7M and reiterated guidance that this should fund operations into 2027, assuming continued prudent spending. Net loss for the quarter was about USD 7.0M, materially lower than a year earlier, reflecting a streamlined operating structure focused on rare disease programs and currency effects.
The company reported no revenue in Q3 2025, as expected for a pre-commercial biotech, and continues to rely on a combination of prior financings and disciplined expense control. Unlike many peers, Mereo currently carries limited traditional financial debt, which reduces interest burden but also means that future larger trials or commercial build-out will require either new equity, non-dilutive deals or a strong partner contribution.
From a purely mechanical perspective, the balance sheet gives Mereo room to reach the setrusumab Phase 3 readouts and negotiate an alvelestat deal without being forced into emergency financing at any specific price. What it does not guarantee is that the science will cooperate – that remains the core risk.
Sentiment: analysts and retail
Sentiment – non-professional traders
After the July interim update, analysts at several firms framed the sell-off as “an overreaction to a non-event”, stressing that the final analysis has a lower statistical bar and that the DMC’s decision to continue the trial supports the safety profile. Some buy-rated notes explicitly highlight Mereo as a “leveraged play” on the Orbit/Cosmic final data, with upside if the final fracture-rate reduction matches or exceeds the mid-stage Orbit Phase 2 results.
On the retail side, MREO sits firmly in the “event-driven rare disease” bucket. Bulls point to: (1) prior Phase 2 data showing substantial reductions in fractures; (2) the potential for setrusumab to become a new standard-of-care in OI if Phase 3 delivers; (3) the attractive economics of retaining European rights; and (4) the relatively lean valuation versus the addressable population. Bears counter that the missed interim threshold may signal thinner efficacy than hoped, that fracture endpoints are noisy, and that an USD 50M-ish cash pile can evaporate quickly if things drag on.
As always, none of these opinions – bullish or bearish – are recommendations. They are useful mostly as context for how crowded, emotional or consensus-driven the trade has become around key data dates.
Scenario map: what could go right or wrong
Upside scenario (conceptual, not a prediction)
In the constructive scenario, final Orbit and Cosmic analyses show statistically and clinically meaningful reductions in fracture rates versus control, with acceptable safety and supportive bone mineral density data. Regulators accept these results as sufficient for approval, and Ultragenyx moves quickly toward filings in the US and EU. In Europe, Mereo is able to leverage its retained rights to build a focused OI commercial footprint, either directly or through regional partners, while alvelestat secures a strong partner and moves into Phase 3.
Execution / middle path
In a middle-of-the-road scenario, setrusumab’s Phase 3 data are positive but not spectacular – for example, meeting the statistical thresholds but with more modest effect sizes or heterogeneity across subgroups. Approval remains possible, but payers and physicians adopt the drug more cautiously, limiting peak penetration. Mereo may still benefit from European rights, but the commercial opportunity is more niche and sensitive to pricing and real-world data, while alvelestat’s partnering value depends heavily on how aggressive potential partners want to be in AATD.
Downside / risk-intensive scenario
In the downside scenario, final Orbit/Cosmic data fail to hit their primary endpoints or show a benefit that regulators and payers judge insufficient to justify approval and reimbursement. Alternatively, safety issues could emerge that materially weaken the benefit–risk balance. In that world, the rare disease setrusumab story unravels, leaving Mereo with a modest cash buffer, a Phase 3–ready but unpartnered alvelestat program and a partnered early-stage bone asset – a much thinner platform than the current valuation implies.
None of these scenarios are guaranteed. They are simply a framework for thinking about where the real risk resides: in the upcoming data, not in the day-to-day noise on the tape.
Risk map
Clinical and regulatory risk
Setrusumab is still in Phase 3. A negative or equivocal final readout would destroy a large part of the current equity story. Even in a positive case, regulators could ask for additional data or impose label restrictions that limit uptake.
Financing and dilution
With under USD 50M of cash, Mereo is better positioned than many micro-caps, but still not immune to financing risk. If data are weaker than hoped or timelines slip, new equity or less favourable deal terms could dilute existing shareholders.
Execution and partner dependence
Ultragenyx controls much of the operational execution on setrusumab. Mereo’s economic outcome depends on Ultragenyx’s prioritisation, pricing strategy and willingness to invest in OI as a commercial franchise. Misalignment or shifting priorities at the partner could constrain long-term value even if the drug is approved.
Bottom line
Mereo BioPharma has quietly become one of the more interesting small-cap rare disease names going into 2026: a lean balance sheet, a single pivotal program that could reshape the standard-of-care in a severe genetic bone disease, and a back-up lung asset with orphan designation and Phase 3 potential.
At the same time, this is an inherently binary, high-volatility setup. The July interim episode showed how quickly expectations can swing, and the final setrusumab readouts will carry even more weight. From a purely informational perspective, the company has enough cash to get to those data and negotiate its options – but the data themselves will decide whether “rare disease pivot” becomes a durable franchise or just another biotech story that nearly made it.
This report is not a recommendation to buy or sell MREO. It is a map of the hard facts and key uncertainties so that traders and investors can form their own view, rather than leaning on rumours or price action alone.
Key sources and links
- Mereo BioPharma – Q1, Q2 and Q3 2025 financial results and corporate highlights (setrusumab Orbit/Cosmic timelines, cash balance, runway guidance, description of rare disease focus).
- Ultragenyx – 2025 press releases and quarterly updates describing UX143 (setrusumab) Phase 3 Orbit and Cosmic studies, interim analysis outcomes, and final analysis timing.
- Mereo corporate update on lead clinical programs (January 2025) and full-year 2024 financial results for details on alvelestat orphan status and Phase 3 readiness.
- Public market commentary (Barron’s, Investors Business Daily, sell-side notes) on the July 2025 Orbit interim reaction, fracture reduction data from earlier studies and perceived potential for setrusumab to become standard-of-care in OI.
- Company and partner disclosures on the vantictumab/āshibio deal in autosomal dominant osteopetrosis type 2 and retention of European commercial rights by Mereo.
Some external links used for charts or tools (for example Finviz, Seeking Alpha, Stocktwits or broker platforms) may include affiliate or referral parameters for Merlintrader. These do not change the content you see or the price you pay, and they do not influence the conclusions of this analysis.
Legal and risk disclaimer
Informational only, not investment advice. This report is based on public information from company filings, regulatory documents and reputable news sources available at the time of writing. It may contain errors, omissions or data that become outdated as new information emerges.
Nothing in this text is a recommendation to buy, sell or hold any security, nor a solicitation to do so. The author is not a registered investment adviser or a licensed financial professional. Any references to scenarios, upside/downside or potential market behaviour are illustrative and not predictions.
Readers should perform their own due diligence, consider their personal financial situation and risk tolerance, and, where appropriate, consult a qualified financial professional. Rare disease biotech investing carries significant scientific, regulatory and commercial risk, including the possibility of losing some or all of the capital invested.
This content is intended for an international audience that includes readers in both the European Union and the United States. The language and structure aim to remain consistent with the spirit of applicable guidance from regulators such as CONSOB and the SEC for purely informational, non-promotional commentary.
Authors: Merlintrader and Jane.
For full legal notes and privacy information, please refer to:
Disclaimer
Termini di Servizio, Privacy, Cookie Policy // Term of Service, Privacy, Cookie Policy
Biotech Catalyst Calendar
For an updated overview of upcoming biotech and healthcare catalysts – PDUFA dates, clinical readouts, regulatory events – you can always refer to the dedicated Merlintrader Biotech Catalyst Calendar page.
Mereo BioPharma (MREO) – Setrusumab nell’osteogenesi imperfetta e la svolta rare disease
Analisi estesa, basata su documenti ufficiali, su Mereo BioPharma a fine 2025: gli studi di Fase 3 Orbit e Cosmic di setrusumab (UX143) nell’osteogenesi imperfetta, il programma alvelestat nel polmone da AATD, il nuovo accordo su vantictumab e il tentativo di trasformarsi in una vera rare-disease company.
MREO
Nasdaq | Mereo BioPharma Group plc
News del giorno – 22 dic 2025
Setrusumab: Orbit e Cosmic verso l’analisi finale dopo lo “stop mancato” a metà 2025
A luglio 2025 Ultragenyx e Mereo hanno comunicato che la seconda interim analysis dello studio Fase 3 Orbit nell’osteogenesi imperfetta non ha raggiunto la soglia statistica per chiudere in anticipo il trial. Il Comitato di Monitoraggio ha raccomandato di proseguire fino all’analisi finale prevista nel Q4 2025; i dati di Orbit e Cosmic sono attesi intorno a fine anno.
- L’annuncio ha innescato un sell-off violento (−25–40% su RARE e MREO), perché il mercato sperava in una chiusura precoce per efficacia “schiacciante”; in realtà il messaggio era: niente stop anticipato, ma studio che prosegue regolarmente con safety allineata alle aspettative.
- Gli aggiornamenti Q2/Q3 hanno ribadito che Orbit e Cosmic stanno procedendo verso l’analisi finale, con almeno 18 mesi di trattamento per i pazienti e soglie di significatività predefinite (p<0,04 per Orbit, p<0,05 per Cosmic).
- Se i dati finali saranno positivi, l’obiettivo dichiarato è andare verso filing regolatori in USA ed Europa, con Ultragenyx leader globale e Mereo titolare dei diritti commerciali in Europa.
Executive summary
Oggi Mereo BioPharma è, di fatto, una scommessa concentrata su setrusumab (UX143), anticorpo anti-sclerostina in partnership con Ultragenyx per l’osteogenesi imperfetta, con un secondo asse su alvelestat per la malattia polmonare da deficit di alfa-1 antitripsina (AATD-LD) e un asset osseo in partnership (vantictumab) per una forma rara di osteopetrosi (ADO2).
Nel 2025 la narrativa è dominata dagli studi Fase 3 Orbit e Cosmic in OI: pienamente arruolati, in rotta verso analisi finali a fine anno e descritti dal management come evento “trasformativo” per la storia aziendale. La seconda interim di metà anno non ha permesso uno stop anticipato per efficacia e ha fatto crollare il titolo, ma non ha evidenziato problemi di safety e i trial procedono.
Sul fronte numerico, Mereo è una small-cap pre-commerciale: nessun ricavo di prodotto, cassa intorno ai 48,7 milioni di dollari a fine Q3 2025 e guidance di runway fino al 2027, grazie a un profilo di spesa relativamente contenuto. La struttura di debito è limitata: il rischio principale non è tanto finanziario immediato, quanto legato all’esito dei trial.
In questo report guardiamo a: (1) disegno, obiettivi e tempistiche di Orbit/Cosmic; (2) posizione strategica e finanziaria di Mereo in vista dei dati; (3) stato di alvelestat e di vantictumab; (4) mappa scenari e rischi, senza sovrainterpretare i movimenti di borsa di breve.
Panoramica aziendale
Mereo BioPharma oggi è una clinical-stage biotech focalizzata sulle malattie rare. Dopo anni di portfolio più ampio (oncologia, endocrino) e varie razionalizzazioni, la struttura attuale ruota attorno a due candidati: setrusumab per l’osteogenesi imperfetta e alvelestat per la malattia polmonare da AATD-LD. A questi si aggiunge vantictumab, asset osseo in licenza ad āshibio per l’osteopetrosi autosomica dominante di tipo 2, con Mereo che mantiene i diritti commerciali in Europa.
La strategia dichiarata è chiara: usare la partnership con Ultragenyx per spingere setrusumab globalmente, mantenendo però una fetta importante di valore in Europa, e contemporaneamente trovare un partner forte per alvelestat, ora supportato da designazioni orfane in USA e EU. In pratica, Mereo punta a diventare un player di nicchia nelle malattie rare di osso e polmone, più che una piattaforma generalista.
Pipeline: setrusumab, alvelestat, vantictumab
| Programma | Indicazione | Partner / area | Stadio |
|---|---|---|---|
| Setrusumab (UX143) | Osteogenesi imperfetta (OI) | Ultragenyx guida globale; Mereo mantiene diritti UE | Fase 3 Orbit (pazienti 5–25 anni) e Cosmic (2–<7 anni), verso analisi finali a fine 2025 dopo almeno 18 mesi di trattamento. |
| Alvelestat | Malattia polmonare grave da AATD-LD | Mereo (in cerca di partner per Fase 3 e commercializzazione) | Dati di Fase 2; programma “Phase 3 ready”; Orphan e Fast Track negli USA; opinione positiva per designazione orfana in UE. |
| Vantictumab | Osteopetrosi autosomica dominante tipo 2 (ADO2) | Licenza ad āshibio; diritti commerciali UE in mano a Mereo | Programma osseo in fase precoce, con dati preclinici incoraggianti presentati ad ASBMR 2025. |
I vecchi asset oncologici o endocrini oggi pesano poco nella tesi: la maggior parte del valore percepito è legato alla capacità di setrusumab di dimostrare un beneficio convincente su fratture e qualità di vita nell’OI, e alla possibilità che alvelestat trovi un partner forte e un percorso credibile verso la Fase 3.
Catalyst e tempistiche (2025 – 2027)
Q1 2025
Guidance su Orbit IA2 e status alvelestat
Mereo ribadisce che Orbit può leggere o alla seconda interim di metà 2025 oppure all’analisi finale nel Q4; al tempo stesso annuncia l’opinione positiva del COMP per la designazione orfana di alvelestat in Europa e la prosecuzione dei lavori di preparazione Fase 3.
Luglio 2025
Seconda interim Orbit: stop anticipato mancato
L’interim IA2 non supera la soglia per una chiusura anticipata per efficacia; il DMC raccomanda di proseguire fino all’analisi finale con un profilo di safety coerente con gli studi precedenti. Il mercato reagisce male, con un repricing pesante di MREO e RARE, ma il programma resta intatto dal punto di vista regolatorio.
Q2–Q3 2025
Aggiornamenti trimestrali: dati year-end, runway
Nei comunicati Q2 e Q3 l’azienda conferma l’attesa di dati finali da Orbit e Cosmic attorno a fine 2025, segnala cassa in calo ma ancora sufficiente a sostenere le operazioni fino al 2027 e comunica l’accordo vantictumab–āshibio, con mantenimento dei diritti UE in una seconda malattia rara dell’osso.
Fine 2025 / inizio 2026
Analisi finali Orbit e Cosmic
I risultati finali dovranno mostrare una riduzione significativa delle fratture in Orbit rispetto al controllo e un vantaggio chiaro in Cosmic rispetto ai bisfosfonati IV. Saranno questi numeri, non il rumore sui prezzi, a decidere quanto setrusumab potrà aspirare allo status di standard-of-care in OI.
2026–2027
Percorso regolatorio e possibile lancio UE
In caso di successo, l’obiettivo dichiarato è andare verso filing in USA ed Europa e preparare un lancio mirato, con Mereo che punta a capitalizzare sui diritti UE e sui rapporti in costruzione con i centri specializzati OI.
Situazione finanziaria e posizione di capitale
Nel Q3 2025 Mereo ha riportato circa 48,7 milioni di dollari di cassa e equivalenti e ha confermato una runway stimata fino al 2027, assumendo una gestione prudente della spesa. La perdita netta trimestrale è intorno ai 7 milioni, in calo rispetto all’anno precedente, grazie a costi più contenuti e a effetti di cambio favorevoli.
Non ci sono ricavi di prodotto e i ricavi totali sono sostanzialmente nulli; il modello è quello classico di una biotech in Fase 3 finanziata da equity, con debito tradizionale limitato. Questo riduce il rischio di carico interessi ma lascia aperta la questione di come finanziare eventuali fasi successive (commercializzazione autonoma, ulteriori trial) se i dati saranno positivi.
In sintesi: i soldi per vedere i dati ci sono; i soldi per costruire un’eventuale macchina commerciale su larga scala dipenderanno dall’esito di setrusumab, dai termini di Ultragenyx e dal successo nel trovare partner per alvelestat.
Sentiment: analisti e retail
Sentiment – trader non professionisti
Dopo lo shock di luglio, diversi analisti hanno definito la reazione del mercato eccessiva, sottolineando che l’assenza di stop anticipato non equivale a fallimento e che la soglia per l’analisi finale è più bassa. In più di un report MREO viene indicata come “leva concentrata” sui dati finali OI, con rating positivi ma grande enfasi sul rischio binario.
Nei commenti retail MREO viene spesso trattata come una storia evento-driven: c’è chi la vede come opportunità asimmetrica se i dati finali confermeranno il potenziale di riduzione fratture visto in studi precedenti, e chi la considera troppo rischiosa per via del cash limitato e della dipendenza da una singola serie di trial.
Come sempre, il sentiment è utile per capire quanto è affollato il trade, non per sostituire una valutazione autonoma. I numeri li fanno i trial, non i commenti su X o Stocktwits.
Mappa scenari: cosa può andare bene o male
Scenario positivo (concettuale, non una previsione)
Nello scenario favorevole, Orbit e Cosmic mostrano riduzioni nette e convincenti nel tasso di fratture, con safety accettabile. Le agenzie regolatorie accettano il pacchetto dati e si va verso approvazioni in USA/UE. Ultragenyx spinge forte su OI, Mereo capitalizza sui diritti UE e alvelestat trova un partner disposto a finanziare una Fase 3 robusta.
Scenario intermedio
In uno scenario medio, i dati sono positivi ma non clamorosi: si supera la soglia statistica, ma con effetti meno “puliti” di quanto si sperava. Il farmaco arriva comunque a filing/approvazione, ma la penetrazione è più lenta e condizionata da payor, concorrenza e fiducia degli specialisti. Mereo beneficia, ma con un profilo di rischio/rendimento meno spettacolare.
Scenario downside
Nello scenario negativo, i dati finali non raggiungono gli endpoint oppure li centrano in modo tale da lasciare molti dubbi sulla rilevanza clinica. In quel caso il valore della storia OI si ridimensiona fortemente, Mereo resta con un asset polmonare ancora da sviluppare e una cassa che, pur non azzerata, non è infinita. Il repricing del titolo in questo scenario potrebbe essere severo, ed è il motivo per cui molti considerano MREO una scommessa ad alto beta.
Mappa rischi
Rischio clinico/regolatorio
Setrusumab è ancora in Fase 3; gli endpoint sono complessi e basati su fratture, variabili per natura. Esiti negativi o “grigi” possono azzerare gran parte del valore atteso sull’OI.
Rischio di finanziamento/diluizione
Con cassa sotto i 50 milioni, Mereo può arrivare ai dati ma difficilmente potrà permettersi di finanziare da sola un lancio globale o più programmi avanzati senza ulteriori capitali. Il rischio di nuove emissioni resta quindi non trascurabile.
Dipendenza dai partner
Molto del valore di setrusumab dipende da Ultragenyx: priorità interne, pricing, strategia sull’OI. Qualsiasi cambio di focus o di appetite da parte del partner può impattare la traiettoria di Mereo anche in presenza di dati positivi.
In sintesi
Mereo BioPharma è una storia concentrata ma interessante: un programma OI avanzato con un partner forte, un asset respiratorio Fase 3–ready con status orfano, un asset osseo aggiuntivo in licenza e una struttura di costi relativamente sotto controllo. Tutto, però, ruota intorno ai dati finali di setrusumab.
Finché quei numeri non saranno sul tavolo, MREO resterà un titolo ad alto beta dove sentiment e aspettative possono cambiare in fretta. Questo testo non ti dice se il titolo “merita” o meno di salire o scendere: mette solo in fila dati, contesto e punti di attenzione per permettere a chi legge di ragionare con la propria testa.
Fonti principali
- Comunicati Mereo BioPharma su risultati finanziari Q1, Q2 e Q3 2025 e aggiornamenti corporate (setrusumab Orbit/Cosmic, alvelestat, accordo con āshibio su vantictumab).
- Comunicati Ultragenyx su UX143 (setrusumab), inclusi quelli relativi all’interim di Orbit e alla prosecuzione degli studi fino all’analisi finale.
- Aggiornamento 2025 sui programmi principali e risultati FY2024 di Mereo (tempistiche IA2 / analisi finale, design OI e status regolatorio di alvelestat).
- Articoli di testate primarie (Barron’s, Investors Business Daily, ecc.) sulla reazione di mercato all’interim Orbit e sulle aspettative per i dati finali.
- Analisi di terzi (es. broker, siti finanziari) che discutono range di prezzo, runway, posizione di cassa e struttura di rischio per MREO.
Alcuni link esterni utilizzati per grafici o strumenti (Finviz, Seeking Alpha, Stocktwits, piattaforme di brokeraggio) possono includere parametri di referral affiliati a Merlintrader. Questo non modifica il contenuto che vedi né il prezzo dei servizi e non influenza le conclusioni dell’analisi.
Disclaimer legale e di rischio
Contenuto puramente informativo, non è una raccomandazione. Questo testo si basa su informazioni pubbliche disponibili al momento della stesura (filings, documenti regolatori, comunicati ufficiali, media di primaria affidabilità) e può contenere errori, omissioni o dati nel frattempo superati.
Nulla di quanto scritto costituisce invito o sollecitazione ad acquistare, vendere o detenere strumenti finanziari, né consulenza personalizzata. L’autore non è un consulente finanziario abilitato. Eventuali riferimenti a scenari, upside/downside o dinamiche di mercato sono esempi concettuali, non previsioni.
Chi legge deve svolgere la propria due diligence, valutare il proprio profilo di rischio e, se necessario, confrontarsi con un professionista abilitato. Le biotech rare-disease con un singolo programma avanzato sono intrinsecamente rischiose e possono portare a perdite significative di capitale.
Questo report è pensato per un pubblico internazionale (UE e USA) e utilizza un linguaggio coerente con lo spirito delle linee guida CONSOB e SEC per commenti informativi non-promozionali.
Authors: Merlintrader and Jane.
Per note legali e privacy complete:
Disclaimer
Termini di Servizio, Privacy, Cookie Policy // Term of Service, Privacy, Cookie Policy
Biotech Catalyst Calendar
Per una panoramica aggiornata di PDUFA, letture di dati clinici e altri eventi chiave su biotech e healthcare, puoi fare riferimento alla pagina dedicata del Biotech Catalyst Calendar di Merlintrader.
Link diretto: https://merlintrader.com/calendario-catalyst/
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


