DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
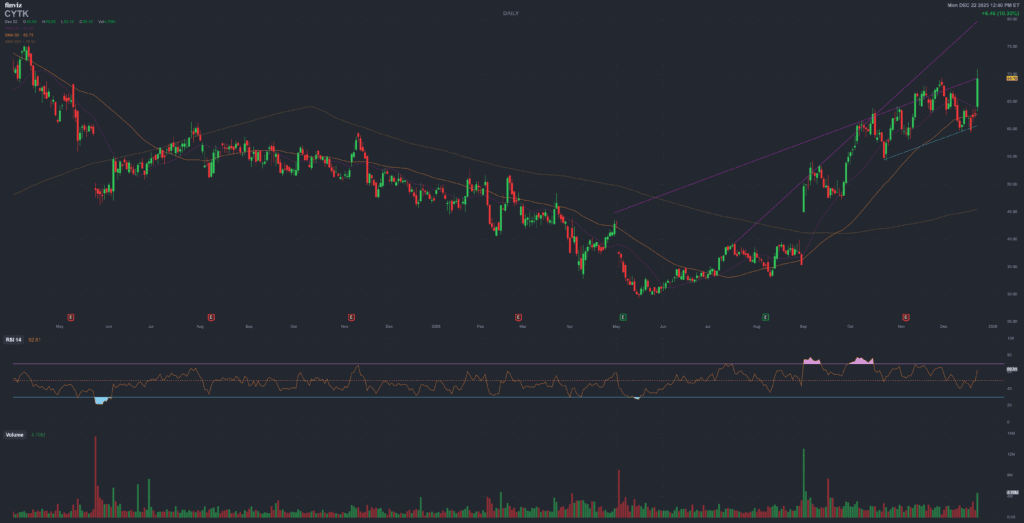
Cytokinetics (CYTK) – MYQORZO, obstructive HCM and the specialty cardiology franchise
Long-form, filings-based deep dive on Cytokinetics at the moment of its first FDA approval: MYQORZO (aficamten) for obstructive HCM, the follow-on trials in nHCM and HFpEF, and how the balance sheet is being re-wired around a specialty cardiology plan.
CYTK
Nasdaq | Cytokinetics, Incorporated
News of the day – 22 Dec 2025
FDA approves MYQORZO (aficamten) – first product on the market for Cytokinetics
On December 19, 2025, the US FDA approved MYQORZO (aficamten) for adults with symptomatic obstructive hypertrophic cardiomyopathy (oHCM), to improve functional capacity and symptoms.
- MYQORZO is an oral cardiac myosin inhibitor and becomes Cytokinetics’ first approved drug and only the second therapy in class after Camzyos (Bristol Myers Squibb).
- In SEQUOIA-HCM, aficamten significantly improved peak VO2 and symptoms in obstructive HCM; in a head-to-head trial versus metoprolol it also showed superior gains in exercise capacity and Kansas City Cardiomyopathy Questionnaire (KCCQ) scores.
- The FDA label includes a REMS program because of heart failure risk, but analysts note MYQORZO’s shorter half-life and simpler monitoring requirements compared with Camzyos, a key point for real-world adoption.
Executive summary
Cytokinetics enters 2026 in a very different position from just a year ago. After years as a development-stage muscle biology company – including the high-profile failure of omecamtiv mecarbil in chronic heart failure – the company now has its first approved product: MYQORZO (aficamten) for symptomatic obstructive HCM.
The immediate investment case is dominated by three moving pieces: (1) the quality of the US MYQORZO launch and how quickly referral patterns and monitoring logistics can support real-world uptake; (2) the global regulatory path (China already approved, EU decision pending) and label dynamics; and (3) the broader myosin-directed pipeline, which extends aficamten into non-obstructive HCM and pediatric oHCM while pushing CK-586 into HFpEF and omecamtiv mecarbil into COMET-HF for severely reduced EF heart failure.
Financially, Q3 2025 shows a company with ~USD 1.25B in cash, cash equivalents and investments, a substantial operating loss, and a capital structure built on convertibles and royalty-style financings, leading to an accounting stockholders’ deficit despite a multi-billion market cap.
This report focuses on: (1) the MYQORZO approval and label; (2) the structure of the specialty cardiology franchise across oHCM, nHCM, HFpEF and HFrEF; (3) the balance sheet and cash runway; (4) analyst and retail sentiment around CYTK; and (5) a scenario map that frames upside, execution paths and key risks without trying to guess the share price.
Company overview
Cytokinetics describes itself as a specialty cardiovascular biopharmaceutical company focused on diseases of cardiac muscle dysfunction, building on more than 25 years of muscle biology work. The historic arc runs from early sarcomere activators (omecamtiv mecarbil) to today’s myosin inhibitors (aficamten and CK-586) and skeletal muscle activators such as CK-089.
The strategic idea is to build a focused cardiology franchise in indications that share a few features: high unmet need, concentrated specialist prescribers, payers who manage to label, and a manageable number of centers (HCM, severely reduced-EF heart failure, a hypercontractile subset of HFpEF). Corporate decks explicitly show aficamten as the “anchor” of this franchise, with additional indications and molecules radiating out over the next five to ten years.
MYQORZO’s approval turns this from a purely aspirational slide into an operational reality: there is now a real product, a REMS, a sales force, and near-term revenue. The rest of the pipeline – ACACIA-HCM, AMBER-HFpEF, COMET-HF and CK-089 – will either reinforce or undermine that strategic ambition over the next cycle.
Key programs and pipeline structure
| Program | Target / modality | Indication(s) | Stage |
|---|---|---|---|
| MYQORZO (aficamten) | Cardiac myosin inhibitor (oral) | Symptomatic obstructive HCM (NYHA II–III) | Approved in US and China; positive CHMP opinion in EU (EC decision expected 1Q 2026) |
| ACACIA-HCM | Aficamten | Symptomatic non-obstructive HCM (nHCM) | Phase 3, enrolling |
| CEDAR-HCM / FOREST-HCM | Aficamten | Pediatric oHCM; long-term extension in HCM | Pediatric oHCM and open-label extension ongoing |
| CK-586 (AMBER-HFpEF) | Cardiac myosin inhibitor | HFpEF with supranormal EF and hypercontractility | Phase 2, 60 patients in dose-finding trial |
| Omecamtiv mecarbil (COMET-HF) | Cardiac myosin activator | Symptomatic HFrEF with severely reduced EF | Phase 3, multinational trial evaluating CV events and transplant risk |
| CK-089 | Fast skeletal muscle troponin activator | Specific muscular dystrophy and other skeletal muscle conditions | Preclinical / early-stage |
Importantly, all programs beyond MYQORZO are still investigational. Company disclosures repeatedly stress that aficamten, omecamtiv mecarbil, CK-586 and CK-089 have not yet been determined safe or effective for any indication outside the newly-approved oHCM label.
Catalyst and timeline overview (late 2025 – 2028)
Dec 19, 2025
US approval – MYQORZO for oHCM
FDA approves MYQORZO (aficamten) for adults with symptomatic obstructive HCM, marking Cytokinetics’ first commercial product and the second approved myosin inhibitor for this disease. Launch expected in the US in January under a REMS program.
4Q 2025 – 1Q 2026
Ex-US decisions (EU, China)
MYQORZO is already approved by the NMPA in China and carries a positive CHMP opinion in Europe; the European Commission is expected to decide in the first quarter of 2026. The pace of reimbursement and center activation in Europe will matter for the medium-term revenue curve.
2026–2027
Aficamten life-cycle: monotherapy and nHCM
ACACIA-HCM is expected to deliver key readouts in non-obstructive HCM, while further data from CEDAR-HCM and MAPLE-HCM (oHCM monotherapy) should inform label expansion and how far aficamten can move away from combination therapy and invasive procedures.
2026–2028
HFpEF and HFrEF programs
AMBER-HFpEF will generate dose-finding and safety data for CK-586 in patients with hypercontractile HFpEF, building on aficamten nHCM data. In parallel, COMET-HF will test whether omecamtiv mecarbil can reduce hard heart failure events in severely reduced EF patients, a higher-risk but potentially large opportunity.
2026–2028+
Franchise consolidation
Corporate roadmaps show a multi-year build-out where MYQORZO anchors the specialty cardiology franchise, with successive indications (nHCM, HFpEF, HFrEF) potentially expanding the addressable population from tens of thousands to hundreds of thousands of patients worldwide – assuming trials succeed and payers accept pricing.
Financial snapshot and capital structure
As of 30 September 2025, Cytokinetics reported total assets of about USD 1.44B and total liabilities close to USD 1.96B, leading to an accounting stockholders’ deficit of roughly USD 521M. This reflects the cumulative losses of a long development history plus layers of term loans, royalty participation agreements and convertible notes.
Cash, cash equivalents and investments stood around USD 1.25B at quarter-end, bolstered by a USD 750M convertible note offering and additional Royalty Pharma funding earlier in the year. Revenues for the first nine months of 2025 were about USD 70M (primarily license and milestone payments), versus operating expenses above USD 504M, driven by R&D and growing commercial readiness costs. Net loss over the period was roughly USD 602M.
The company’s own guidance points to full-year 2025 GAAP operating expenses of USD 680–700M, with a significant portion being non-cash stock-based compensation. At face value, the liquidity profile suggests more than a year of runway even at elevated spending levels, but “runway” is now less relevant than the speed and quality of the MYQORZO commercialization – which will eventually need to carry a meaningful share of that cost base for the model to be sustainable.
In practical terms: Cytokinetics has cash to execute, but the balance sheet comes with embedded leverage and revenue participation. The more MYQORZO (and future products) sell, the more those structures matter for how much economic value actually accrues to common equity.
Sentiment: analysts and retail
Sentiment – non-professional traders
Analyst commentary after the MYQORZO approval has generally framed the decision as a clear win: first product approval, a relatively clean oHCM label and the perception of a safer, more convenient profile vs Camzyos (shorter half-life, simpler monitoring, fewer interaction issues). Several sell-side notes now focus on peak sales scenarios in the USD 1–2B range over the next decade, while also highlighting the very large spend required to build a commercial infrastructure from scratch.
Earlier in 2025, the failure of Bristol Myers’ Camzyos in non-obstructive HCM temporarily weighed on CYTK, but some analysts argued that aficamten’s profile and trial design still leave room for success in nHCM – with the added twist that reduced competition in that niche could be a long-term positive if ACACIA-HCM works.
On Stocktwits, Reddit and X, CYTK is now firmly in the “crowded cardiology” bucket: plenty of bulls posting cardiology slides, TAM charts and comparisons to Camzyos; plenty of bears pushing back on valuation, debt structure and the risk of a slow launch. The tone is less meme-like than small-cap biotech: many posts come from people who clearly follow HCM and HF as themes, but the usual momentum traders are present as well, especially after the double-digit rally on approval day.
This sentiment section is based on public comments from non-professional traders on Reddit, Stocktwits and X, combined with published analyst notes. None of these views should be treated as investment advice or as a substitute for independent due diligence.
Scenario map: what could go right or wrong
Upside scenario (conceptual, not a prediction)
In a constructive world, MYQORZO establishes itself as the preferred myosin inhibitor in obstructive HCM thanks to a practical label, robust exercise capacity data and a REMS that proves manageable in the real world. Ex-US approvals (EU, China, other regions) follow broadly in line with expectations, building a multi-region revenue base over 2026–2028.
ACACIA-HCM succeeds in nHCM, demonstrating that aficamten can improve functional measures and quality of life where Camzyos failed, and AMBER-HFpEF identifies a subset of HFpEF patients where CK-586 can meaningfully change symptoms and biomarkers. COMET-HF delivers a positive signal in severely reduced EF heart failure, opening another high-need segment. In that environment, Cytokinetics looks less like a “one-drug story” and more like a multi-asset specialty cardiology platform.
Execution / middle path
A more neutral – and arguably more realistic – path has MYQORZO ramping, but with the usual friction: center capacity limits, REMS learning curve, payer negotiation, and cautious cardiologists who have lived through other launch disappointments. Aficamten’s follow-on trials progress, but ACACIA-HCM and AMBER-HFpEF take longer than hoped to deliver clean answers. COMET-HF may show mixed results, keeping the heart failure opportunity in play but not fully de-risked.
Downside / risk-intensive scenario
On the downside, several things could converge: slower-than-expected MYQORZO uptake, pushback on pricing or REMS logistics, or safety signals emerging in broader use or in related myosin-inhibitor programs. ACACIA-HCM might replicate the disappointing nHCM experience seen with Camzyos, undermining the multi-indication story, while HFpEF and HFrEF trials fail to generate compelling data. In that world, the combination of high operating expense, leverage and modest revenue growth would put real pressure on the equity case.
None of these scenarios are forecasts. They are simply a structured way to think about where most of the risk actually sits: not in whether MYQORZO is technically approved (it now is), but in how fast the franchise scales and how many of the follow-on bets actually pay off.
Risk map
Regulatory / safety
Myosin modulation is powerful biology. Long-term safety in broader oHCM use, as well as in nHCM, HFpEF and HFrEF, remains to be demonstrated. Any meaningful safety signal (heart failure events, arrhythmias, off-target effects) could trigger tighter labels or slow adoption across the class.
Commercial execution
Success depends on referral networks, echocardiography capacity, REMS compliance and payer agreements. If centers are slow to adopt MYQORZO, or if payers steer patients to cheaper options or invasive procedures, the revenue curve could lag even with good clinical data.
Capital structure & dilution
Cytokinetics carries significant debt and revenue participation obligations. If launch metrics disappoint, the combination of high burn and leverage could eventually force further equity issuance or renegotiation, diluting existing shareholders.
Bottom line
With MYQORZO now approved, Cytokinetics has crossed the line from “development-stage story” to active commercial player in a tightly-defined but meaningful cardiology niche. The data supporting approval are real, the unmet need in oHCM is not in dispute, and the company has spent years preparing the infrastructure to launch.
At the same time, the stock remains high-beta by nature: the balance sheet is leveraged, operating spend is heavy, and the valuation already bakes in a substantial amount of future execution. Whether CYTK ultimately belongs in the “great specialty franchises” or “over-extended launch stories” bucket is precisely what the next few years of data, prescriptions and financials will decide.
This text is not a recommendation to buy or sell CYTK. It is a map of the current facts and moving parts so that traders and investors can decide for themselves how – or whether – this name fits their own approach, time horizon and risk tolerance.
Key sources and links
- Cytokinetics – FDA approval press release for MYQORZO (aficamten) in symptomatic oHCM, December 2025.
- Cytokinetics – Q3 2025 financial results and business update (cash position, debt and participation structures, operating expense guidance).
- Corporate presentations and trial-specific websites for ACACIA-HCM, AMBER-HFpEF and COMET-HF (clinical design, endpoints, target populations).
- Peer-reviewed publications and NEJM/Eur Heart Journal papers on aficamten and SEQUOIA-HCM exercise capacity and symptom outcomes.
- Reuters, Investors Business Daily and other major outlets on MYQORZO approval, label comparison vs Camzyos and early analyst expectations.
Some external links used for charts or tools (for example Finviz, Seeking Alpha, Stocktwits or broker platforms) may include affiliate or referral parameters for Merlintrader. These do not change the content you see or the price you pay, and they do not influence the conclusions of this analysis.
Legal and risk disclaimer
Informational only, not investment advice. This report is based on public information from company filings, regulatory documents and reputable news sources available at the time of writing. It may contain errors, omissions or data that become outdated as new information emerges.
Nothing in this text is a recommendation to buy, sell or hold any security, nor a solicitation to do so. The author is not a registered investment adviser or a licensed financial professional. Any references to scenarios, upside/downside or potential market behaviour are illustrative and not predictions.
Readers should perform their own due diligence, consider their personal financial situation and risk tolerance, and, where appropriate, consult a qualified financial professional. Cardiovascular drug development carries significant scientific, regulatory and commercial uncertainty. It is possible to lose some or all of the capital invested.
This content is intended for an international audience that includes readers in both the European Union and the United States. The language and structure aim to remain consistent with the spirit of applicable guidance from regulators such as CONSOB and the SEC for purely informational, non-promotional commentary.
Authors: Merlintrader and Jane.
For full legal notes and privacy information, please refer to:
Disclaimer
Termini di Servizio, Privacy, Cookie Policy // Term of Service, Privacy, Cookie Policy
Biotech Catalyst Calendar
For an updated overview of upcoming biotech and healthcare catalysts – PDUFA dates, clinical readouts, regulatory events – you can always refer to the dedicated Merlintrader Biotech Catalyst Calendar page.
Cytokinetics (CYTK) – MYQORZO, HCM ostruttiva e la franchise di cardiologia specialistica
Analisi estesa, basata su documenti ufficiali, su Cytokinetics nel momento della prima approvazione FDA: MYQORZO (aficamten) per HCM ostruttiva, i trial successivi in nHCM e HFpEF e come il bilancio si sta riallineando intorno a una strategia di cardiologia specialistica.
CYTK
Nasdaq | Cytokinetics, Incorporated
News del giorno – 22 dic 2025
Approvato MYQORZO (aficamten) – primo prodotto in commercio per Cytokinetics
Il 19 dicembre 2025 la FDA ha approvato MYQORZO (aficamten) per il trattamento di adulti con cardiomiopatia ipertrofica ostruttiva sintomatica (oHCM), con indicazione a migliorare capacità funzionale e sintomi.
- MYQORZO è un inibitore orale della miosina cardiaca: è il primo prodotto mai approvato per Cytokinetics e solo il secondo farmaco della classe dopo Camzyos di Bristol Myers.
- Nel trial pivotale SEQUOIA-HCM aficamten ha migliorato in modo significativo la capacità di esercizio (peak VO2) e i sintomi rispetto a placebo; in uno studio testa-a-testa contro metoprololo ha mostrato benefici superiori su capacità di esercizio e KCCQ.
- L’etichetta prevede un programma REMS per il rischio di scompenso, ma diversi analisti sottolineano emivita più breve e schema di monitoraggio meno complesso rispetto a Camzyos, aspetto chiave per l’adozione pratica.
Executive summary
Cytokinetics entra nel 2026 in una posizione molto diversa rispetto a un anno fa. Dopo anni da biotech pre-commerciale focalizzata sulla biologia del muscolo – con in mezzo il caso sfortunato di omecamtiv mecarbil nello scompenso cronico – l’azienda ha ora il suo primo farmaco approvato: MYQORZO (aficamten) per HCM ostruttiva sintomatica.
La tesi di breve/medio periodo ruota soprattutto su tre blocchi: (1) qualità e velocità del lancio USA di MYQORZO e capacità della rete di centri/REMS di supportare l’adozione reale; (2) percorso regolatorio globale (Cina già approvata, UE in arrivo) e dinamica dell’etichetta; (3) pipeline più ampia di farmaci diretti alla miosina, che estende aficamten alla nHCM e ai pazienti pediatrici, porta CK-586 in HFpEF e omecamtiv mecarbil nel trial COMET-HF per HFrEF severo.
A livello finanziario, il Q3 2025 mostra circa 1,25 miliardi di dollari fra cassa ed investimenti, una perdita significativa e una struttura di capitale fatta di prestiti, note convertibili e accordi su royalty che portano a un deficit di patrimonio netto contabilizzato, pur in presenza di una capitalizzazione di mercato di diversi miliardi.
In questo report ci concentriamo su: (1) approvazione e label di MYQORZO; (2) struttura della franchise di cardiologia specialistica tra oHCM, nHCM, HFpEF e HFrEF; (3) profilo finanziario e struttura del capitale; (4) sentiment di analisti e retail; (5) mappa scenari e principali rischi, senza pretendere di “indovinare” il prezzo del titolo.
Panoramica aziendale
Cytokinetics si definisce una biopharma di cardiologia specialistica, focalizzata sulle malattie da disfunzione del muscolo cardiaco, con oltre 25 anni di lavoro sulla biologia del muscolo. L’arco storico va dagli attivatori del sarcomero (omecamtiv mecarbil) agli inibitori di miosina di nuova generazione (aficamten, CK-586) e agli attivatori del muscolo scheletrico come CK-089.
L’idea strategica è costruire una franchise di cardiologia specializzata in indicazioni con poche terapie, alta unmet need e un numero relativamente concentrato di centri e prescrittori (HCM, HFrEF severa, sottogruppi di HFpEF). Le presentazioni aziendali mostrano chiaramente aficamten come “ancora” del modello, con indicazioni addizionali e nuove molecole che si aggiungono nel corso dei prossimi anni.
L’approvazione di MYQORZO rende questo schema concreto: da ora non stiamo più parlando solo di slide, ma di pazienti in trattamento, REMS attivo, forza vendita e primi ricavi ricorrenti. Il modo in cui ACACIA-HCM, AMBER-HFpEF, COMET-HF e CK-089 si comporteranno determinerà quanto questa franchise potrà diventare davvero “multi-asset”.
Pipeline e programmi principali
| Programma | Target / modalità | Indicazioni | Stadio |
|---|---|---|---|
| MYQORZO (aficamten) | Inibitore di miosina cardiaca (orale) | HCM ostruttiva sintomatica negli adulti | Approvato in USA e Cina; parere CHMP positivo in UE (decisione attesa 1Q 2026) |
| ACACIA-HCM | Aficamten | HCM non ostruttiva sintomatica (nHCM) | Phase 3, arruolamento in corso |
| CEDAR-HCM / FOREST-HCM | Aficamten | oHCM pediatrica; estensione open-label in HCM | Studi in corso |
| CK-586 (AMBER-HFpEF) | Inibitore di miosina cardiaca | HFpEF con EF supranormale e ipercontrattilità | Phase 2, studio dose-finding ~60 pazienti |
| Omecamtiv mecarbil (COMET-HF) | Attivatore di miosina cardiaca | HFrEF con frazione di eiezione severamente ridotta | Phase 3, endpoint su eventi di scompenso e trapianto |
| CK-089 | Attivatore troponina muscolo scheletrico | Alcune forme di distrofia muscolare e debolezza muscolare | Preclinico / early stage |
Tutti i programmi oltre MYQORZO restano comunque sperimentali. Nei documenti ufficiali l’azienda ribadisce che aficamten fuori dall’indicazione approvata, omecamtiv mecarbil, CK-586 e CK-089 non sono ancora stati giudicati sicuri o efficaci da FDA o altre agenzie.
Catalyst e tempistiche (fine 2025 – 2028)
19 dic 2025
Approvazione FDA – MYQORZO per oHCM
La FDA approva MYQORZO (aficamten) per adulti con HCM ostruttiva sintomatica: primo prodotto in assoluto per Cytokinetics e secondo inibitore di miosina in classe. Lancio USA previsto a gennaio, con schema REMS per mitigare il rischio di scompenso.
4Q 2025 – 1Q 2026
Decisioni ex-USA (UE, Cina)
MYQORZO è già approvato dall’NMPA in Cina e ha ricevuto parere positivo dal CHMP in Europa; la decisione della Commissione UE è attesa nel primo trimestre 2026. La velocità con cui rimborsi e centri si allineeranno in UE peserà molto sul profilo di ricavi 2026–2028.
2026–2027
Ciclo di vita aficamten
ACACIA-HCM dovrebbe fornire le letture chiave nella nHCM, mentre CEDAR-HCM e MAPLE-HCM (monoterapia oHCM) delineeranno se aficamten può espandersi oltre lo scenario combinazione/centro ultra-specializzato verso usi più larghi ma sempre controllati.
2026–2028
HFpEF e HFrEF
AMBER-HFpEF genererà dati di dose e sicurezza per CK-586 in un sottogruppo HFpEF ipercontrattile, partendo dall’esperienza nHCM con aficamten. In parallelo COMET-HF verificherà se omecamtiv mecarbil può ridurre eventi duri di scompenso e trapianto in pazienti con HFrEF severa.
2026–2028+
Consolidamento della franchise
Nelle slide aziendali, MYQORZO è il perno di una franchise che, se i trial andranno bene, potrebbe estendersi a nHCM, HFpEF e HFrEF, ampliando la popolazione potenziale da decine di migliaia a qualche centinaio di migliaia di pazienti a livello globale, ovviamente subordinata a successo clinico e accettazione di prezzo da parte dei payor.
Situazione finanziaria e struttura del capitale
Al 30 settembre 2025 Cytokinetics riportava un attivo totale di circa 1,44 miliardi di dollari e passività per circa 1,96 miliardi, con un deficit di patrimonio netto intorno a 521 milioni. Questo riflette anni di perdite cumulative più una serie di prestiti, note convertibili e accordi di revenue participation.
La cassa complessiva (cassa, equivalenti e investimenti) era circa 1,25 miliardi, rafforzata da una emissione di note convertibili da 750 milioni e da nuove tranche Royalty Pharma nel 2025. I ricavi 9M 2025 sono circa 70 milioni di dollari, principalmente da upfront/milestone, a fronte di oltre 504 milioni di spese operative; la perdita netta dei primi nove mesi è circa 602 milioni.
La guidance 2025 indica spese operative GAAP fra 680 e 700 milioni di dollari, con una quota rilevante di stock-based compensation. A livelli così alti, la “runway” teorica in anni conta meno del ritmo con cui MYQORZO riuscirà a trasformare questa struttura di costi in un business con ricavi ricorrenti e margini sostenibili.
Tradotto: l’azienda ha benzina per correre, ma il serbatoio è legato a debito e accordi di revenue sharing. Più MYQORZO (e i futuri prodotti) venderanno, più diventerà importante capire quanto di quel fatturato resta davvero in tasca agli azionisti ordinari.
Sentiment: analisti e retail
Sentiment – trader non professionisti
Dopo l’approvazione di MYQORZO, molti analisti hanno definito la decisione un passaggio “transformational”: primo prodotto, label relativamente pulita e percezione di profilo più gestibile rispetto a Camzyos (washout più rapido, interazioni e teratogenicità meno problematiche). Diverse note ragionano ormai su scenari di picco vendite nell’ordine del miliardo abbondante, ma con forte enfasi sulla complessità di costruire una struttura commerciale da zero.
In primavera, il fallimento di Camzyos nella nHCM aveva pesato su CYTK, ma alcuni analisti hanno sottolineato che disegno e profilo di aficamten potrebbero ancora consentire un successo in quella popolazione, e che una minore concorrenza lì potrebbe rivelarsi un fattore positivo in caso di esito positivo di ACACIA-HCM.
Sul lato retail, CYTK è chiaramente un ticker “crowded”: molti post con slide su HCM, grafici di TAM e confronti con Camzyos; altri focalizzati su valuation tirata, struttura di debito e rischio di lancio lento. Il tono è più da “cardiology nerd” che da meme stock, ma la componente momentum non manca, soprattutto dopo il rally a doppia cifra post-FDA.
Il sentiment riassume opinioni pubbliche di trader non professionisti su Reddit, Stocktwits e X, integrate con alcuni report di analisti. Non va interpretato come suggerimento operativo né come sostituto di un’analisi indipendente.
Mappa scenari: cosa può andare bene o male
Scenario positivo (concettuale, non una previsione)
Nello scenario favorevole, MYQORZO si afferma come opzione preferita nei centri HCM per oHCM, con un’etichetta gestibile e dati solidi su capacità di esercizio e sintomi. Le decisioni ex-USA (UE, Cina, altri paesi) procedono senza intoppi e costruiscono una base di ricavi multi-regionale tra 2026 e 2028.
ACACIA-HCM ha successo nella nHCM, dimostrando che aficamten può dare risultati lì dove Camzyos non c’è riuscito, e AMBER-HFpEF identifica un sottogruppo HFpEF dove CK-586 produce miglioramenti clinicamente rilevanti. COMET-HF dà un segnale positivo nello HFrEF severo, aprendo un segmento aggiuntivo ad alta unmet need. In questo contesto, Cytokinetics somiglia sempre meno a una “single-asset story” e sempre più a una piattaforma di cardiologia specialistica.
Scenario di esecuzione intermedio
Uno scenario più neutro vede MYQORZO crescere, ma con ovvi attriti: centri lenti ad adeguarsi, REMS laborioso, payor prudente, cardiologi che vogliono dati e esperienza real-world prima di cambiare routine. I trial su nHCM e HFpEF proseguono ma con tempi dilatati e risultati più sfumati. COMET-HF offre magari un segnale parziale che mantiene la storia viva ma non completamente de-rischizzata.
Scenario negativo / ad alto rischio
Nello scenario pessimistico, il lancio di MYQORZO procede a rilento, tra resistenze di centri e payor, eventuali segnali di safety o dati meno brillanti nei registri real-world. ACACIA-HCM potrebbe non riuscire a differenziarsi dal quadro visto con Camzyos nella nHCM; AMBER-HFpEF e COMET-HF potrebbero dare risultati deboli o inconcludenti. Con burn elevato e struttura di debito già pesante, il rischio sarebbe di dover intervenire sul capitale in modo diluitivo in un contesto di sentiment più freddo sul settore.
Anche qui non si tratta di probabilità, ma del ventaglio di esiti possibili che un holder di CYTK deve tenere a mente: la variabile decisiva non è più “verrà approvato?”, ma “quanto velocemente e con quale ampiezza verrà davvero adottato MYQORZO, e quante delle scommesse successive funzioneranno?”.
Mappa rischi
Rischio regolatorio/sicurezza
Modulare la miosina è potente ma delicato. La safety di lungo periodo in oHCM, nHCM, HFpEF e HFrEF va ancora dimostrata. Qualsiasi segnale negativo potrebbe tradursi in label più restrittive o in una frenata nell’adozione di tutta la classe.
Esecuzione commerciale
La riuscita dipende da percorsi di invio, capacità di imaging, gestione REMS e negoziazioni con payor. Se questi pezzi non girano in modo coordinato, il profilo di ricavi può restare sotto le aspettative anche con buoni dati clinici.
Struttura del capitale e diluizione
Nota convertibile, term loan e accordi di revenue sharing rendono la struttura complessa. Con burn alto, un’eventuale delusione sul lancio o sui trial successivi potrebbe tradursi in nuova equity a sconto o in rinegoziazioni non favorevoli per gli azionisti esistenti.
In sintesi
Con MYQORZO approvato, Cytokinetics ha finalmente un prodotto reale sul mercato in una nicchia di cardiologia specialistica con bisogni significativi. I dati alla base dell’approvazione sono solidi e l’azienda ha lavorato a lungo per preparare la struttura commerciale.
Allo stesso tempo il titolo resta inevitabilmente ad alto beta: spesa operativa elevata, struttura di capitale complessa e una quota importante di valore già scontata nelle aspettative sugli anni a venire. Se CYTK finirà nel gruppo delle “franchise solide” o in quello delle “storie di lancio che non decollano” dipenderà da ciò che succederà nei prossimi 2–4 anni su ricavi, trial e percezione del rischio di classe.
Questo testo non è un invito a comprare o vendere CYTK, ma un tentativo di mettere in ordine i fatti rilevanti per chi vuole ragionare sulla storia con la propria testa.
Fonti principali
- Comunicato Cytokinetics sull’approvazione FDA di MYQORZO (aficamten) in oHCM, dicembre 2025.
- Cytokinetics – risultati finanziari Q3 2025 e business update (cassa, debito, guidance spese operative).
- Presentazioni corporate e siti trial dedicati per ACACIA-HCM, AMBER-HFpEF e COMET-HF (design clinico, endpoint, popolazioni target).
- Pubblicazioni peer-reviewed su aficamten e SEQUOIA-HCM (NEJM, Eur Heart Journal) con dati su peak VO2, sintomi e qualità di vita.
- Reuters, Investors Business Daily e altri media primari su approvazione MYQORZO, confronto con Camzyos e reazione del mercato.
Alcuni link esterni utilizzati per grafici o strumenti (Finviz, Seeking Alpha, Stocktwits, piattaforme di brokeraggio) possono includere parametri di referral affiliati a Merlintrader. Questo non modifica il contenuto che vedi né il prezzo dei servizi e non influenza le conclusioni dell’analisi.
Disclaimer legale e di rischio
Contenuto puramente informativo, non è una raccomandazione. Questo testo si basa su informazioni pubbliche disponibili al momento della stesura (filings, documenti regolatori, comunicati ufficiali, media di primaria affidabilità) e può contenere errori, omissioni o dati nel frattempo superati.
Nulla di quanto scritto costituisce invito o sollecitazione ad acquistare, vendere o detenere strumenti finanziari, né consulenza personalizzata. L’autore non è un consulente finanziario abilitato. Eventuali riferimenti a scenari, upside/downside o dinamiche di mercato sono solo esempi concettuali e non previsioni.
Chi legge deve svolgere la propria due diligence, valutare il proprio profilo di rischio e, se necessario, confrontarsi con un professionista abilitato. Le storie di cardiologia avanzata e, in particolare, i farmaci sul sarcomero comportano rischi elevati e la possibilità di perdere anche l’intero capitale investito.
Questo report è pensato per un pubblico internazionale (UE e USA) e utilizza un linguaggio coerente con lo spirito delle linee guida CONSOB e SEC per commenti informativi non-promozionali.
Authors: Merlintrader and Jane.
Per note legali e privacy complete:
Disclaimer
Termini di Servizio, Privacy, Cookie Policy // Term of Service, Privacy, Cookie Policy
Biotech Catalyst Calendar
Per una panoramica aggiornata di PDUFA, letture di dati clinici e altri eventi chiave su biotech e healthcare, puoi fare riferimento alla pagina dedicata del Biotech Catalyst Calendar di Merlintrader.
Link diretto: https://merlintrader.com/calendario-catalyst/
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


