DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
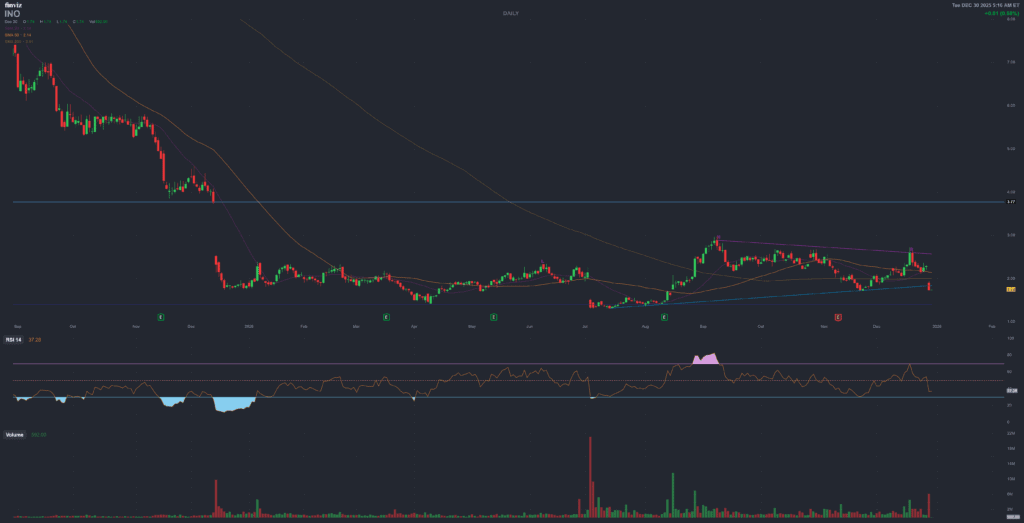
Inovio (INO) – INO-3107, RRP and the long road into the 2026 PDUFA
BLA acceptance for INO-3107 in Recurrent Respiratory Papillomatosis, Standard Review with October 30, 2026 PDUFA, long-term surgery-reduction data, repeated dilution and a fully binary risk profile for equity holders. Bilingual EN/IT switch below.
News of the day – December 29, 2025
FDA accepts INO-3107 BLA, Standard Review, PDUFA October 30, 2026
On December 29, 2025 the FDA accepted Inovio’s Biologics License Application for INO-3107 as a potential treatment for adults with Recurrent Respiratory Papillomatosis (RRP). The review classification is Standard and the agency set a PDUFA target action date of October 30, 2026. The FDA also indicated that it is currently not planning to hold an Advisory Committee for this dossier.
Inovio filed under the accelerated approval pathway, but in the file-acceptance letter the FDA flagged as a potential review issue its preliminary view that the company has not yet submitted adequate information to justify accelerated approval. Inovio still believes INO-3107 provides a meaningful benefit over surgery and plans to request a meeting with the agency to discuss how to remain eligible for the accelerated route. For now, the company explicitly says it is not preparing a traditional-pathway filing.
Equity market reaction was brutal: on the same day, INO shares dropped about 24% to 1.73 USD, with volume (about 6.1 million shares) far above the recent average, underscoring how central this BLA is to the entire equity story.
Takeaway: the regulatory clock is now visible (late-2026 PDUFA) but the FDA has already
signalled that accelerated approval is not guaranteed on the current data package.
Executive summary – why INO is so binary
Inovio today is essentially a single-asset equity story centred on INO-3107 in adult RRP. If approved, INO-3107 would be both Inovio’s first commercial product and the first DNA medicine approved in the United States, off a small but painful rare disease niche.
- Clinical data: in the Phase 1/2 trial (32 adults with frequent RRP surgeries), 72% of patients had a 50–100% reduction in the number of surgeries in the first year after treatment. A retrospective follow-up shows that this proportion increased to 86% in the second year, with the mean number of surgeries falling from 4.1 per year before treatment to 0.9 by Year 2 and half of patients requiring no surgeries at all.
- Regulatory setup: the BLA is in, with a fixed date (30 October 2026) but the FDA has already warned that current data may not fully support accelerated approval, adding a non-trivial layer of regulatory risk on top of the usual binary outcome.
- Balance sheet and dilution: cash, cash equivalents and short-term investments were about 50.8 million USD at 30 September 2025, with runway only into the second quarter of 2026, and no debt. Over the last few years the company has repeatedly resorted to sizeable equity raises (2021, April 2024, December 2024, July 2025, November 2025), almost always at a discount and often followed by double-digit share-price drops.
- Sentiment: RRP patients and clinicians are intrigued or cautiously optimistic; long-time retail holders in INO are much more divided, with visible frustration on Reddit and forums after years of dilution and negative performance.
- Analyst view: consensus rating around “Hold”, with a 12-month average target in the high-single-digits – implying large upside from current levels, but also embedding strong assumptions about regulatory success and a survivable capital-structure path to commercialisation.
Put bluntly: if INO-3107 fails or gets stuck in regulatory limbo, there is little else in the current setup that can support the equity in the near term.
Quick data panel (as of late December 2025)
Ticker / Exchange
INO – Nasdaq
Close 29 Dec 2025
1.73 USD (-24.45% on day)
52-week range
1.30 – 2.98 USD
Market cap
~155–160 M USD
Cash & ST inv. (30 Sep 2025)
50.8 M USD – no debt
Runway guidance
into 2Q 2026 (company estimate)
Consensus rating
Hold (5 Buy / 3 Hold / 1 Sell)
Avg. 12-m PT
≈ 9 USD (wide range 3–18)
First-in-class DNA medicine angle
Rare disease / small market
Heavy historical dilution
Short cash runway vs PDUFA date
Prices and valuation metrics here are indicative snapshots around 29 December 2025 and will move with the market. The purpose is to frame orders of magnitude, not to provide real-time data.
Company and DNA medicines platform
Inovio is a small biotechnology company focused on DNA medicines – plasmid-based constructs delivered with the proprietary CELLECTRA electroporation device. The idea is to let host cells transiently produce antigenic proteins or therapeutic antibodies directly in vivo, avoiding some of the limitations of viral vectors and classic protein manufacturing.
The current pipeline is concentrated around three thematic pillars:
- HPV-related diseases: INO-3107 for adult RRP, and the VGX-3100 / INO-3100 family for cervical and lower-genital tract lesions (now largely de-prioritised outside China).
- Immuno-oncology: multi-antigen candidates such as INO-5401 for glioblastoma and prevention programmes in BRCA-mutated populations, often in combination with checkpoint inhibitors.
- Infectious diseases and DMAb: Ebola booster INO-4201 and DNA-encoded monoclonal antibodies (DMAb) in collaboration with Wistar, AstraZeneca and academic centres.
From a value-creation standpoint, however, the entire near-term equity story is dominated by INO-3107 in adult RRP.
INO-3107 in RRP – mechanism, data and designations
Mechanism and target disease
INO-3107 is a DNA immunotherapy designed to induce T-cell responses against the E6 and E7 proteins of HPV-6 and HPV-11, the low-risk HPV types responsible for most cases of RRP. The idea is to train cytotoxic T cells to recognise and clear infected cells in the respiratory tract, reducing or even eliminating the papillomas that currently require repetitive surgery.
RRP itself is a rare but debilitating airway disease. Benign papillomas grow in the larynx and sometimes the lower airway, causing hoarseness, airway obstruction, repeated surgical interventions and a meaningful impact on quality of life. Surgery remains the standard of care but is palliative and damaging over time.
Phase 1/2 and long-term follow-up
The pivotal clinical package rests on:
- a Phase 1/2 open-label trial (RRP-001) in 32 adults who had at least two surgeries in the year before dosing; and
- a retrospective long-term follow-up (RRP-002) in 28 of those patients, with a median total follow-up of about 2.8 years after treatment.
Key reported points from the Phase 1/2 and retrospective dataset:
- Patients had a median of 4 surgeries (range 2–8) in the 12 months prior to INO-3107.
- In the first 12 months after dosing, around 72% of patients achieved a 50–100% reduction in the number of surgeries.
- In the second 12-month period, without any additional dosing, the proportion with a 50–100% reduction increased to about 86%, with the complete response rate (zero surgeries) rising from roughly 28% to 50%.
- The mean number of surgeries per year dropped from about 4.1 in the pre-treatment period to 1.7 in Year 1 and 0.9 in Year 2, with partial data into Year 3 maintaining the downward trend.
- Safety has been benign so far, with mostly low-grade adverse events such as injection-site pain and fatigue and no significant long-term safety signal reported in the RRP cohorts.
Immunology work published in peer-reviewed journals shows that INO-3107 induces antigen-specific CD4 and CD8 T-cells that traffic to airway tissue and correlate with clinical improvement, giving mechanistic support to the observed reduction in surgeries.
Regulatory status and designations
On the regulatory front, INO-3107 has accumulated an unusually rich set of designations:
- Orphan Drug and Breakthrough Therapy designation in the United States.
- Orphan designation in the European Union.
- Innovation Passport in the UK under the ILAP framework.
- CE-mark for the CELLECTRA delivery device, allowing commercial use of the device in CE-recognising markets.
The key new piece is the BLA acceptance under Standard Review with PDUFA on 30 October 2026. The controversy around accelerated approval is now explicit: the FDA has told the company that, in its preliminary view, the current package does not yet sufficiently justify accelerated approval, even if the agency is proceeding with the review.
Inovio intends to meet the FDA to argue its case; in parallel, a confirmatory trial in adult RRP (approximately 100 patients, randomised 2:1, around 20 US sites) is planned during the review period.
Other pipeline assets (short overview)
INO-3112 – HPV-related head and neck cancer
INO-3112 combines an HPV16/18 DNA immunotherapy with the anti-PD-1 antibody LOQTORZI in high-risk, HPV-positive oropharyngeal squamous cell carcinoma (OPSCC). The Phase 3 design has been discussed with the FDA and alignment with European regulators is in progress. This is a medium-term catalyst and unlikely to change the 2026 funding picture before INO-3107’s PDUFA.
INO-5401 – glioblastoma and BRCA-mutated prevention
INO-5401 is a three-antigen construct (hTERT, WT-1, PSMA) in early-stage development. Combination studies with Libtayo in glioblastoma have produced encouraging but non-definitive survival data; additional work in BRCA1/2-mutated subjects focuses on prevention and immune priming. These programmes are currently scientific upside rather than financial drivers.
INO-4201 and DMAb technology
INO-4201 is an Ebola booster candidate for individuals previously vaccinated with Ervebo, with early-stage data indicating robust boosting of protective immunity. The DMAb platform (DNA-encoded antibodies) has delivered proof-of-concept in humans for long-acting expression of neutralising antibodies against SARS-CoV-2, in partnership with Wistar, AstraZeneca and academic groups. These platforms are valuable scientifically, but they sit behind INO-3107 in the queue for capital and commercial attention.
Financial snapshot and five-year dilution pattern
Current financial position
- Cash, cash equivalents and short-term investments: 50.8 million USD as of 30 September 2025.
- No debt reported on the balance sheet at that date.
- Net loss Q3 2025: 45.5 million USD, roughly double the prior-year quarter, largely due to a non-cash loss on warrant revaluation; operating loss was about 21.2 million USD.
- Cash runway guidance: into the second quarter of 2026, assuming no additional financings and an estimated net cash burn of about 22 million USD in Q4 2025.
Equity raises – the pattern
Over the last five years Inovio has repeatedly issued new equity and warrants to fund operations. A non-exhaustive list of larger deals illustrates the pattern:
- January 2021 – public offering of common stock, followed by full exercise of the underwriters’ option, resulting in proceeds around the mid-hundreds of millions of dollars and a significant expansion of the share count.
- April 2024 – underwritten offering of common stock and pre-funded warrants, with expected gross proceeds of about 36 million USD; the stock fell more than 20% in after-hours trading on the news.
- December 2024 – public offering of common stock and warrants targeting about 30 million USD of gross proceeds.
- July 2025 – additional public offering combining shares and warrants, publicly announced at roughly 25 million USD in gross proceeds.
- November 2025 – underwritten stock offering of 13.158 million shares at 1.90 USD per share, plus a 30-day option for almost 2 million extra shares, again for about 25 million USD in gross proceeds.
Together with previous years’ activity, these transactions explain why many long-time retail investors describe the stock as having been turned into a “cash machine” for the company. From a purely factual standpoint, Inovio has funded essentially all of its RRP development and BLA work via repeated equity issuance, and the runway still stops well before the 2026 PDUFA date.
The straight conclusion is that, unless non-dilutive capital appears, at least one more financing event
before the PDUFA looks more likely than not – with obvious consequences for existing shareholders.
Retail sentiment and community chatter
Sentiment block – non-professional commentary onlyStocktwits and trading communities
On Stocktwits, INO has more than ninety-thousand followers and behaves like a classic high-beta event-driven small cap. In bullish phases the stream fills with posts focusing on “first DNA medicine”, “RRP game changer” and implied multi-bagger scenarios if INO-3107 is approved. On days like 29 December 2025, the tone flips quickly to anger and capitulation as another regulatory nuance or capital raise hits the tape.
Reddit: two very different angles
- In r/Inovio and similar spaces, some users still share optimistic breakdowns of RRP data and 2025/2026 milestones, arguing that slower-than-expected surgery counts and durable responses put the company in a strong negotiating position with regulators.
- Others, including self-described long-time investors who committed over 100k USD five years ago and now sit on losses above 90%, explicitly state they will not add a single share until the company gets a product approved and generates real revenue. For them, management has “spent” its credibility through years of dilution and delays.
Patient and disease-focused communities
In RRP-focused patient forums, the tone is very different: discussions tend to be detailed and pragmatic, centred on surgery burden, quality of life and the prospect of an injectable treatment that might allow patients to go months or years without going back to the operating room. Here, the company’s messaging around “every surgery matters” resonates strongly and the main concern is access and timing rather than stock price.
Overall retail sentiment is split: RRP patients and clinicians see INO-3107 as a serious, potentially disease-changing
option if approved; many equity holders look at the same company and mainly see years of dilution and missed timelines.
Both perspectives are valid and need to be kept in mind when framing risk.
Important: all comments from Reddit, Stocktwits, forums and similar platforms come from non-professional traders or patients. They can be useful to gauge sentiment but they are not a reliable source of financial, medical or regulatory advice.
Analyst expectations and scenario map
Consensus view
According to recent consensus compilations, nine covering analysts currently classify INO as a “Hold” on average, with one Sell, three Hold and five Buy ratings, and an average 12-month price target around 9 USD. Individual targets span a wide range (roughly 3–18 USD), reflecting very different assumptions about probability of approval, revenue ramp and capital structure evolution.
Independent aggregators that look at a slightly different analyst set report a similar picture: median targets in the high-single-digits, with upside of several hundred percent relative to late-December 2025 spot prices, but explicitly framed as high-risk, binary-outcome exposure.
Very high-level scenario sketch (editorial, not valuation)
- Positive regulatory outcome, survivable dilution INO-3107 is approved in RRP, whether under accelerated or traditional approval, and Inovio manages to bridge the gap to launch with a mix of equity and non-dilutive funding that does not completely crush the cap table. In this world, INO behaves like a traditional rare-disease commercialisation story with potential upside from label expansion and ex-US rights.
- Regulatory delay or messy negotiation FDA pushes for additional data, a stricter endpoint or a different analysis, delaying or complicating approval. With cash runway into 2Q 2026 and PDUFA in Q4 2026, this scenario almost automatically implies more heavy dilution, and sentiment could deteriorate sharply even before a final decision.
- Regulatory failure A clear rejection or a requirement for a new, large trial without a credible funding path could effectively collapse the current equity story, leaving early-stage assets (INO-3112, INO-5401, DMAb) as scientific, but not near-term commercial, optionality.
None of these sketches is a forecast or probability assignment. They are simple frames to highlight how much of the current analyst upside is contingent on a narrow set of regulatory and financing assumptions.
Key risks and editorial bottom line
Key risks
- Single-asset concentration – near-term equity value is overwhelmingly tied to INO-3107; other pipeline assets are too early or too small to materially de-risk the story on their own.
- Regulatory uncertainty around accelerated approval – the FDA has already flagged concerns about eligibility; details of the discussion will matter, and a Standard Review timetable does not guarantee a positive outcome.
- Funding gap vs PDUFA – current cash does not clearly cover the period up to and beyond the October 2026 PDUFA. Additional financing – likely equity or equity-linked – looks probable, with dilution risk for existing shareholders.
- Execution risk in a rare disease market – even with approval, commercial execution in a small, specialised market (ENT centres, tertiary hospitals, Europe/UK alignment) is non-trivial and will require investment in a lean but competent field infrastructure.
- Reputational overhang with retail – years of heavy dilution and missed timelines mean that parts of the retail base have effectively written off management’s credibility; this can exacerbate volatility and limit the “story stock” premium even if data are good.
Bottom line (editorial, educational only)
The INO equity story is simple and harsh at the same time: a small company with a potentially important DNA medicine for a rare but very real disease burden, but with a long history of dilution and a funding runway that stops before the key regulatory date.
Clinically, the surgery-reduction data in RRP, plus the durability now supported by The Laryngoscope paper, make INO-3107 a serious candidate to become the first non-surgical standard in this niche if approved. Regulators, however, do not approve “mechanistic plausibility plus nice graphs”; they approve drugs when they are convinced that the totality of evidence supports safety and efficacy under the chosen framework, and the latest FDA letter shows that the debate on that framework is still open.
For traders and investors, this remains a high-beta, binary-outcome name where risk management, position sizing and time horizon may matter more than the raw upside scenarios advertised in many retail posts. The market clearly understands the binary nature of the story – as seen by the violent move on 29 December – but opinions differ widely on whether the current price compensates for that risk.
This entire section is an editorial synthesis meant for educational purposes and discussion. It is not, and must not be interpreted as, a recommendation to buy, hold or sell INO or any other security.
Sources and further reading (EN)
- Inovio IR – FDA Accepts for Review INOVIO’s BLA for INO-3107 for the Treatment of Adults with RRP (press release, 29 Dec 2025). Link
- Inovio IR – Data Published in The Laryngoscope shows INO-3107 Resulted in Long-Term Surgery Reduction in RRP (press release, 11 Aug 2025). Link
- Inovio – DNA Medicines Pipeline (INO-3107 overview and designations). Link
- Inovio IR / PRNewswire – INOVIO Highlights Anticipated 2025 Milestones and 2024 Key Accomplishments (9 Jan 2025). Link
- Inovio IR / PRNewswire – INOVIO Reports Third Quarter 2025 Financial Results and Recent Business Highlights (10 Nov 2025). Link
- PRNewswire / IR – INOVIO Announces Pricing of Public Offering of Common Stock (Jan 2021); April 2024, December 2024 and November 2025 offering press releases. News list
- MarketBeat – “Inovio Pharmaceuticals, Inc. (NASDAQ: INO) Given Consensus Recommendation of ‘Hold’ by Analysts” (6 Dec 2025). Link
- MarketWatch – daily trading recap for INO on 29 Dec 2025 (price move and volume). Quote page
- Stocktwits – INO symbol page (price, followers and sentiment stream). Link
- Reddit – r/Inovio and r/RRP threads on INO-3107 durability, BLA milestones and personal investor stories. r/Inovio · r/RRP
All external links were last checked around the end of December 2025. Figures and opinions from those sources may change over time.
Important disclaimer (English)
This report is an editorial and educational analysis based on publicly available information (company filings, official press releases, peer-reviewed publications and major financial news sources). It is not, and must not be interpreted as, investment research, personalised advice or a solicitation to buy or sell any financial instrument. The information may be incomplete or become outdated and no guarantee is given on its accuracy. Readers should always do their own due diligence, cross-check figures with official filings and consider seeking advice from a qualified financial professional before making any investment decision. The author and Merlintrader trading Blog may use referral or affiliate links for third-party tools or platforms; any such commercial relationships do not change the substance of the analysis.
This report is an editorial and educational analysis based on publicly available information (company filings, official press releases, peer-reviewed publications and major financial news sources). It is not, and must not be interpreted as, investment research, personalised advice or a solicitation to buy or sell any financial instrument. The information may be incomplete or become outdated and no guarantee is given on its accuracy. Readers should always do their own due diligence, cross-check figures with official filings and consider seeking advice from a qualified financial professional before making any investment decision. The author and Merlintrader trading Blog may use referral or affiliate links for third-party tools or platforms; any such commercial relationships do not change the substance of the analysis.
Legal resources (site): Disclaimer · Condizioni d’uso e privacy
News del giorno – 29 dicembre 2025
La FDA accetta la BLA di INO-3107, Standard Review, PDUFA 30 ottobre 2026
Il 29 dicembre 2025 la FDA ha accettato per revisione la Biologics License Application di INO-3107 come potenziale trattamento per gli adulti con Recurrent Respiratory Papillomatosis (RRP). La classificazione della revisione è Standard e l’agenzia ha fissato una PDUFA target action date al 30 ottobre 2026. Al momento la FDA ha anche indicato che non prevede di convocare un Advisory Committee su questo dossier.
Inovio ha presentato la domanda nel percorso di accelerated approval, ma nella lettera di accettazione la FDA segnala come “potential review issue” la propria conclusione preliminare secondo cui i dati attuali non sono ancora sufficienti a giustificare l’accesso a questo percorso. L’azienda continua a sostenere che INO-3107 offra un beneficio clinico rilevante rispetto alla sola chirurgia e intende chiedere un meeting con l’agenzia per discutere come restare nel programma di approvazione accelerata. In parallelo, precisa di non avere in programma un filing nel percorso tradizionale.
Il mercato azionario ha reagito in modo violento: nella stessa seduta le azioni INO sono scese di circa -24% fino a 1,73 USD, con volumi attorno a 6,1 milioni di pezzi – ben oltre la media recente – segno di quanto questa BLA sia centrale per l’intera storia azionaria.
In sintesi: il calendario regolatorio ora è visibile (PDUFA a fine 2026), ma la FDA ha già messo nero su bianco
che l’eleggibilità all’accelerated approval non è affatto scontata con il pacchetto dati attuale.
Executive summary – perché INO è una scommessa binaria
Oggi Inovio è, di fatto, una storia azionaria quasi mono-asset centrata su INO-3107 negli adulti con RRP. Se approvato, INO-3107 sarebbe sia il primo prodotto commerciale della società sia il primo DNA medicine approvato negli Stati Uniti, su una nicchia rara ma con un peso clinico importante.
- Dati clinici: nello studio di Fase 1/2 (32 adulti con numerosi interventi l’anno) il 72% dei pazienti ha ottenuto una riduzione del 50–100% del numero di interventi chirurgici nel primo anno dopo il trattamento. Nel follow-up retrospettivo questa quota sale all’86% nel secondo anno, con una riduzione della media degli interventi da 4,1 per anno a 0,9 e circa metà dei pazienti senza più interventi.
- Setup regolatorio: la BLA è stata accettata, con data fissata (30 ottobre 2026), ma la FDA ha già fatto capire che il tema dell’accelerated approval è aperto e che i dati potrebbero non bastare nei termini attuali.
- Struttura finanziaria: cassa e investimenti a breve per circa 50,8 milioni di USD al 30 settembre 2025, nessun debito, ma una guidance di runway solo fino al secondo trimestre 2026. Negli ultimi anni l’azienda ha fatto ricorso ripetuto ad aumenti di capitale importanti (2021, aprile 2024, dicembre 2024, luglio 2025, novembre 2025), spesso a forte sconto e seguiti da crolli a doppia cifra.
- Sentiment: nel mondo RRP (pazienti e specialisti) la percezione è di interesse e cauto ottimismo; tra i retail storici su INO la spaccatura è forte, con molti che lamentano perdite superiori al 90% dopo anni di diluizione.
- Analisti: il consenso si colloca intorno al “Hold”, con un target price medio a 12 mesi intorno ai 9 USD e un range molto ampio, che incorpora ipotesi aggressive su successo regolatorio e sostenibilità della struttura del capitale.
Tradotto senza giri di parole: se INO-3107 fallisce o si incaglia, c’è ben poco nel setup attuale che possa sostenere il titolo nel breve.
Quick data panel (fine dicembre 2025)
Ticker / Mercato
INO – Nasdaq
Close 29/12/2025
1,73 USD (-24,45% nella seduta)
Range 52 settimane
1,30 – 2,98 USD
Market cap
~155–160 M USD
Cassa + ST inv. (30/09/2025)
50,8 M USD – nessun debito
Runway stimata
fino a 2Q 2026 (guidance aziendale)
Rating consenso
Hold (5 Buy / 3 Hold / 1 Sell)
Target medio 12 mesi
≈ 9 USD (range 3–18)
Potenziale primo DNA medicine approvato
Mercato raro ma reale
Forte diluizione storica
Runway corta vs PDUFA
Prezzi e metriche qui sono una fotografia indicativa intorno al 29 dicembre 2025. Servono solo a dare ordini di grandezza e non sostituiscono dati in tempo reale.
Azienda e piattaforma DNA medicines
Inovio è una small cap biotech focalizzata sulle DNA medicines, plasmidi consegnati con il device proprietario CELLECTRA. L’approccio punta a far produrre alle cellule del paziente, per un periodo limitato, le proteine di interesse (antigeni o anticorpi) direttamente in vivo, evitando alcuni limiti dei vettori virali e delle produzioni proteiche tradizionali.
La pipeline ruota attorno a tre assi principali:
- Patologie HPV-correlate: INO-3107 per RRP negli adulti e il gruppo VGX-3100 / INO-3100 per le lesioni cervicali e genitali (in buona parte de-prioritizzati fuori dalla Cina).
- Immuno-oncologia: candidati multi-antigene come INO-5401 per il glioblastoma e programmi in portatori di mutazioni BRCA1/2.
- Malattie infettive e DMAb: il booster Ebola INO-4201 e gli anticorpi monoclonali codificati da DNA (DMAb) in collaborazione con Wistar, AstraZeneca e centri accademici.
Dal punto di vista del valore per l’azionista, però, nel breve la storia è quasi interamente INO-3107 in RRP.
INO-3107 in RRP – meccanismo, dati e stato regolatorio
Meccanismo d’azione e patologia target
INO-3107 è un’immunoterapia a DNA progettata per indurre risposte T-cellulari contro le proteine E6/E7 di HPV-6 e HPV-11, i genotipi responsabili della maggior parte dei casi di RRP. L’obiettivo è “insegnare” al sistema immunitario a riconoscere e eliminare le cellule infette nelle vie aeree, riducendo o eliminando le papillomatosi che oggi richiedono interventi chirurgici ripetuti.
La RRP è una malattia rara ma altamente invalidante delle vie aeree: papillomi benigni del laringe e, talvolta, delle vie aeree inferiori causano disfonia, ostruzione respiratoria, infezioni ricorrenti e un impatto enorme sulla qualità di vita. La chirurgia resta lo standard of care ma è solo palliativa e cumulativamente dannosa.
Dati di Fase 1/2 e follow-up a lungo termine
Il pacchetto clinico chiave si basa su:
- uno studio di Fase 1/2 open-label (RRP-001) in 32 adulti con almeno due interventi l’anno prima del trattamento; e
- un follow-up retrospettivo (RRP-002) in 28 di questi pazienti, con un follow-up mediano totale di circa 2,8 anni dopo il trattamento.
I punti principali comunicati da Inovio e dal paper su The Laryngoscope:
- mediana di 4 interventi nei 12 mesi pre-trattamento (range 2–8);
- nel primo anno dopo INO-3107 circa il 72% dei pazienti ha avuto una riduzione del 50–100% del numero di interventi;
- nel secondo anno, senza ulteriori dosi, la quota con riduzione del 50–100% sale a ~86%, con il tasso di risposta completa (zero interventi) che passa da circa 28% a 50%;
- il numero medio di interventi per anno scende da ~4,1 nel periodo pre-trattamento a 1,7 nel primo anno e 0,9 nel secondo, con dati parziali del terzo anno che confermano il trend;
- il profilo di sicurezza è favorevole: eventi avversi principalmente di grado lieve (dolore in sede di iniezione, affaticamento) e nessun segnale di problemi a lungo termine nel gruppo RRP.
I dati immunologici pubblicati mostrano che INO-3107 induce popolazioni di linfociti T CD4 e CD8 antigeno-specifiche che raggiungono il tessuto delle vie aeree e si associano alla riduzione degli interventi chirurgici, dando coerenza meccanicistica al beneficio clinico.
Designazioni e percorso regolatorio
Sul fronte regolatorio, INO-3107 ha ottenuto:
- Orphan Drug e Breakthrough Therapy designation negli Stati Uniti;
- Orphan designation nell’Unione Europea;
- Innovation Passport nel Regno Unito (ILAP);
- CE-mark per il device CELLECTRA in UE e in altri mercati che riconoscono la marcatura CE.
Il punto nuovo è l’accettazione della BLA con Standard Review e PDUFA al 30 ottobre 2026. La FDA ha però già indicato che, nella sua analisi preliminare, il pacchetto dati potrebbe non essere sufficiente a sostenere l’accelerated approval. L’azienda cercherà un confronto formale con l’agenzia; in parallelo è previsto uno studio confermatorio randomizzato in RRP nell’arco della revisione.
Altra pipeline (cenni rapidi)
INO-3112 – tumori testa/collo HPV-positivi
INO-3112 combina un’immunoterapia a DNA anti-HPV16/18 con l’anti-PD-1 LOQTORZI in pazienti con OPSCC HPV-positivo ad alto rischio. Il disegno di Fase 3 è stato discusso con la FDA; si cerca l’allineamento con EMA. È un catalyst di medio periodo, improbabile che sposti il profilo di rischio prima del 2026.
INO-5401, INO-4201, DMAb
INO-5401 (glioblastoma e prevenzione BRCA), INO-4201 (booster Ebola) e la piattaforma DMAb rappresentano upside scientifico interessante, ma oggi non sono i driver della cassa. La traiettoria a breve resta vincolata al binomio INO-3107 + struttura del capitale.
Situazione finanziaria e pattern di diluizione
Foto attuale
- Cassa + investimenti a breve: 50,8 M USD al 30 settembre 2025, nessun debito.
- Perdita netta Q3 2025: 45,5 M USD (0,87 USD per azione), con una parte importante legata al fair value dei warrant; la perdita operativa è più contenuta (~21,2 M USD).
- Guidance di cassa: runway stimato fino al secondo trimestre 2026, assumendo nessun nuovo aumento di capitale e un burn di ~22 M USD nel Q4 2025.
Gli aumenti di capitale negli ultimi anni
Negli ultimi cinque anni Inovio ha fatto ricorso in modo ricorrente ad aumenti di capitale e emissione di warrant. In sintesi:
- Gennaio 2021 – offerta pubblica di azioni ordinarie con successivo esercizio completo dell’opzione greenshoe da parte degli underwriter, per un controvalore complessivo nell’ordine delle centinaia di milioni di dollari.
- Aprile 2024 – underwritten offering di azioni + pre-funded warrant per circa 36 M USD di proventi lordi, con crollo del titolo di oltre il 20% in after-hours.
- Dicembre 2024 – nuova offerta pubblica di azioni + warrant per circa 30 M USD di proventi lordi.
- Luglio 2025 – ulteriore operazione mista azioni + warrant per circa 25 M USD lordi.
- Novembre 2025 – aumento da 25 M USD con 13,158 milioni di azioni a 1,90 USD e opzione per quasi 2 milioni di azioni aggiuntive.
Sommando queste mosse ai passaggi precedenti, è abbastanza evidente perché molti retail descrivono la società come un “bancomat azionario”: l’intero percorso di sviluppo e BLA di INO-3107 è stato finanziato quasi esclusivamente tramite equity, e nonostante questo la cassa non copre ancora il tratto fino e oltre la PDUFA.
Tradotto: a meno di accordi non diluitivi inattesi, è ragionevole aspettarsi almeno un’altra operazione
di raccolta prima della PDUFA, con potenziale impatto ulteriore sugli azionisti esistenti.
Sentiment retail e community
Sentiment – commenti di trader e pazienti non professionistiStocktwits e trading “mordi e fuggi”
Su Stocktwits INO ha oltre novantamila follower e si comporta come una small cap event-driven ad altissimo beta. Nei momenti di entusiasmo abbondano i post che puntano su “primo DNA medicine approvato”, “game changer in RRP” e su upside multipli se la FDA dirà sì. Nelle giornate negative (come il 29 dicembre) il flusso si riempie rapidamente di sfiducia, frustrazione e accuse al management per l’ennesima doccia fredda.
Reddit: tra speranza e burnout
- Nei thread più tecnici compaiono analisi dettagliate di dati, design dello studio confermatorio e timeline regolatorio, con utenti convinti che la durabilità dell’effetto chirurgico dia a INO-3107 una posizione forte nella trattativa con l’FDA.
- In altri thread, investitori retail di lungo corso raccontano di aver investito oltre 100k USD cinque anni fa e di trovarsi oggi con perdite superiori al 90%, dichiarando esplicitamente di non voler più “mettere un centesimo” finché non vedranno un prodotto approvato e ricavi reali. Per molti di loro la fiducia nel management è finita.
Community RRP e pazienti
Nei forum dedicati alla RRP il tono è completamente diverso: il focus è sul numero di interventi, sulla voce, sul rischio di tracheostomie ripetute e sul peso psicologico della malattia. Qui il messaggio “ogni intervento conta” arriva forte; l’interesse principale non è il prezzo del titolo, ma quando un trattamento come INO-3107 potrà essere disponibile, quanto durerà l’effetto e come sarà gestito l’accesso.
Nel complesso il sentiment è polarizzato: la community RRP vede in INO-3107 un potenziale cambio di paradigma;
una parte rilevante dei piccoli azionisti vede soprattutto anni di diluizione e promesse non mantenute.
Chi valuta il titolo deve tenere presente entrambi i lati della medaglia.
Nota: i commenti provenienti da Reddit, Stocktwits, forum e simili non rappresentano analisi professionali. Sono utili per capire il clima, non per prendere decisioni operative.
Analisti e scenari possibili
Consenso attuale
Le sintesi più recenti indicano un rating medio “Hold” su INO, con 1 Sell, 3 Hold e 5 Buy e un target price medio a 12 mesi intorno ai 9 USD. Il range dei target è molto ampio (circa 3–18 USD), segno che le ipotesi su probabilità di approvazione, ricavi potenziali e diluizione sono tutt’altro che uniformi.
Tre scenari molto semplificati
- Scenario positivo – INO-3107 viene approvato (accelerated o tradizionale) e Inovio riesce a superare il gap di cassa con una combinazione di equity e capitali non diluitivi senza distruggere totalmente la struttura del capitale. Il titolo evolve verso una classica storia di commercializzazione in malattia rara.
- Scenario di frizione/regolatorio – la FDA chiede dati aggiuntivi, modifica dell’endpoint o un ulteriore trial, con allungamento dei tempi. Con una runway dichiarata solo fino a 2Q 2026 e una PDUFA a fine ottobre 2026, questo scenario implica quasi automaticamente nuova diluizione pesante.
- Scenario negativo – rifiuto netto o richiesta di un nuovo studio di grandi dimensioni senza una chiara via di finanziamento. In questo caso la storia su INO cambia radicalmente: gli asset di pipeline restano interessanti, ma il profilo azionario nel breve può diventare molto fragile.
Si tratta solo di schemi qualitativi per orientare il ragionamento, non di previsioni né di probabilità associate.
Rischi principali e conclusione editoriale
Rischi da tenere ben presenti
- Concentrazione su un solo asset – nel breve quasi tutto dipende da INO-3107; gli altri programmi sono troppo indietro per compensare un eventuale esito negativo.
- Incertezza sull’accelerated approval – la FDA ha già messo in dubbio l’eleggibilità; le discussioni con l’agenzia saranno determinanti e l’esito non è scontato.
- Gap di cassa rispetto alla PDUFA – l’attuale cassa non copre chiaramente il percorso fino e oltre la decisione del 2026; altre operazioni di funding sono probabili e potenzialmente diluitive.
- Esecuzione commerciale in malattia rara – anche con l’approvazione, costruire un’infrastruttura commerciale efficiente in un mercato piccolo e specialistico non è banale e richiede ulteriore capitale.
- Overhang reputazionale verso il retail – anni di diluizione e promesse disattese hanno logorato la fiducia di una parte degli investitori individuali, con effetti su volatilità e capacità del titolo di prezzare scenari positivi.
Bottom line (editoriale, non operativa)
La storia Inovio oggi è estremamente semplice e allo stesso tempo scomoda: un’azienda con una tecnologia interessante e un candidato che potrebbe cambiare la gestione di una nicchia rara come la RRP, ma con una struttura di capitale tirata, una lunga sequenza di aumenti e un percorso regolatorio ancora in evoluzione.
I dati su riduzione degli interventi e durabilità sono solidi per una fase 1/2 e il razionale meccanicistico è credibile; tuttavia, come sempre, non è il mercato a decidere, ma la FDA. Il fatto che l’agenzia abbia acceso un faro sull’accelerated approval indica che la discussione tecnica sarà complessa.
Per chi guarda il titolo, il punto non è tanto se esista o meno upside potenziale (il consenso sugli analisti dice che sulla carta è enorme), ma quanto rischio si è disposti ad assumere in una storia così binaria e quanto spazio si lascia a nuove diluizioni. Sono variabili da valutare caso per caso, sulla base del proprio profilo di rischio e orizzonte temporale.
Questa sezione rappresenta una sintesi editoriale a fini informativi. Non costituisce in alcun modo una raccomandazione di acquisto, vendita o mantenimento del titolo INO o di altri strumenti finanziari.
Fonti principali (IT)
- Inovio IR – FDA Accepts for Review INOVIO’s BLA for INO-3107 for the Treatment of Adults with RRP (29 dicembre 2025). Link
- Inovio IR – Data Published in The Laryngoscope shows INO-3107 Resulted in Long-Term Surgery Reduction in RRP (11 agosto 2025). Link
- Pagina ufficiale Inovio – DNA Medicines Pipeline (sezione INO-3107). Link
- Inovio – “INOVIO Highlights Anticipated 2025 Milestones and 2024 Key Accomplishments” (9 gennaio 2025). Link
- Inovio – “INOVIO Reports Third Quarter 2025 Financial Results and Recent Business Highlights” (10 novembre 2025). Link
- PR e comunicati su aumento di capitale (gennaio 2021, aprile 2024, dicembre 2024, luglio 2025, novembre 2025) da IR Inovio e PRNewswire. News list
- MarketBeat – consenso analisti e target price su INO (articolo 6 dicembre 2025). Link
- MarketWatch – scheda quotazione INO e recap giornaliero della seduta del 29 dicembre 2025. Link
- Stocktwits – INO symbol page (followers, sentiment). Link
- Reddit – community r/Inovio e r/RRP (discussioni su INO-3107, BLA, esperienze personali di pazienti e investitori). r/Inovio · r/RRP
Disclaimer importante (italiano)
Questo report è un’analisi editoriale a scopo esclusivamente informativo e didattico, basata su fonti pubbliche considerate affidabili (comunicati ufficiali, filing SEC, pubblicazioni peer-review, principali fonti di news). Non costituisce ricerca in senso regolamentare, né raccomandazione personalizzata, né sollecitazione al pubblico risparmio. Dati e valutazioni possono essere incompleti o soggetti a variazioni; chi legge è tenuto a verificare sempre le informazioni direttamente nelle fonti primarie (SEC, comunicati societari, FDA) e a valutare la propria situazione economico-finanziaria, eventualmente con il supporto di un consulente abilitato. Il sito Merlintrader trading Blog può utilizzare link di affiliazione verso terze parti (es. piattaforme dati o broker); tali rapporti commerciali non modificano la sostanza del contenuto editoriale.
Questo report è un’analisi editoriale a scopo esclusivamente informativo e didattico, basata su fonti pubbliche considerate affidabili (comunicati ufficiali, filing SEC, pubblicazioni peer-review, principali fonti di news). Non costituisce ricerca in senso regolamentare, né raccomandazione personalizzata, né sollecitazione al pubblico risparmio. Dati e valutazioni possono essere incompleti o soggetti a variazioni; chi legge è tenuto a verificare sempre le informazioni direttamente nelle fonti primarie (SEC, comunicati societari, FDA) e a valutare la propria situazione economico-finanziaria, eventualmente con il supporto di un consulente abilitato. Il sito Merlintrader trading Blog può utilizzare link di affiliazione verso terze parti (es. piattaforme dati o broker); tali rapporti commerciali non modificano la sostanza del contenuto editoriale.
Link legali del sito: Disclaimer · Condizioni d’uso e info privacy
Biotech Catalyst Calendar
Per avere una visione d’insieme aggiornata dei principali catalyst biotech (PDUFA, letture di trial, meeting FDA, eventi regolatori), puoi consultare il Biotech Catalyst Calendar dedicato sul sito Merlintrader. È uno strumento pensato per affiancare i singoli report sui titoli con una vista calendario ordinata per data.
Vai al Biotech Catalyst CalendarScanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


