Aquestive Therapeutics (AQST) – Anaphylm CRL 2026 Deep Dive: Human Factors, PK Study and the Road to Resubmission
Quick Snapshot – Where We Stand After the CRL
- Ticker / Exchange: AQST – NASDAQ
- Lead asset: Anaphylm™ (dibutepinephrine sublingual film)
- Indication: Type I allergic reactions, including anaphylaxis, in patients ≥30 kg
- Original PDUFA: January 31, 2026 (NDA now the subject of a CRL dated January 30, 2026)
- CRL scope: Human factors (pack opening, film placement), instructions for use, pouch/carton labeling, plus one PK study linked to the packaging changes – no new large clinical trials requested, no CMC issues raised
- Clinical package: 11 studies, ~967 total administrations, 411 subjects, 840 single-dose and 127 repeat-dose exposures
- Balance sheet: Cash and cash equivalents of $129.1M as of September 30, 2025; company later guided to roughly $120M (unaudited) as of December 31, 2025
- Global plan: Expects to file in Europe and Canada in 2H 2026; EMA feedback indicated no additional clinical trials needed before EU submission
- Today’s tape: sharp rebound (around +40–45% intraday) as the market digests a CRL that is serious, but appears fixable and bounded compared with worst-case fears
0. Executive Summary – From Unknown “Deficiencies” to a Bounded CRL
In early January 2026, the FDA notified Aquestive that it had identified “deficiencies that precluded discussions of labeling and post-marketing requirements” for the Anaphylm NDA. At that point, neither investors nor management had visibility on which part of the dossier was at risk: clinical robustness, safety, CMC, human factors, or something else.
Our previous deep dive on Merlintrader took a deliberately cautious but not catastrophic stance: we flagged the letter as a non-trivial event, but also underlined that without concrete details it was impossible to conclude that “the drug was dead”. The stock reacted with a violent sell-off (around –36% in pre-market), effectively repricing the probability of delay and of a potential Complete Response Letter.
On January 30, 2026, the FDA indeed issued a Complete Response Letter for Anaphylm. The crucial point is what the CRL does and does not say:
- The deficiencies are limited to human factors and administration: difficulty opening the pouch and incorrect film placement in the HF validation study, plus labeling/instructions-for-use aspects.
- Once HF issues are addressed, the Agency wants a single PK study to understand the impact of the modifications – HF and PK can be run in parallel.
- The CRL does not raise new CMC concerns and does not question the underlying clinical efficacy/safety package; comparability data submitted with the NDA were not challenged.
- No additional large efficacy trials were requested. The company expects to resubmit the NDA as early as Q3 2026, subject to completing HF and PK work and normal FDA timelines.
In other words, we are looking at a real delay, not a clean approval – but also at a CRL that appears operational and bounded rather than a fundamental repudiation of Anaphylm’s pharmacology. This is why the stock is sharply higher today: the market had already priced in a disaster scenario where “deficiencies” meant deep clinical or safety problems, and instead it got something closer to a packaging/administration reset with one supportive PK study.
The flip side is time. Even in a “fixable” CRL, running a fresh HF validation study, a PK trial, having a Type A meeting, resubmitting in the second half of 2026 and then going through a new review cycle means many months where the story is again largely binary and catalyst-light. After today’s relief rally, AQST is back in a zone where patience and risk tolerance will matter more than adrenaline.
1. Company Snapshot and Why Anaphylm Matters So Much
1.1 Business model in one paragraph
Aquestive Therapeutics is a specialty pharma business built around complex-molecule delivery via oral and sublingual film technologies. Historically known under the “PharmFilm” umbrella, the platform has already delivered multiple licensed products in CNS and addiction, manufactured by Aquestive and commercialized by partners. Revenue today comes from these licensed films plus milestone and royalty structures, while the key equity driver is the proprietary pipeline – with Anaphylm front and center as the potential first non-invasive epinephrine rescue option.
1.2 What Anaphylm is trying to do
Anaphylm is a sublingual film containing a prodrug of epinephrine for the treatment of severe allergic reactions, including anaphylaxis, in patients weighing at least 30 kg. The core idea is simple: replace a bulky, needle-based auto-injector with a small, thin, fast-dissolving film that can be carried more easily and used with less hesitation in emergencies.
The target market is the same as for classic auto-injectors (EpiPen and peers), but the positioning is built on:
- Eliminating the needle and the “stabbing” step;
- Higher portability (primary packaging smaller and thinner than a credit card);
- A PK profile designed to be comparable to IM epinephrine according to the existing data package.
2. Clinical and PK/PD Package – What Has Not Changed
One of the most important clarifications in the CRL is what is not under attack. The company explicitly notes that comparability data such as bracketing, repeat-dose and sustainability – the backbone of the Anaphylm clinical development program – were not questioned in the CRL.
2.1 Size and structure of the program
The Anaphylm NDA is supported by 11 independent clinical studies comprising about 967 total administrations in 411 subjects, with 840 single-dose and 127 repeat-dose exposures. The dataset includes healthy-volunteer PK work, pharmacodynamic readouts (blood pressure, heart rate), as well as more “real-world style” evidence.
2.2 PK/PD versus auto-injectors
Peer-reviewed data and conference presentations (for example at AAAAI) have consistently shown that the sublingual epinephrine film achieves rapid and sustained plasma epinephrine levels in the same ballpark as IM auto-injectors, together with the expected sympathomimetic PD effects. This is the scientific foundation of the “non-invasive alternative to auto-injectors” narrative.
2.3 The OAS challenge study
A key differentiator in the program is the oral allergy syndrome (OAS) study, designed to emulate real-world allergen exposure. In this trial, patients underwent allergen-induced challenge and received Anaphylm in a setting that is closer to actual clinical practice than standard PK/PD work in healthy volunteers. For regulators and clinicians, this is a proof-of-performance layer that confirms the concept beyond pure pharmacokinetics.
3. Regulatory Timeline – From NDA Acceptance to the 2026 CRL
3.1 Acceptance, PDUFA and “no AdComm” signal
The FDA accepted the NDA for Anaphylm in mid-2025 and set a PDUFA goal date of January 31, 2026 for the treatment of Type I allergic reactions, including anaphylaxis. In September 2025, the Agency informed Aquestive that it did not intend to hold an Advisory Committee meeting on the NDA – at the time, that was widely interpreted as a sign of a relatively straightforward review path.
3.2 January 9, 2026 – “Deficiencies that preclude labeling discussions”
On January 9, 2026, Aquestive disclosed that the FDA had identified deficiencies in the NDA that precluded labeling and post-marketing commitment discussions. The letter did not specify the nature of these deficiencies. The FDA also said they did not plan to issue a standard Discipline Review Letter, but might send additional information requests. The official language stressed that no final decision had been made on the NDA and that the review was continuing.
In our earlier Merlintrader piece (“AQST – Anaphylm NDA Deficiencies Deep Dive”) we highlighted exactly this uncertainty: the notification was clearly serious, but there was no direct evidence that efficacy or core safety were in question. We framed three scenarios – from “mostly technical” to “heavy reset” – without trying to guess which one the FDA would ultimately land on.
3.3 January 30, 2026 – Complete Response Letter
The CRL that arrived on January 30, 2026 finally puts structure around those “deficiencies”. According to the company’s February 2 press release, the FDA’s concerns are focused on:
- Human factors validation: instances of difficulty opening the pouch and incorrect film placement, which in the Agency’s view could lead to significant safety issues in the acute anaphylaxis setting if left unaddressed.
- Instructions for use and labeling: the way directions, warnings and packaging text guide the patient through the critical steps of administration.
- One additional PK study: clinical pharmacology requested a single study to characterize the impact of any packaging/label changes on exposure, but explicitly allowed this to be conducted in parallel with the new HF validation work.
Notably, the CRL does not request additional large efficacy or safety trials and does not highlight any CMC issues. The comparability data within the NDA were not challenged in the letter, which is important: the core clinical story and manufacturing backbone appear intact at this stage.
3.4 Company plan and estimated resubmission
Aquestive has already modified pouch opening design, instructions for use, and carton/pouch labeling, and intends to conduct a new HF validation study using the updated materials. In parallel, it will run the requested PK study and address tolerability considerations flagged in the CRL. The company plans to request a Type A meeting to align on the most efficient path and currently guides toward a resubmission in Q3 2026, with a request for rapid review.
4. Why the Market Likes This CRL More Than the January Letter
At first glance it may sound paradoxical: a CRL is a formal rejection of the NDA, yet the stock is up strongly today. The reason is that clarity has value. The January deficiencies letter created a vacuum where every bearish scenario – from deep clinical flaws to structural safety problems or messy CMC – could be projected onto Anaphylm.
The actual CRL, by contrast, narrows the problem set to something that:
- Is clearly defined: how users open the pouch and place the film, the wording and visual design of instructions and labels, and the PK impact of those changes.
- Appears technically solvable with finite, designable work streams (new HF study, new PK study, label refinements).
- Does not reopen the entire clinical development strategy or force a multi-year, large-scale trial.
For a stock that had already been punished on the mere possibility of a worst-case regulatory outcome, this configuration naturally supports a relief rally. The market is effectively saying: “This is a real setback, but it could have been much worse.”
5. Balance Sheet and Runway – Can AQST Afford the Delay?
The CRL inevitably pushes out any potential U.S. launch and revenue ramp. The key question then becomes: does Aquestive have the financial capacity to bridge 2026 and reach the next decision point?
5.1 Cash and losses going into the CRL
According to the company’s Q3 2025 Form 10-Q, cash and cash equivalents stood at $129.1 million as of September 30, 2025, with a quarterly net loss in the mid-teens of millions of dollars. In the January 9, 2026 business update, Aquestive guided to approximately $120 million (unaudited) in cash and equivalents as of December 31, 2025.
This improved cash position relative to mid-2025 has been driven by:
- Underwritten equity offerings in 2024–2025;
- Active use of an at-the-market (ATM) facility;
- A high-yield debt structure, including 13.5% senior secured notes and royalty obligations.
5.2 Management’s message post-CRL
In the CRL press release, the company reiterates that it remains well capitalized and expects to end 2026 with a significant cash balance, while funding the HF and PK work, the resubmission, and pre-launch activities, as well as regulatory work in Europe and Canada. That does not eliminate dilution risk – biotech history says capital raises tend to appear on any strength – but it does suggest that, at today’s burn profile, the company has room to maneuver through the resubmission process without an immediate liquidity crisis.
The underlying trade-off is straightforward: the same cash that was once meant to support a 2026 launch now has to finance an extended pre-launch + remediation phase. If everything goes well, that may still be enough; if there are further delays or new surprises, dilution risk will inevitably increase.
6. Global Strategy – Canada and Europe as an Additional Layer
One important aspect that sometimes gets lost in the U.S.-centric noise is the global roll-out plan. Before the CRL, Aquestive had already begun engaging with regulators in Canada, Europe and the UK. The company reports that the EMA provided positive feedback indicating no additional clinical trials are needed prior to EU submission, which, if confirmed in final filing, would substantially de-risk the European path from a development standpoint.
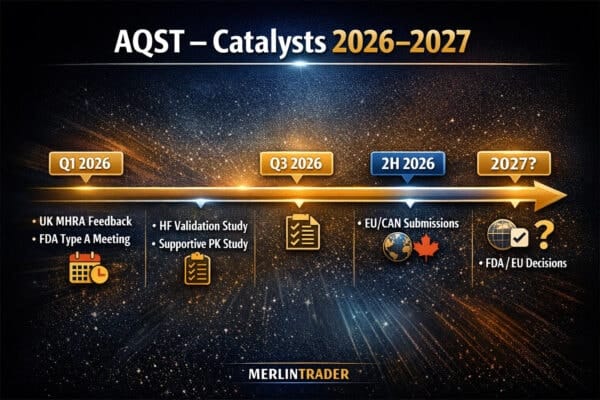
Post-CRL, Aquestive still plans to submit a marketing authorization application in Europe and a New Drug Submission in Canada in the second half of 2026. Feedback from the UK’s MHRA is expected in the first quarter of 2026. If the U.S. pathway converges and at least one major ex-U.S. region opens up, Anaphylm’s value proposition starts to look more like a global platform than a one-country bet.
7. Sentiment, Ownership and the +40–45% Rebound
The price action tells you a lot about expectations. After the January deficiencies letter, AQST traded as if a severe CRL or even a structural failure of the program was a live scenario. Today’s move – roughly in the +40–45% range as the market absorbs the CRL – says that the actual content of the letter was less damaging than feared.
Analyst targets going into the CRL were generally in the low double digits, built on the assumption of a 2026 launch and a straightforward risk/benefit profile. Those targets will now need to be re-cut to reflect the delay and the execution risk around HF/PK, but the fact that the underlying program was not dismantled makes it easier to argue for a longer-term recovery path.
On the insider side, public data in late 2025 showed executives monetizing shares at substantially higher levels. That doesn’t automatically imply “they knew”, but it does remind us that management incentives and retail pain thresholds are not always aligned. In a post-CRL phase that may last well into 2027, the emotional side of the trade will play a big role – both on the upside in relief phases and on the downside during quiet periods.
8. Risk Map – What Could Still Break from Here
A CRL focused on human factors and a single PK study is far from a free pass. Several things can still go wrong:
- The new HF validation study might not fully satisfy the FDA if user behavior in stressful conditions still looks error-prone.
- The PK study linked to packaging/label modifications might show differences that regulators consider clinically relevant, forcing further iteration.
- Timeline assumptions (Type A meeting, study start, enrollment, data readout, resubmission and review) may slip beyond the currently guided Q3 2026 resubmission.
- The funding environment for high-beta biotech could worsen, making any future capital raise more painful.
None of these risks negate the fundamental idea that the CRL is less catastrophic than what the January deficiencies letter had led some investors to fear. But they do underline that AQST is still a high-volatility, binary-outcome story, not a dividend stock.
9. Previous Merlintrader Coverage and Key Primary Sources
Merlintrader articles on AQST (background)
- AQST – Company background and first deep dive
- AQST – Expanded pipeline and balance-sheet analysis
- AQST – Anaphylm PDUFA January 31 and deficiencies letter: first read
Key regulatory and news sources
- Aquestive Therapeutics – CRL press release (Feb 2, 2026) (FDA issues Complete Response Letter for Anaphylm, deficiencies limited to human factors and packaging, one PK study requested, resubmission targeted for Q3 2026).
- Aquestive Therapeutics – Regulatory Development and Business Update (Jan 9, 2026) (FDA deficiencies letter, review ongoing, no final decision, ~120M USD unaudited cash at year-end 2025).
- FDA/EMEA/Health Canada interactions – company updates on global expansion plan and EMA feedback that no additional clinical trials are required prior to EU submission.
- Peer-reviewed PK/PD publications and AAAAI 2024 poster on epinephrine sublingual film vs auto-injector.
- SEC filings, including the Q3 2025 Form 10-Q with detailed cash figures and debt structure.
10. Personal Note – Merlintrader
Back in January, when the only thing we had was a vague deficiencies letter, it was tempting to jump straight to the worst possible conclusion. We chose not to: the whole point of that first deep dive was to separate what was actually written in the 8-K from the fears running through the tape. The CRL that arrived now vindicates that approach in part – the problem is serious, but focused and potentially solvable.
Today’s +40–45% move is the market saying “it could have been much worse”. For anyone looking at AQST now, though, this is just the beginning of a new phase: HF work, PK study, Type A meeting, resubmission, and another review. Months – maybe more than a year – where headlines will be scarce and patience will be tested. The risk/reward can be attractive if Anaphylm ultimately gets through, but it is also very clear that this remains a high-beta, biotech-style waiting room, not a quiet corner of the market.
Catalyst Calendar – AQST (2026–2027)
Aquestive Therapeutics (AQST) – Deep Dive sulla CRL di Anaphylm 2026: Human Factors, PK Study e nuova timeline
Dati rapidi – Situazione attuale dopo la CRL
- Ticker / Exchange: AQST – NASDAQ
- Asset principale: Anaphylm™ (dibutepinephrine sublingual film)
- Indicazione: Reazioni allergiche di tipo I, inclusa anafilassi, in pazienti ≥30 kg
- PDUFA originaria: 31 gennaio 2026 (NDA ora oggetto di CRL datata 30 gennaio 2026)
- Ambito CRL: Human factors (apertura della confezione, posizionamento del film), istruzioni d’uso, etichettatura di pouch e cartone, più uno studio PK legato a queste modifiche – nessun nuovo grande studio di efficacia richiesto, nessun problema CMC evidenziato
- Pacchetto clinico: 11 studi, ~967 somministrazioni totali, 411 soggetti, 840 dosi singole + 127 dosi ripetute
- Situazione cassa: 129,1 M USD di cash ed equivalenti al 30 settembre 2025; guidance a circa 120 M USD (non auditato) al 31 dicembre 2025
- Piano globale: Submission in Europa e Canada previste nella seconda metà del 2026; feedback EMA precedente che non richiede ulteriori studi clinici prima della submission UE
- Andamento odierno: forte rimbalzo (intorno a +40–45% intraday) perché il mercato interpreta la CRL come seria ma risolvibile, rispetto agli scenari peggiori temuti dopo la lettera di gennaio
0. Executive Summary – Da “deficiencies” generiche a una CRL circoscritta
A inizio gennaio 2026 la FDA ha notificato ad Aquestive di aver identificato “deficiencies che impedivano le discussioni su etichetta e impegni post-marketing” per la NDA di Anaphylm. In quel momento, né il mercato né il management sapevano se il problema fosse clinico, di sicurezza, CMC, human factors o altro.
Nel nostro precedente approfondimento su Merlintrader avevamo volutamente mantenuto una posizione prudente ma non apocalittica: abbiamo definito la lettera come evento serio, ma abbiamo anche sottolineato che, senza ulteriori dettagli, non c’erano prove per dire che “il farmaco era morto”. Il titolo era comunque crollato (circa –36% in pre-market), riprezzando la probabilità di ritardo e di una possibile Complete Response Letter.
Il 30 gennaio 2026 la FDA ha effettivamente emesso una Complete Response Letter per Anaphylm. Il punto chiave è cosa la CRL dice e cosa non dice:
- Le deficiencies sono limitate a human factors e somministrazione: difficoltà nell’apertura della bustina e posizionamento scorretto del film nello studio di validazione HF, con potenziali implicazioni di sicurezza se non corrette.
- Una volta sistemati gli aspetti HF, la FDA richiede un solo studio PK per valutare l’impatto delle modifiche; HF e PK possono essere condotti in parallelo.
- La CRL non solleva nuovi problemi CMC e non mette in discussione il pacchetto clinico di efficacia/sicurezza; i dati di comparabilità presentati con la NDA non vengono contestati.
- Non vengono richiesti nuovi grandi trial di efficacia. La società stima di poter ri-presentare la NDA già nel Q3 2026, una volta completati studi HF e PK, e prevede di chiedere una revisione rapida.
In pratica non abbiamo più una “via libera” ma un rinvio strutturato, con problemi che sembrano operativi e circoscritti piuttosto che un rigetto totale della farmacologia di Anaphylm. È questo il motivo per cui oggi il titolo rimbalza: il mercato aveva già prezzato scenari da incubo in cui le “deficiencies” indicavano gravi criticità cliniche o di sicurezza; la CRL effettiva appare invece più vicina a un reset su packaging/uso, con un solo studio PK di supporto.
Il rovescio della medaglia è il fattore tempo. Anche in una CRL “fixable”, rifare la validazione HF, condurre uno studio PK, fare il Type A meeting, ri-presentare nel secondo semestre 2026 e affrontare una nuova review significa mesi e mesi con la storia di nuovo molto binaria e con pochi catalyst intermedi. Dopo l’euforia del rimbalzo, AQST torna a essere un titolo per chi ha pazienza e stomaco, non per chi cerca il “colpo secco”.
1. Chi è Aquestive e perché Anaphylm è così centrale
1.1 Modello di business in breve
Aquestive Therapeutics è una specialty pharma costruita attorno al delivery di molecole complesse tramite film orali e sublinguali. La piattaforma (storicamente “PharmFilm”) ha già portato sul mercato diversi prodotti su licenza in ambito CNS e dipendenze, di cui Aquestive è produttore esclusivo. I ricavi attuali arrivano da queste licenze (royalty, milestone) e il vero driver azionario è la pipeline proprietaria, con Anaphylm in prima linea come possibile prima opzione di epinefrina non invasiva per le emergenze allergiche.
1.2 Cosa vuole essere Anaphylm
Anaphylm è un film sublinguale contenente un pro-farmaco dell’epinefrina per il trattamento delle reazioni allergiche gravi, inclusa l’anafilassi, in pazienti di almeno 30 kg. L’idea è sostituire un auto-injector ingombrante e basato su ago con un film sottile, facile da trasportare e rapido da usare, che si scioglie sotto la lingua senza bisogno di acqua.
Il mercato di riferimento è lo stesso degli auto-injector (EpiPen e simili), ma la value proposition si gioca su:
- eliminazione dell’ago e del gesto “stabbare la coscia”;
- maggiore portabilità (packaging sottile, tipo carta di credito);
- profilo PK progettato per essere comparabile alla somministrazione IM.
2. Pacchetto clinico e PK/PD – Cosa la CRL non mette in discussione
Uno degli elementi più importanti della CRL è ciò che non viene messo in discussione. La società sottolinea che i dati di comparabilità – bracketing, repeat-dose, sostenibilità – che costituiscono l’ossatura del programma clinico di Anaphylm non vengono contestati.
2.1 Dimensione e struttura del programma
La NDA di Anaphylm è supportata da 11 studi clinici indipendenti con circa 967 somministrazioni totali in 411 soggetti, di cui 840 dosi singole e 127 dosi ripetute. Nel pacchetto rientrano studi di farmacocinetica su volontari, dati di farmacodinamica (pressione, frequenza cardiaca) e dati in contesti più “realistici”.
2.2 PK/PD rispetto agli auto-injector
Le pubblicazioni peer-review e i poster presentati a congressi come l’AAAAI mostrano che il film sublinguale di epinefrina raggiunge livelli plasmatici rapidi e sostenuti in linea con quelli degli auto-injector IM, accompagnati dal tipico profilo simpaticomimetico. È questa la base scientifica dell’idea di Anaphylm come alternativa non invasiva agli auto-injector.
2.3 Studio OAS in setting “real-world”
Un elemento distintivo è lo studio su oral allergy syndrome (OAS) con challenge allergenico. Qui i pazienti vengono esposti all’allergene e trattati in un contesto che ricorda molto la pratica clinica reale, andando oltre il classico studio PK/PD su volontari sani. Per regolatori e allergologi questo aggiunge uno strato di evidenza “real-world like” fondamentale per un farmaco di rescue.
3. Timeline regolatoria – Dall’accettazione della NDA alla CRL
3.1 Accettazione, PDUFA e segnale “no AdComm”
La FDA ha accettato la NDA di Anaphylm a metà 2025, con PDUFA goal date al 31 gennaio 2026 per il trattamento delle reazioni allergiche di tipo I, inclusa l’anafilassi. A settembre 2025 l’agenzia ha informato Aquestive di non prevedere un Advisory Committee sulla NDA: all’epoca il mercato lo ha letto come un segnale di percorso regolatorio relativamente lineare.
3.2 9 gennaio 2026 – Lettera di “deficiencies che impediscono le discussioni sull’etichetta”
Il 9 gennaio 2026 Aquestive comunica che la FDA ha identificato deficiencies nella NDA che impediscono le discussioni su etichetta e impegni post-marketing. La lettera non specifica la natura di tali deficiencies. La FDA chiarisce anche di non voler emettere una classica Discipline Review Letter e sottolinea che non è stata presa alcuna decisione finale sulla NDA.
Nel pezzo precedente su Merlintrader (“AQST – Anaphylm NDA Deficiencies Deep Dive”) avevamo proprio insistito su questo punto: la lettera era chiaramente un segnale di allarme, ma senza dettagli non era corretto dedurre automaticamente problemi strutturali di efficacia o sicurezza. Abbiamo impostato tre scenari – da “problemi tecnici gestibili” a “reset pesante del programma” – senza pretendere di indovinare quale sarebbe stato l’esito finale.
3.3 30 gennaio 2026 – Arriva la Complete Response Letter
La CRL del 30 gennaio 2026 porta finalmente chiarezza su quali siano queste “deficiencies”. Come si legge nel comunicato del 2 febbraio, le criticità individuate dalla FDA riguardano:
- La validazione di human factors: difficoltà ad aprire la bustina e posizionamento scorretto del film, che in uno scenario di anafilassi potrebbero tradursi in problemi di sicurezza se non affrontati.
- Le istruzioni d’uso e l’etichettatura (testo, layout, avvertenze su bustina e cartone).
- Un singolo studio PK legato alle modifiche di packaging/label, richiesto da clinical pharmacology per valutare l’effetto di tali modifiche sull’esposizione.
È altrettanto importante ciò che la CRL non chiede: nessun nuovo grande studio di efficacia o sicurezza, nessuna issue CMC evidenziata, nessuna messa in discussione esplicita dei dati di comparabilità già nel file. Questo non equivale a “tutto ok”, ma restringe il campo rispetto agli scenari peggiori temuti a gennaio.
3.4 Piano aziendale e stima di resubmission
Aquestive ha già modificato il design della bustina, le istruzioni d’uso e il labeling di bustina e cartone, e intende condurre un nuovo studio di validazione HF con questi aggiornamenti. In parallelo pianifica il nuovo studio PK richiesto e un affinamento degli aspetti di tollerabilità citati nella CRL. La società prevede di chiedere un Type A meeting alla FDA per concordare il percorso più efficiente e oggi indica come obiettivo una resubmission nel Q3 2026, con richiesta di revisione rapida.
4. Perché il mercato interpreta positivamente questa CRL rispetto alla lettera di gennaio
Sulla carta può sembrare strano: una CRL è pur sempre un rigetto formale della NDA, eppure il titolo oggi è in forte rialzo. La risposta è che la chiarezza ha un valore. La lettera di gennaio apriva un buco informativo in cui ogni scenario ribassista – dal disastro clinico al problema di sicurezza grave o al caos CMC – poteva essere proiettato su Anaphylm.
La CRL reale, invece, restringe il campo a qualcosa che:
- È chiaramente definito: apertura confezione, posizionamento del film, testi di etichetta e istruzioni, più un singolo studio PK legato a queste modifiche.
- Sembra tecnicamente risolvibile con workstream finiti e progettabili (nuovo HF study, nuovo PK, raffinamento di IFU/label).
- Non richiede di riaprire da zero il percorso clinico con grandi studi aggiuntivi.
Per un titolo che era già stato “punito” sulla sola possibilità dello scenario peggiore, questa configurazione giustifica un relief rally. Il mercato, semplificando, sta dicendo: “Il colpo è arrivato, ma poteva essere molto peggio”.
5. Situazione finanziaria e runway – AQST può permettersi il ritardo?
La CRL sposta inevitabilmente più avanti nel tempo qualsiasi ipotesi di lancio USA e di ramp up dei ricavi. La domanda diventa: Aquestive ha le risorse per arrivare dall’altra parte del ponte?
5.1 Cassa e perdite all’ingresso della CRL
Nel Form 10-Q del Q3 2025 la società riporta 129,1 milioni di dollari di cassa ed equivalenti al 30 settembre 2025, con una perdita trimestrale nell’ordine di decine di milioni. Nel business update del 9 gennaio 2026, Aquestive indica circa 120 milioni di dollari (dato non auditato) al 31 dicembre 2025.
Il rafforzamento rispetto a metà 2025 è stato ottenuto grazie a:
- aumenti di capitale underwritten tra 2024 e 2025;
- uso attivo di una linea ATM (at-the-market);
- una struttura di debito costosa, con senior secured notes al 13,5% e accordi di royalty.
5.2 Messaggio del management dopo la CRL
Nel comunicato sulla CRL la società ribadisce di sentirsi ben capitalizzata e di aspettarsi di chiudere il 2026 con una cassa significativa, pur finanziando studi HF e PK, resubmission, attività di pre-lancio e iter regolatori in Europa e Canada. Questo non azzera il rischio di diluizione – nella storia del biotech i rafforzamenti di capitale arrivano quasi sempre nei momenti di forza – ma suggerisce che, ai livelli di burn attuali, c’è spazio per attraversare il processo di resubmission senza andare subito in emergenza liquidità.
Il trade-off è chiaro: la stessa cassa che prima serviva a sostenere un lancio 2026 ora deve finanziare una lunga fase di pre-lancio + remediation. Se tutto va liscio, potrebbe bastare; se i tempi si allungano o spuntano nuovi problemi, il rischio di diluizione aumenta.
6. Strategia globale – Canada e UE come layer aggiuntivo
Un aspetto spesso sottovalutato nel rumore USA-centrico è il piano globale. Già prima della CRL Aquestive aveva aperto canali con Canada, Europa e Regno Unito. La società riporta che l’EMA ha fornito un feedback positivo, indicando che non sono necessari ulteriori studi clinici prima della submission europea.
Dopo la CRL, il piano non cambia: Aquestive conferma l’intenzione di presentare domanda di autorizzazione all’immissione in commercio in Europa e New Drug Submission in Canada nella seconda metà del 2026, mentre i feedback da parte della MHRA britannica sono attesi nel primo trimestre 2026. Se il percorso USA si riallinea e almeno una grande regione ex-USA si apre, Anaphylm diventa sempre più un progetto globale e non solo una scommessa sulla FDA.
7. Sentiment, azionariato e rimbalzo del +40–45%
Il price action racconta parecchio. Dopo la lettera di deficiencies di gennaio, AQST ha trattato come se una CRL pesante o addirittura un fallimento strutturale del programma fosse uno scenario concreto. Il movimento di oggi – attorno a +40–45% mentre il mercato assimila la CRL – indica che il contenuto reale della lettera è meno distruttivo di quanto scontato.
I target price degli analisti prima della CRL erano in genere nella bassa doppia cifra, basati sull’ipotesi di lancio nel 2026 e su un profilo rischio/beneficio piuttosto lineare. Ora quei target andranno rivisti alla luce del ritardo e dei rischi esecutivi su HF/PK, ma il fatto che il programma non sia stato smontato rende più facile immaginare un percorso di recupero nel medio periodo.
Sul fronte insider, i dati di fine 2025 mostrano vendite da parte di executive a livelli di prezzo ben superiori a quelli attuali. Non è di per sé una prova di “sapere in anticipo”, ma ricorda che incentivi del management e resistenza emotiva del retail non sono sempre allineati. In una fase post-CRL che potrebbe durare fino al 2027, la componente psicologica del trade sarà enorme – sia nei momenti di euforia che in quelli di noia e drawdown.
8. Rischi principali – Cosa può ancora andare storto
Una CRL centrata su human factors e un singolo studio PK è certamente meglio di scenari ultra-bearish, ma non è un lasciapassare automatico. Alcuni punti critici:
- Il nuovo studio di validazione HF potrebbe non soddisfare pienamente la FDA se, in condizioni simulate di emergenza, gli errori di utilizzo restano troppo frequenti.
- Lo studio PK legato alle modifiche di packaging/label potrebbe mostrare differenze che la FDA giudica clinicamente rilevanti, imponendo ulteriori iterazioni.
- Le tempistiche (Type A meeting, avvio studi, enrollment, readout, resubmission, nuova review) potrebbero spostare la data di resubmission oltre il Q3 2026 oggi stimato.
- Il contesto macro per il biotech high-beta potrebbe peggiorare, rendendo eventuali aumenti di capitale più diluitivi.
Nulla di tutto questo cancella il fatto che la CRL sia meno devastante delle paure di gennaio, ma conferma che AQST resta una scommessa ad alta volatilità e fortemente binaria, non un titolo “da cassettista tranquillo”.
9. Articoli Merlintrader e fonti primarie
Articoli Merlintrader su AQST (background)
- AQST – Panoramica iniziale su azienda e piattaforma
- AQST – Analisi estesa di pipeline e bilancio
- AQST – PDUFA 31 gennaio e lettera di deficiencies: prima lettura
Principali fonti regolatorie e news
- Comunicato Aquestive – CRL su Anaphylm (2 febbraio 2026) (Complete Response Letter con criticità limitate a human factors/packaging, richiesta di uno studio PK e guida a resubmission nel Q3 2026).
- Comunicato Aquestive – Regulatory Development e business update (9 gennaio 2026) (lettera di deficiencies, review in corso, nessuna decisione finale, indicazione di ~120 M USD di cassa non auditata a fine 2025).
- Interazioni regolatorie in UE/Canada – aggiornamenti societari sul piano di espansione globale e sul feedback EMA di assenza di necessità di nuovi trial prima della submission.
- Pubblicazioni peer-review e poster AAAAI 2024 su PK/PD del film sublinguale di epinefrina vs auto-injector.
- Filing SEC, inclusi i Form 10-Q con i dati di cassa e la struttura del debito.
10. Nota personale – Merlintrader
A gennaio, con in mano solo una lettera di deficiencies generica, era fin troppo facile lasciarsi trascinare dallo scenario peggiore. Abbiamo scelto di non farlo: l’obiettivo di quel primo deep dive era proprio separare ciò che c’era scritto nero su bianco nell’8-K dalle paure più estreme del mercato. La CRL di oggi in parte conferma quell’approccio – il colpo è arrivato, ma è focalizzato e potenzialmente risolvibile.
Il +40–45% di oggi è il mercato che dice “poteva andare peggio”. Per chi guarda AQST adesso, però, questo è solo l’inizio di una nuova fase: studi HF e PK da fare, Type A meeting, resubmission, un’altra review. Mesi – forse più di un anno – in cui le notizie vere saranno poche e la pazienza verrà testata. Il profilo rischio/rendimento può essere interessante se Anaphylm alla fine passa, ma è chiaro che resta una storia per stomaci forti, non per chi vuole dormire sonni tranquilli.
Calendario Catalyst – AQST (2026–2027)
RELATED POSTS
View all



