DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
Merlintrader trading Blog – Single-ticker deep dive
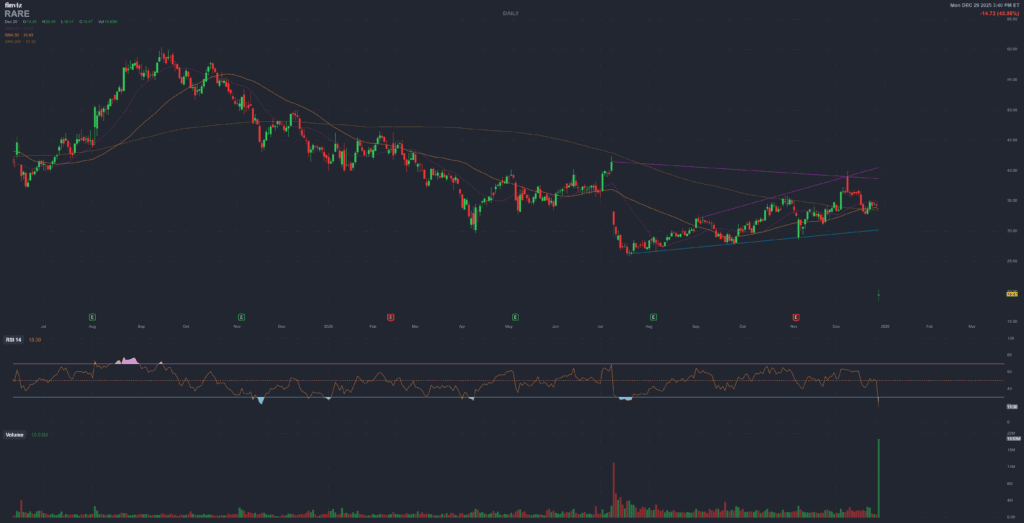
Ultragenyx (RARE) – UX143 Phase 3 failure in OI, what is left on the table?
The long-awaited Phase 3 ORBIT and COSMIC results for setrusumab (UX143) in osteogenesis imperfecta
arrived with the worst possible headline: no statistical benefit on fracture rate and a one-day
collapse of more than forty percent in Ultragenyx’s share price. Under the surface, though, the
picture is more nuanced: strong bone mineral density gains, an intact commercial base and a pipeline
that now has to carry the story without UX143.
Data and prices: intraday snapshot on 29 December 2025, based on public sources. Figures can move quickly
and should be re-checked on primary sources before any decision.
Ticker / exchange
RARE – Nasdaq
Ultragenyx Pharmaceutical Inc.
Share price (approx.)
$19–20
Down about 44 percent on the day (from roughly $34), near the lowest levels since early listing.
Market cap
~$3.3 billion
Post-crash, according to major quote providers.
2025 revenue guidance
$640–670 million
Crysvita $460–480M, Dojolvi $90–100M, reaffirmed with Q3 2025 results.
Cash (Q3 2025)
$447M + $400M
$447M cash, equivalents and securities at 30 Sep 2025, plus $400M from Crysvita royalty sale.
Net cash used in ops
$91M (Q3)
$366M used in operations over the first nine months of 2025, highlighting a heavy burn.
News of the day – UX143 Phase 3 failure
On 29 December 2025 Ultragenyx announced that the Phase 3 ORBIT and COSMIC
studies of setrusumab (UX143) in osteogenesis imperfecta did not meet their primary endpoints
of reducing annualized clinical fracture rate versus placebo (ORBIT) or bisphosphonates (COSMIC).
Both trials, however, showed statistically significant and substantial improvements in bone
mineral density at key skeletal sites and no new safety signals. In response, the company stated
it will conduct further analyses of bone health and clinical endpoints, discuss the data with
regulators and implement significant expense reductions to refocus on other late-stage programs.
This is a huge setback for the OI franchise and for Mereo’s partner economics, but it does not erase
Ultragenyx’s commercial base (Crysvita, Dojolvi, Mepsevii, Evkeeza ex-US) nor the rest of the pipeline
(GTX-102, DTX401, DTX301, UX701, UX111). The key question is how much of the current valuation can be
supported by those assets once UX143 is either re-scoped or effectively written down.
1. Executive summary
Ultragenyx enters the end of 2025 in one of the hardest spots a rare-disease company can face: its most promising late-stage asset, setrusumab (UX143) for osteogenesis imperfecta, has just failed two pivotal Phase 3 trials on their primary fracture endpoints, wiping out roughly forty percent of the market value in a single session.
The Phase 3 ORBIT and COSMIC studies delivered a mixed picture. On the one hand, neither study achieved statistically significant reductions in fracture rate versus placebo or standard-of-care bisphosphonates. On the other hand, both showed robust, highly significant improvements in bone mineral density and a tolerable safety profile – essentially confirming the Phase 2 bone biology signal, but failing to convert it into a fracture benefit strong enough for a clean label.
Financially, Ultragenyx still looks like a “mini-platform” rather than a single-asset story. In the third quarter of 2025 the company reported $160 million in revenue (+15 percent year-on-year), driven primarily by Crysvita and Dojolvi, and held $447 million in cash, equivalents and marketable securities as of September 30, bolstered by a recent $400 million royalty sale on part of its Crysvita economics. The downside is that net cash used in operations reached $366 million over the first nine months of 2025, implying a very heavy burn even before any restructuring.
On the Street side, the reaction is not one of wholesale abandonment. Several banks have reiterated Overweight / Outperform ratings with targets in the roughly $55–80 range and frame UX143 as a serious but not fatal setback, given the rest of the pipeline and the commercial base. That said, analyst optimism does not remove the reality that one of the most visible near-term growth drivers has been badly damaged.
In short: UX143’s failure in OI cuts deeply into the “transformational” part of the Ultragenyx story, but
does not leave the company without assets. Crysvita, Dojolvi, Mepsevii and Evkeeza still provide a growing
revenue base; GTX-102, DTX401, DTX301 and UX701 form a meaningful late-stage pipeline; the balance sheet
has been reinforced just ahead of this read-out. The open question is whether the company can resize its
cost base and rebuild trust fast enough to turn the current panic into a long, slow recovery rather than
a structural value trap.
2. What happened today – ORBIT and COSMIC in plain language
2.1 Headline results
- Design: ORBIT and COSMIC are Phase 3 trials of setrusumab (UX143) in osteogenesis imperfecta (OI), a brittle-bone disease with high fracture burden and limited treatment options.
- Primary endpoints: reduction in annualized clinical fracture rate vs placebo (ORBIT) and vs bisphosphonates (COSMIC).
- Outcome: neither study achieved statistical significance on the primary endpoints, despite positive Phase 2 data and strong expectations from management and investors.
2.2 Secondary endpoints and bone biology signal
- Both studies showed statistically significant and substantial improvements in bone mineral density (BMD) at the lumbar spine and other key sites versus their comparators, consistent with prior Phase 2 data.
- Safety profile remained broadly consistent with earlier experience, with no new major safety signals reported in the company’s summary.
- In COSMIC, pediatric patients had higher baseline fracture rates and showed a numerical reduction in fractures versus bisphosphonates, but again without statistical significance on the predefined primary endpoint.
2.3 Immediate company response
- Ultragenyx stated it will perform deeper analyses of the data, including other bone health and functional endpoints, and will discuss the totality of evidence with regulators to determine whether any path remains for UX143 in specific OI subgroups.
- At the same time, management announced plans to review operations and define significant expense reductions, effectively signalling that UX143 spend will be curtailed and resources reallocated to other programs.
- The stock reaction was brutal: RARE fell about 43–45 percent intraday, trading near $19–20 and at or below prior 52-week lows.
For OI patients and clinicians this is more than a stock story: a potentially disease-modifying antibody
has failed to deliver the fracture benefit regulators want to see, despite clear improvements in bone
density. It is a reminder that in rare disease, biology, statistics and regulatory standards do not
always align the way investors would like.
3. 2025 timeline – from optimism to fracture failure
- February 2025: Full-year 2024 results: revenue reaches $560M, with Crysvita at $410M and Dojolvi at $88M. Guidance for 2025 total revenue is set at $640–670M. UX143 Phase 3 studies are highlighted as key upcoming catalysts.
- July 2025: Ultragenyx and Mereo announce that the ORBIT study is progressing to final analysis after interim assessments, reinforcing market confidence that the Phase 3 OI program is on track for a year-end readout.
- July–August 2025: The company completes enrollment in the Phase 3 ASPIRE study for GTX-102 in Angelman syndrome and prepares the Aurora trial for broader genotypes and age groups, signalling a strong second pillar in CNS.
- Q2–Q3 2025: Financial updates show continued revenue growth but also heavy operating losses. Q3 revenue reaches $160M (+15 percent Y/Y), Crysvita $112M, Dojolvi $24M and Evkeeza $17M in Ultragenyx territories. Cash stands at $447M, with a $400M Crysvita royalty monetisation deal further bolstering the balance sheet.
- October 2025: First subject dosed in Aurora (GTX-102) and commercial roll-out of Evkeeza expands in Europe, including Italy, underscoring Ultragenyx’s multi-product commercial infrastructure.
- November 2025: Q3 earnings call reiterates 2025 revenue guidance and emphasises “multiple late-stage data read-outs, multiple regulatory submissions and multiple launches” over the next 12–18 months, with OI data framed as a key element of that wave.
- 29 December 2025: ORBIT and COSMIC Phase 3 results for UX143 in OI are announced: no statistically significant reduction in fracture rates vs comparators, although BMD improves robustly. Ultragenyx signals expense reductions and a strategic reassessment of the program. The stock suffers a historic one-day drawdown of over 40 percent.
In twelve months the market has gone from viewing UX143 as a likely next commercial pillar alongside
Crysvita and Dojolvi to treating it as a damaged asset. The rest of the timeline – particularly GTX-102,
DTX401, DTX301 and UX701 – now matters much more than it did a week ago.
4. Pipeline and remaining catalysts
4.1 Commercial base – four approved products
- Crysvita (burosumab): antibody for X-linked hypophosphatemia (XLH) and tumor-induced osteomalacia (TIO), co-developed with Kyowa Kirin. 2024 revenue reached about $410M and 2025 guidance stands at roughly $460–480M in Ultragenyx territories.
- Dojolvi (triheptanoin): oral therapy for long-chain fatty acid oxidation disorders (LC-FAOD), with 2024 revenue around $88M and 2025 guidance of $90–100M.
- Mepsevii (vestronidase alfa): enzyme replacement for MPS VII (Sly syndrome); smaller but strategically important ultra-rare franchise.
- Evkeeza (evinacumab): antibody for homozygous familial hypercholesterolemia (HoFH), with rights outside the US acquired from Regeneron. Evkeeza generated about $17M revenue in Q3 2025 and is being launched in selected international markets, including Italy.
4.2 UX143 (setrusumab) – where can it still matter?
- Despite failing primary fracture endpoints, UX143 showed strong, significant BMD improvements and a clean safety profile.
- Ultragenyx and Mereo intend to explore subgroup analyses, particularly in pediatric OI with higher baseline fracture rates, and to discuss these data with regulators.
- Realistically, the probability of a broad OI label has sharply decreased. However, a narrower indication based on bone health surrogates, or a more regional/limited approach, remains a possibility until analyses and regulatory feedback are complete.
- From a valuation standpoint, most of the previous “blue sky” for UX143 should now be treated as optionality, not as a central pillar.
4.3 Key late-stage programs beyond UX143
GTX-102 (Angelman syndrome)
- Antisense oligonucleotide (ASO) for Angelman syndrome, designed to increase expression of the paternal UBE3A allele.
- Phase 3 ASPIRE study has completed enrollment, and Aurora – an additional study covering broader genotypes and age groups – has started dosing.
- This program now becomes one of the most important future catalysts in Ultragenyx’s CNS portfolio.
DTX401 and DTX301 (gene therapies)
- DTX401 – AAV gene therapy for glycogen storage disease type Ia (GSDIa); Ultragenyx initiated a rolling BLA submission to the FDA during 2025, suggesting a potential regulatory decision in 2026–2027.
- DTX301 – gene therapy for ornithine transcarbamylase (OTC) deficiency, progressing towards registrational development.
UX701 (Wilson disease gene therapy)
- UX701 is an AAV gene therapy in the pivotal Cyprus2+ Phase 1/2/3 study for Wilson disease.
- Early-stage updates have shown encouraging trends, and further data from the ongoing study will act as another medium-term catalyst.
UX111 and other programs
- UX111 – gene therapy for Sanfilippo syndrome (MPS IIIA) – received a Complete Response Letter (CRL) from the FDA earlier in 2025, but Ultragenyx has committed to resubmission after addressing agency feedback.
- Additional earlier-stage programs and lifecycle work around Crysvita, Dojolvi and Evkeeza provide secondary, but non-trivial, catalyst potential.
Taken together, the pipeline still contains multiple shots on goal. UX143 moves from “likely growth driver”
to “question mark with residual value”; GTX-102, DTX401/301 and UX701 step up as the new core of the
late-stage narrative, supported by a commercial base that – if managed carefully – can finance part of
the journey.
5. Financial snapshot and dilution risk
5.1 Revenue and profitability
- Total revenue Q3 2025: about $160M, up 15 percent year-on-year.
- Crysvita revenue: $112M; Dojolvi: $24M; Evkeeza: $17M in the quarter.
- 2024 revenue: roughly $560M; 2025 guidance reaffirmed at $640–670M.
- Net loss Q3 2025: roughly $180M (EPS around −1.8), with total operating expenses above $330M, reflecting heavy R&D and pre-launch manufacturing spend.
5.2 Cash, runway and royalty financing
- Cash, cash equivalents and marketable securities: about $447M as of 30 September 2025.
- Ultragenyx monetised 25 percent of its North American Crysvita economics for $400M upfront from an institutional investor, with a capped multiple on royalties, adding substantial non-dilutive cash.
- Net cash used in operations: roughly $91M in Q3; about $366M across the first nine months of 2025.
A simple, rough extrapolation of the burn would suggest that the pre-UX143 failure balance sheet could
fund roughly two years of operations. The announced expense reductions should extend that, but the
exact magnitude will depend on how aggressively OI costs and other R&D programs are trimmed.
5.3 Dilution and funding risk after UX143
- Even with a reinforced cash position, Ultragenyx is not a self-funding business: operating losses are large and multiple late-stage programs require substantial capital to reach approval and launch.
- The UX143 failure removes a potentially meaningful near-term revenue contributor, increasing the relative importance of GTX-102, DTX401/301 and UX701 for future cash flows.
- Management’s commitment to significant expense reductions suggests a move to preserve runway and avoid emergency financing at depressed prices, but equity issuance or further royalty deals remain likely at some point in the next 2–3 years if the company continues to pursue its full pipeline.
- Some analysts have highlighted the improved cash position and royalty monetisation as positives, while also acknowledging that profitability is not in sight in the short term.
6. Market reaction and sentiment
6.1 One of the worst days in Ultragenyx’s history
- Ultragenyx stock dropped around 43–45 percent on the UX143 news, trading near $19–20 and approaching post-IPO lows.
- Several outlets noted that the sell-off is among the steepest since the company went public, and that Mereo BioPharma, Ultragenyx’s partner, suffered an even more extreme collapse.
6.2 Street takes – not a unanimous abandonment
- A number of banks reiterated Overweight / Outperform ratings and targets well above current trading levels, framing the setback as serious but not thesis-breaking given the broader pipeline and commercial platform.
- Their arguments focus on the durability of Crysvita/Dojolvi/Evkeeza sales and the upcoming data from GTX-102 and the gene therapy programs.
- However, price targets do not change the fact that UX143 was a major part of previous long-term valuation models and that confidence has been shaken.
6.3 Retail sentiment (Stocktwits, Reddit, X)
- Initial reaction on social platforms is a predictable mix of shock and anger: many posts focus on the magnitude of the drop, the contrast with prior Phase 2 success, and accusations that management was “overconfident”.
- A subset of traders are already framing the move as an opportunity, pointing to:
- the strong BMD signal and lack of safety surprises,
- the still-growing Crysvita/Dojolvi franchises,
- and Street targets that remain far above the new share price.
- At the same time, familiar social myths reappear quickly: that “shorts knew”, that “analysts will pump it back” or that “fracture endpoints don’t matter because BMD is enough”, all of which need to be handled with caution.
The important message is not that “everyone is wrong” or “everyone is right”, but that the composition of
the holder base changes. A large one-day drawdown tends to flush out weak hands and bring in event-driven
traders. What matters next is whether upcoming catalysts and execution can attract longer-term,
fundamentals-driven capital back into the name.
7. Scenario map (illustrative only)
Base case – refocus and slow repair
UX143 does not become a broad commercial success, but a limited path (for specific OI subgroups or regions) remains possible after further analyses. Management executes on announced expense reductions, prioritises GTX-102, DTX401/301 and UX701, and maintains Crysvita/Dojolvi/Evkeeza growth broadly in line with guidance. The stock trades more on the balance between cash runway and pipeline progress than on UX143 alone, with volatility remaining high but the worst of the panic behind.
Bull case – UX143 salvage plus pipeline delivery
Post-hoc analyses and discussions with regulators yield a viable niche path for UX143, perhaps focused on severe pediatric OI with BMD and clinical benefit strong enough for meaningful adoption. In parallel, GTX-102 generates compelling data in Angelman, DTX401 gains regulatory approval and UX701 continues to impress in Wilson disease. Revenue grows towards and beyond the upper end of guidance, and the company is able to finance expansion largely through internal cash flow plus selective, non-punitive deals.
Bear case – UX143 write-off and funding squeeze
UX143 is effectively written off as a commercial asset; subgroup analyses fail to produce a convincing regulatory path. One or more of the other late-stage programs disappoint, while operating costs prove difficult to reduce fast enough. In this setting, additional financing is required under pressure, leading to heavy dilution, multiple compression and a long-lasting overhang on the equity.
These scenarios are qualitative frames, not probabilities or recommendations. They are meant to make it
easier to think in terms of ranges and moving parts – fracture data, other pivotal read-outs, cash burn,
financing options – rather than a single yes/no outcome.
8. Key risks and red flags
Clinical risk across the pipeline
The UX143 failure is a reminder that even apparently strong Phase 2 signals can wash out at Phase 3. GTX-102, DTX401/301, UX701 and UX111 all carry significant clinical and regulatory risk; another high-profile disappointment would meaningfully damage the investment case.
High structural burn
Operating expenses above $300M per quarter and nine-month operating cash use of roughly $366M indicate a business model that is still far from breakeven. Expense reductions can help, but will need to be balanced against the need to keep late-stage programs moving at pace.
Financing and dilution
Even with $447M in cash and $400M from royalty monetisation, Ultragenyx is likely to require additional capital within a few years if it continues to pursue a broad pipeline. The timing and structure of such financings (equity, royalty, debt) will materially affect existing shareholders.
Competition and payer dynamics
In rare disease and gene therapy, the competitive and pricing landscapes are evolving quickly. Future approvals by other companies in Angelman, Wilson disease, GSDIa or other indications could compress peak sales assumptions for Ultragenyx’s assets or pressure pricing and reimbursement.
9. Outlook – is a comeback possible?
A forty-plus percent drawdown on a Phase 3 failure is never “just a buying opportunity”. It reflects a genuine loss of expected future cash flows and a hit to management credibility. At the same time, the Ultragenyx story is not a one-asset biotech imploding to cash; it is a commercial-stage rare-disease company with a diversified portfolio of marketed products and late-stage programs.
In the short term, the key variables are:
- the depth and credibility of expense reductions and reprioritisation after UX143,
- the pace and quality of progress in GTX-102, DTX401/301 and UX701,
- whether any meaningful, narrower-scope path remains for UX143 based on BMD and clinical subgroups,
- and the timing/terms of any future financing transactions.
From an educational perspective, the RARE case is a clear example of why catalyst trading around pivotal data needs a framework that goes beyond “Phase 2 looked good” and “Street is bullish”. The company still has levers it can pull to attempt a long, slow recovery; whether that translates into value creation for shareholders will depend on execution, discipline on spending and some help from the remaining pipeline.
10. “My tale” – personal angle (to be filled by the author)
Where RARE fits (or does not fit) in a real biotech strategy
Space reserved for your personal view: how a name like Ultragenyx fits – or does not fit – the RunUp /
catalyst logic. For example:
– whether after a crash like this you consider it only for technical bounces,
– whether you still see a role in a basket of “platform rare-disease names” with real revenue,
– or whether the risk/reward has worsened too much versus other opportunities in the space.
– whether after a crash like this you consider it only for technical bounces,
– whether you still see a role in a basket of “platform rare-disease names” with real revenue,
– or whether the risk/reward has worsened too much versus other opportunities in the space.
11. Sources and further reading
Key sources used for this report include official Ultragenyx and Mereo press releases, SEC filings, quarterly results and independent news/analyst coverage. Readers should always re-check the latest primary documents before acting on any information.
This report is an educational and editorial overview based solely on publicly available information.
It does not constitute investment advice, an offer or solicitation to buy or sell any security, or a
personalised recommendation. Data, dates and interpretations may contain errors or become outdated.
Readers should perform their own due diligence, cross-check primary sources (company filings, official
press releases, regulatory documents) and, where appropriate, consult regulated financial professionals
before making any decision.
Merlintrader trading Blog – Approfondimento singolo titolo
Ultragenyx (RARE) – Fallimento di UX143 in Fase 3 OI, cosa resta davvero in mano?
I risultati di Fase 3 ORBIT e COSMIC per setrusumab (UX143) nell’osteogenesi imperfetta sono arrivati
con il titolo peggiore possibile: nessun beneficio statisticamente significativo sul tasso di fratture
e crollo in borsa di oltre il quaranta per cento in una sola seduta. Sotto la superficie, però, il quadro
è più sfumato: miglioramenti robusti della densità ossea, base commerciale attiva e una pipeline che ora
deve reggere la storia senza UX143.
Dati e prezzi: fotografia intraday al 29 dicembre 2025, basata su fonti pubbliche. Le cifre possono
muoversi rapidamente e vanno sempre ricontrollate sulle fonti primarie prima di qualsiasi decisione.
Ticker / mercato
RARE – Nasdaq
Ultragenyx Pharmaceutical Inc.
Prezzo azione (circa)
19–20 USD
Circa −44 percento nella seduta (da ~34 USD), vicino ai livelli più bassi da anni.
Market cap
~3,3 miliardi USD
Valutazione post-crash secondo i principali provider di dati.
Guidance ricavi 2025
640–670 mln USD
Crysvita 460–480M, Dojolvi 90–100M, guidance confermata con i risultati Q3 2025.
Cassa (Q3 2025)
447M + 400M
447M USD tra cassa, equivalenti e titoli al 30 settembre 2025, più 400M da monetizzazione royalty Crysvita.
Cash burn operativo
91M (Q3)
366M USD di cassa utilizzata nelle operazioni nei primi 9 mesi 2025, segnale di burn elevato.
News del giorno – fallimento UX143 in Fase 3
Il 29 dicembre 2025 Ultragenyx ha comunicato che gli studi di Fase 3 ORBIT e
COSMIC su setrusumab (UX143) nell’osteogenesi imperfetta non hanno raggiunto gli endpoint primari
di riduzione del tasso annualizzato di fratture rispetto a placebo (ORBIT) o bisfosfonati (COSMIC).
Entrambi gli studi hanno però mostrato miglioramenti significativi e sostanziali della densità
minerale ossea e nessun nuovo segnale rilevante di sicurezza. Ultragenyx ha dichiarato che effettuerà
ulteriori analisi sugli endpoint di salute ossea e clinici, discuterà i dati con i regolatori e
implementerà forti riduzioni di spesa per rifocalizzarsi sugli altri programmi avanzati della pipeline.
Per la storia OI e per Mereo partner è un colpo pesante, ma non azzera la base commerciale di
Ultragenyx (Crysvita, Dojolvi, Mepsevii, Evkeeza fuori USA) né il resto della pipeline (GTX-102,
DTX401, DTX301, UX701, UX111). La domanda vera diventa quanta parte della capitalizzazione attuale
può essere sostenuta da questi asset ora che UX143 passa da “pilastro” a optionalità.
1. Executive summary
Ultragenyx chiude il 2025 in una delle situazioni più difficili per una rare-disease company: l’asset avanzato più visibile, setrusumab (UX143) per osteogenesi imperfetta, ha appena fallito due studi di Fase 3 sui primary endpoint di fratture, cancellando in poche ore oltre il quaranta percento della market cap.
ORBIT e COSMIC hanno offerto un quadro misto. Da un lato, nessuno dei due studi ha ottenuto una riduzione statisticamente significativa del tasso di fratture rispetto ai comparatori, nonostante la Fase 2 positiva e le aspettative elevate. Dall’altro, entrambi hanno mostrato miglioramenti robusti della densità minerale ossea e un profilo di sicurezza coerente con l’esperienza precedente: la biologia ossea risponde, ma l’effetto sugli eventi clinici non ha centrato il livello richiesto per un’etichetta pulita.
Dal punto di vista economico, Ultragenyx non è una one-shot biotech: nel Q3 2025 ha riportato circa 160M USD di ricavi (+15 percento anno su anno), trainati da Crysvita e Dojolvi, e disponeva di circa 447M USD di cassa, equivalenti e titoli al 30 settembre, rafforzati da 400M USD incassati via monetizzazione di una quota delle royalty Crysvita. Il rovescio della medaglia è un cash burn operativo di circa 366M USD sui primi 9 mesi, con Opex trimestrali oltre i 300M USD: un modello ancora molto lontano dal break-even.
Dal lato Street, la reazione non è di abbandono totale. Diverse case hanno ribadito rating positivi con target ben superiori ai prezzi attuali e inquadrano UX143 come un colpo duro ma non fatale, alla luce della base commerciale e della pipeline residua. Detto questo, l’ottimismo degli analisti non cancella il fatto che uno dei driver di crescita più visibili è stato seriamente compromesso.
In sintesi: il fallimento di UX143 taglia in profondità la parte “trasformazionale” della storia
Ultragenyx, ma non lascia la società senza asset. Crysvita, Dojolvi, Mepsevii ed Evkeeza continuano a
costituire una base di ricavi in crescita; GTX-102, DTX401/301 e UX701 formano un nucleo avanzato di
pipeline; il bilancio è stato rafforzato proprio in vista di queste milestone. La domanda aperta è se la
società saprà ridimensionare i costi e ricostruire fiducia abbastanza in fretta da trasformare il panico
attuale in una lenta rimonta, invece che in una trappola di valore strutturale.
2. Cosa è successo oggi – ORBIT e COSMIC in parole semplici
2.1 Risultato in breve
- Design: ORBIT e COSMIC sono studi di Fase 3 su setrusumab (UX143) nell’osteogenesi imperfetta (OI), malattia rara delle ossa con forte burden di fratture e poche opzioni terapeutiche.
- Endpoint primari: riduzione del tasso annualizzato di fratture rispetto a placebo (ORBIT) e rispetto a bisfosfonati (COSMIC).
- Outcome: nessuno dei due studi ha raggiunto la significatività statistica sugli endpoint primari, nonostante la Fase 2 positiva e le aspettative elevate.
2.2 Endpoint secondari e segnale di biologia ossea
- Entrambi gli studi hanno mostrato miglioramenti significativi e sostanziali della densità minerale ossea rispetto ai comparatori, in linea con quanto visto in Fase 2.
- Il profilo di sicurezza è rimasto sostanzialmente invariato rispetto all’esperienza precedente, senza segnali nuovi di rilievo.
- In COSMIC, su popolazione pediatrica con tasso di fratture di base più elevato, si è osservata una riduzione numerica delle fratture rispetto ai bisfosfonati, che però non ha raggiunto la soglia di significatività statistica predefinita.
2.3 Risposta immediata della società
- Ultragenyx ha dichiarato che effettuerà analisi più approfondite, incluse altre misure di salute ossea e endpoint clinici, e discuterà il totale dei dati con i regolatori per capire se resta uno spazio potenziale per UX143 in sottogruppi specifici di OI.
- Parallelamente, il management ha annunciato una revisione delle operazioni e significative riduzioni di spesa, segnale implicito che i costi su OI verranno ridimensionati e che le risorse verranno riassegnate ad altri programmi.
- La reazione in borsa è stata violentissima: RARE ha perso circa il 43–45 percento nella seduta, trattando intorno a 19–20 USD e toccando livelli vicini ai minimi storici.
Per pazienti e clinici OI non è solo una storia di prezzo: un anticorpo potenzialmente disease-modifying
ha fallito l’obiettivo di ridurre le fratture, pur migliorando nettamente la densità ossea. È un promemoria
di quanto, nelle malattie rare, biologia, statistica e standard regolatori possano non allinearsi nel modo
in cui il mercato spera.
3. Timeline 2025 – dall’ottimismo al fallimento sulle fratture
- Febbraio 2025: risultati 2024: ricavi a circa 560M USD, di cui 410M da Crysvita e 88M da Dojolvi. Guidance 2025 a 640–670M di ricavi totali. UX143 in OI è tra i catalyst più attesi.
- Luglio 2025: Ultragenyx e Mereo annunciano che lo studio ORBIT prosegue verso l’analisi finale dopo gli interim, rafforzando l’idea che il programma di Fase 3 in OI sia in rotta per un read-out entro fine anno.
- Luglio–agosto 2025: completato l’arruolamento della Fase 3 ASPIRE su GTX-102 (sindrome di Angelman), mentre parte lo studio Aurora su varianti genotipiche ed età più ampie: il pilastro CNS inizia a pesare.
- Q2–Q3 2025: aggiornamenti finanziari mostrano crescita dei ricavi ma perdite operative elevate. Nel Q3 ricavi a circa 160M USD, con Crysvita 112M, Dojolvi 24M ed Evkeeza 17M. Cassa a circa 447M USD, ulteriormente rafforzata da 400M USD di monetizzazione delle royalty Crysvita.
- Ottobre 2025: primo paziente trattato nello studio Aurora (GTX-102) e prosecuzione del lancio di Evkeeza in Europa, Italia inclusa, a conferma dell’infrastruttura commerciale globale.
- Novembre 2025: call Q3 in cui il management ribadisce la guidance 2025 e parla di “multiple late-stage data readouts, multiple regulatory submissions and multiple launches” nei 12–18 mesi successivi, con OI tra i cardini di questo ciclo.
- 29 dicembre 2025: comunicati i risultati ORBIT e COSMIC: nessuna significatività statistica sulla riduzione delle fratture, ma BMD in netto miglioramento. Annunciati tagli di spesa e rivalutazione strategica del programma. Il titolo subisce uno dei drawdown giornalieri più pesanti della sua storia.
In dodici mesi il mercato è passato dal vedere UX143 come prossimo pilastro accanto a Crysvita/Dojolvi
al trattarlo come asset danneggiato. Il resto della timeline – soprattutto GTX-102, DTX401/301 e UX701 –
ora pesa molto di più di una settimana fa.
4. Pipeline e catalyst residui
4.1 Base commerciale – quattro prodotti approvati
- Crysvita (burosumab): anticorpo per XLH e TIO, in collaborazione con Kyowa Kirin. Ricavi 2024 circa 410M USD, guidance 2025 a 460–480M nelle territory Ultragenyx.
- Dojolvi (triheptanoin): terapia orale per LC-FAOD, con ricavi 2024 attorno a 88M USD e guidance 2025 a 90–100M.
- Mepsevii (vestronidase alfa): ERT per MPS VII (Sly), franchise ultra-rara e mirata.
- Evkeeza (evinacumab): anticorpo per HoFH, con diritti fuori USA acquisiti da Regeneron. Ha generato circa 17M USD nel Q3 2025, con lancio progressivo in vari mercati europei, Italia inclusa.
4.2 UX143 – quanto può valere ancora?
- Pur fallendo gli endpoint primari sulle fratture, UX143 ha mostrato un segnale molto netto su BMD e un profilo di sicurezza pulito.
- Ultragenyx e Mereo esploreranno analisi di sottogruppo, in particolare nella popolazione pediatrica con tassi di fratture più elevati, e discuteranno il pacchetto con i regolatori.
- Realisticamente, la probabilità di un’etichetta ampia per OI si è ridotta in modo drastico. Resta comunque una possibile strada più stretta (per esempio su subset pediatrici con endpoint compositi di salute ossea e funzionale), da verificare dopo analisi complete e feedback delle agenzie.
- Dal punto di vista valutativo, la parte di “blue sky” su UX143 va ora letta come optionalità, non più come driver centrale di equity story.
4.3 Programmi avanzati oltre UX143
GTX-102 (sindrome di Angelman)
- ASO per sindrome di Angelman, progettato per aumentare l’espressione dell’allele paterno UBE3A.
- Lo studio di Fase 3 ASPIRE ha completato l’arruolamento; Aurora – studio aggiuntivo su genotipi ed età più ampi – ha iniziato il dosaggio.
- Dopo il colpo su UX143, GTX-102 diventa uno dei catalyst principali per la parte CNS di Ultragenyx.
DTX401 e DTX301 (gene therapy)
- DTX401 – terapia genica AAV per GSDIa; avviata una rolling BLA nel 2025, con possibili decisioni regolatorie nel 2026–2027.
- DTX301 – terapia genica per deficit di OTC, in percorso verso sviluppo registrativo.
UX701 (morbo di Wilson)
- UX701 è una terapia genica AAV in studio Cyprus2+ (Fase 1/2/3) per morbo di Wilson.
- Gli aggiornamenti delle coorti iniziali hanno mostrato segnali promettenti; ulteriori dati attesi nel 2026 rappresentano un catalyst importante nel filone gene therapy.
UX111 e altri programmi
- UX111 – gene therapy per sindrome di Sanfilippo (MPS IIIA) – ha ricevuto una CRL nel 2025, con l’azienda intenzionata a ripresentare dopo aver affrontato i rilievi FDA.
- Altri programmi in fase più precoce e lavori di lifecycle su Crysvita, Dojolvi, Evkeeza aggiungono catalyst “secondari” alla storia complessiva.
Nel complesso la pipeline contiene ancora diversi “tiri in porta”. UX143 passa da probabile driver a
punto interrogativo con valore residuo; GTX-102, DTX401/301 e UX701 salgono sul podio dei catalyst, con
la base commerciale a finanziare – almeno in parte – il percorso.
5. Situazione finanziaria e rischio diluizione
5.1 Ricavi e redditività
- Ricavi totali Q3 2025: circa 160M USD, +15 percento anno su anno.
- Ricavi Crysvita: 112M; Dojolvi: 24M; Evkeeza: 17M nel trimestre.
- Ricavi 2024: circa 560M USD; guidance 2025 confermata a 640–670M.
- Perdita netta Q3 2025: circa 180M USD, con Opex totali oltre 330M USD, riflesso di R&D elevata e spese pre-launch.
5.2 Cassa, runway e royalty financing
- Cassa, equivalenti e titoli a breve: circa 447M USD al 30 settembre 2025.
- Ultragenyx ha monetizzato una parte delle economics Crysvita in Nord America per 400M USD upfront, aggiungendo cassa non diluitiva ma rinunciando a una fetta delle royalty future.
- Cassa utilizzata nelle operazioni: circa 91M nel Q3; circa 366M sui 9M 2025.
Un’estrapolazione grossolana del burn suggerisce che, nella situazione pre-fallimento UX143, il
bilancio avrebbe finanziato circa due anni di operatività. Le riduzioni di spesa annunciate dovrebbero
estendere la runway, ma l’effetto concreto dipenderà da quanto in profondità verrà tagliato su OI e
su altri programmi.
5.3 Rischio funding e diluizione dopo UX143
- Anche con una posizione di cassa rafforzata, Ultragenyx non è ancora un business auto-sostenibile: le perdite operative sono elevate e più programmi late-stage richiedono capitali significativi per arrivare all’approvazione e al lancio.
- Il fallimento di UX143 rimuove un potenziale contributore di ricavi nel medio termine, aumentando il peso relativo di GTX-102, DTX401/301 e UX701 nelle aspettative future.
- L’impegno a significative riduzioni di spesa indica la volontà di preservare la runway ed evitare finanza in emergenza a prezzi depressi, ma operazioni future di equity, royalty o debito restano probabili nei prossimi 2–3 anni se la società vorrà portare avanti l’intera pipeline.
- Diverse case hanno evidenziato il rafforzamento della posizione di cassa via royalty deal, pur riconoscendo che la redditività non è ancora all’orizzonte nel breve.
6. Reazione di mercato e sentiment
6.1 Una delle peggiori sedute della storia RARE
- Il titolo Ultragenyx ha perso circa il 43–45 percento sulla news UX143, scendendo in area 19–20 USD e avvicinandosi ai minimi storici post-quotazione.
- Diverse testate hanno sottolineato come il drawdown sia tra i peggiori da quando la società è in borsa, mentre Mereo – partner su UX143 – ha subito un crollo ancora più drastico.
6.2 Cosa dice la Street
- Alcune banche hanno ribadito rating Overweight/Outperform con target ben sopra i livelli post-crash, definendo il colpo su UX143 serio ma non tale da distruggere la tesi complessiva, alla luce di pipeline e base commerciale.
- I loro argomenti puntano sulla resilienza dei ricavi Crysvita/Dojolvi/Evkeeza e sui prossimi dati di GTX-102 e dei programmi gene therapy.
- Resta comunque il fatto che UX143 pesava molto nei modelli di lungo periodo e che la fiducia ha subito un colpo significativo.
6.3 Sentiment retail (Stocktwits, Reddit, X)
- La reazione iniziale sui social è la solita miscela di shock e frustrazione: molti post puntano l’attenzione sull’entità del crollo, sul contrasto con la Fase 2 e su accuse di eccesso di fiducia da parte del management.
- Un sottoinsieme di trader inizia subito a raccontare la storia come possibile occasione, mettendo
l’accento su:
- segnale netto su BMD e safety intatta,
- base commerciale Crysvita/Dojolvi/Evkeeza ancora in crescita,
- target price ben sopra i livelli post-panic.
- Ricompagiono anche molti miti classici: short che “sapevano già tutto”, analisti che “riporteranno il prezzo su”, o frasi tipo “le fratture contano poco perché basta la BMD”; tutti elementi che vanno filtrati con molta prudenza.
Il punto non è che “la folla ha torto” o “la folla ha ragione”, ma che la composizione del book cambia.
Un tonfo così violento di solito espelle le mani più deboli e attira trader event-driven. Quello che conta,
dopo, è se i catalyst futuri e l’esecuzione riusciranno a riportare dentro capitali più pazienti e orientati
ai fondamentali.
7. Mappa scenari (solo illustrativa)
Scenario base – rifocalizzazione e lenta riparazione
UX143 non diventa un best seller ampio, ma resta possibile una strada limitata (per subset specifici o mercati selezionati) dopo analisi aggiuntive. Il management esegue in modo credibile i tagli di spesa, mette GTX-102, DTX401/301 e UX701 al centro, e mantiene crescita Crysvita/Dojolvi/Evkeeza grossomodo in linea con le guidance. Il titolo si muove sul bilanciamento tra runway e progressi pipeline, con volatilità alta ma panico iniziale in parte assorbito.
Scenario bull – salvataggio parziale UX143 + delivery pipeline
Analisi post-hoc e confronto con i regolatori portano a una via praticabile per UX143, magari in un segmento pediatrico severo dove BMD e beneficio clinico sono abbastanza forti da sostenere l’uso. In parallelo, GTX-102 genera dati robusti in Angelman, DTX401 ottiene l’ok regolatorio e UX701 continua a mostrare risultati convincenti in Wilson. I ricavi si muovono verso la parte alta della guidance (e oltre), e la società riesce a finanziare lo sviluppo principalmente con cassa interna e deal non punitivi.
Scenario bear – write-off UX143 e squeeze sul funding
UX143 viene di fatto azzerato come asset commerciale; le analisi di sottogruppo non portano a un percorso regolatorio appetibile. Uno o più programmi avanzati falliscono (per esempio un problema su GTX-102 o sulle gene therapy), mentre i costi si rivelano più rigidi del previsto. In questo contesto servono nuove risorse in condizioni sfavorevoli, con forte diluizione, compressione dei multipli e overhang di lungo periodo sull’equity.
Gli scenari non sono previsioni né consigli operativi, ma cornici per ragionare in termini di range
piuttosto che di singolo “sì/no”: dati sulle fratture, altri readout pivotal, burn, opzioni di finanziamento.
8. Rischi principali e red flags
Rischio clinico trasversale alla pipeline
Il fallimento UX143 ricorda che anche segnali di Fase 2 apparentemente solidi possono dissolversi in Fase 3. GTX-102, DTX401/301, UX701 e UX111 portano con sé rischio clinico e regolatorio; un altro flop di peso indebolirebbe in modo sostanziale la tesi su RARE.
Burn strutturalmente elevato
Opex oltre i 300M USD a trimestre e circa 366M USD di cassa bruciata in 9 mesi indicano un modello ancora lontano dall’equilibrio. I tagli annunciati aiuteranno, ma vanno bilanciati con l’esigenza di non sterilizzare i programmi avanzati.
Finanza e diluizione
Anche con 447M di cassa e 400M da royalty deal, è verosimile che Ultragenyx debba ricorrere a nuova finanza entro pochi anni se vorrà portare avanti l’intera pipeline. Tempistica e struttura (equity, royalty, debito) avranno un impatto diretto sugli azionisti attuali.
Concorrenza e payers
Nel mondo rare disease/gene therapy, concorrenza e dinamiche di prezzo si stanno muovendo rapidamente. Futuri approcci concorrenti in Angelman, Wilson, GSDIa o altre indicazioni potrebbero ridimensionare alcune aspettative di picco o comprimere prezzi e rimborsi.
9. Outlook – rimonta possibile o trappola?
Un drawdown di oltre il quaranta percento su un fallimento di Fase 3 non è mai “solo una buying opportunity”: riflette una perdita reale di flussi di cassa attesi e un colpo alla credibilità del management. Allo stesso tempo, Ultragenyx non è la classica one-asset biotech che implode a livello cassa; è una realtà già commerciale nel mondo delle malattie rare, con più prodotti approvati e una pipeline ampia.
Nel breve, le variabili chiave sono:
- la profondità e la credibilità delle riduzioni di spesa e della rifocalizzazione post-UX143,
- il ritmo e la qualità dei progressi su GTX-102, DTX401/301 e UX701,
- l’eventuale esistenza di una via residua, anche limitata, per UX143 in sottogruppi OI,
- e la tempistica/condizioni delle future operazioni di finanziamento.
Da un punto di vista educativo, il caso RARE è un promemoria forte del perché il trading sui catalyst non possa basarsi solo su “Fase 2 buona” e “analisti ottimisti”. La società ha ancora leve da giocare per tentare una rimonta lenta; se questo si tradurrà in creazione di valore per gli azionisti dipenderà da esecuzione, disciplina sulla spesa e un po’ di fortuna sui prossimi readout.
10. “My tale” – la lettura personale (spazio autore)
Dove (eventualmente) si incastra RARE in una strategia biotech reale
Qui entra la tua voce: come un nome come Ultragenyx può – o non può – rientrare nella logica RunUp e
nella gestione pratica del rischio. Per esempio:
– se dopo un tonfo del genere lo consideri solo per swing/rimbalzi tecnici,
– se lo vedi come parte di un paniere di “platform biotech” con ricavi reali ma rischi elevati,
– oppure se ritieni che il bilancio rischio/rendimento sia peggiorato troppo rispetto ad altre opportunità nel settore.
Il box serve per collegare numeri, pipeline e sentiment con regole concrete: size, ingresso/uscita, gestione dei catalyst e tolleranza al drawdown.
– se dopo un tonfo del genere lo consideri solo per swing/rimbalzi tecnici,
– se lo vedi come parte di un paniere di “platform biotech” con ricavi reali ma rischi elevati,
– oppure se ritieni che il bilancio rischio/rendimento sia peggiorato troppo rispetto ad altre opportunità nel settore.
Il box serve per collegare numeri, pipeline e sentiment con regole concrete: size, ingresso/uscita, gestione dei catalyst e tolleranza al drawdown.
11. Fonti e letture consigliate
Principali fonti utilizzate: comunicati ufficiali Ultragenyx/Mereo, risultati finanziari trimestrali, filing SEC, e articoli di sintesi di testate finanziarie specializzate. Prima di qualsiasi decisione operativa è sempre necessario rileggere i documenti più recenti direttamente dalle fonti primarie.
Questo report ha finalità esclusivamente informative e formative. Non costituisce in alcun modo
consulenza in materia di investimenti, né offerta o sollecitazione al pubblico risparmio. Dati, date
e interpretazioni possono contenere errori o diventare rapidamente non aggiornati. Ogni decisione
operativa richiede verifiche autonome sulle fonti primarie (filing, comunicati ufficiali, documenti
regolatori) e, ove necessario, il supporto di professionisti abilitati.
Biotech Catalyst Calendar
If you want a structured view of upcoming PDUFA dates, Phase 2/3 read-outs and other key biotech events,
you can check the dedicated Biotech Catalyst Calendar on Merlintrader trading Blog.
Per una vista d’insieme su PDUFA, letture di Fase 2/3 e date chiave del settore biotech, puoi consultare
la pagina dedicata sul sito Merlintrader. Il calendario aggrega gli eventi più rilevanti e viene aggiornato
periodicamente.
Vai al Biotech Catalyst Calendar
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


