DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
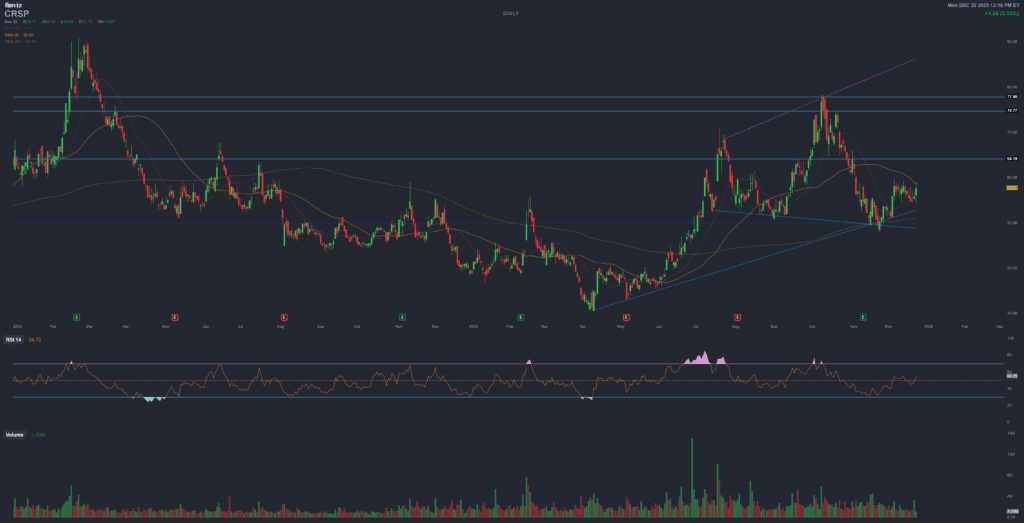
CRISPR Therapeutics (CRSP) – Casgevy, Zugo-cel and the Next Wave of Gene Editing
Long-form, filings-based look at where CRISPR Therapeutics stands at the end of 2025: from the first commercial CRISPR therapy to autoimmune CAR T and in vivo lipid editing.
CRSP
Nasdaq | CRISPR Therapeutics AG
News of the day – 22 Dec 2025
Zugo-cel update: early autoimmune signal and strong LBCL responses
CRISPR Therapeutics released a broad update on zugocaptagene geleucel (zugo-cel, ex CTX112) in autoimmune disease and B-cell malignancies.
- In autoimmune disease (early Phase 1), four patients at the 100M cell dose showed rapid and deep B-cell depletion, with the first SLE patient reported in DORIS remission at month 6 so far.
- In relapsed/refractory LBCL, the recommended Phase 2 dose at 600M cells delivered around 90 percent overall response and about 70 percent complete responses in the evaluable cohort, with good early tolerability for an allogeneic product.
- The company also announced a collaboration with Eli Lilly to test zugo-cel in combination with pirtobrutinib in aggressive B-cell lymphomas and signalled further expansion to immune cytopenias like ITP and wAIHA.
Executive summary
CRISPR Therapeutics enters 2026 as a hybrid story: part royalty-like partner on a first-in-class commercial gene therapy (Casgevy for SCD/TDT), part high-risk platform company pushing CRISPR into autoimmune disease, oncology, cardiovascular disease and regenerative medicine.
On the de-risked side, Casgevy is ramping with dozens of authorized treatment centers and tens of patients already infused, while pediatric Phase 3 programs in 5–11 year olds are fully enrolled and moving toward data and label expansion. On the high-beta side, zugo-cel and the in vivo ANGPTL3/Lp(a) programs are generating eye-catching early data but still need larger, longer trials before anyone can talk about durable benefit or commercial footprint.
Financially, the company couples a very large cash balance and no traditional product-based revenue yet on its own books (Casgevy economics flow through Vertex), with a sizeable operating loss driven by R&D and collaboration expense. The cash pile gives several years of runway at the current burn rate, but investors have clearly priced in expectations for pipeline execution and a second wave of value beyond Casgevy.
This report focuses on: (1) where the Casgevy launch really stands; (2) the structure and risk profile of zugo-cel in autoimmune disease and lymphoma; (3) the in vivo cardiovascular programs CTX310/320 and the SyNTase AATD program (CTX460); (4) the balance sheet; and (5) how analysts and retail traders are currently framing the stock.
Company overview
CRISPR Therapeutics AG is a gene-editing company headquartered in Zug (Switzerland) with major operations in Boston. The core technology is ex vivo and in vivo editing using CRISPR/Cas9, with a pipeline that now spans hemoglobinopathies, oncology, autoimmune disease, cardiovascular and metabolic disorders, alpha-1 antitrypsin deficiency, refractory hypertension, acute hepatic porphyria and type 1 diabetes.
The first commercial product, Casgevy (exagamglogene autotemcel), is co-developed with Vertex for sickle cell disease and transfusion-dependent beta-thalassemia. It is approved across the US, Europe and several Middle East markets, with more than sixty thousand patients considered eligible across those regions and a growing network of authorized treatment centers processing referrals, collections and infusions.
Beyond Casgevy, management is deliberately building a diversified platform: in vivo lipid editing (CTX310/320), allogeneic CAR T (zugo-cel/CTX112 and CTX131), RNA-based anticoagulation (SRSD107 with Sirius Therapeutics) and regenerative medicine programs for type 1 diabetes, supported by an internal GMP manufacturing facility for cell therapies.
Key programs and pipeline structure
| Program | Modality / target | Indication(s) | Stage |
|---|---|---|---|
| Casgevy (exa-cel) | Ex vivo CRISPR-edited autologous HSC | Sickle cell disease, TDT | Approved (multiple regions), Phase 3 pediatrics |
| Zugo-cel (CTX112) | Allogeneic CD19 CAR T | R/R B-cell malignancies, refractory autoimmune disease (SLE, SSc, IIM) | Phase 1/2, RMAT for some lymphomas |
| CTX310 | In vivo CRISPR, ANGPTL3 | Severe lipid disorders, sHTG, mixed dyslipidemia | Phase 1, moving to Phase 1b |
| CTX320 | In vivo CRISPR, LPA | Elevated Lp(a), cardiovascular risk reduction | Phase 1, update expected 1H 2026 |
| CTX460 (SyNTase) | In vivo gene correction, SERPINA1 | Alpha-1 antitrypsin deficiency | Preclinical, first-in-human planned mid-2026 |
| CTX340 | In vivo CRISPR, AGT | Refractory hypertension | IND/CTA-enabling |
| SRSD107 | siRNA, Factor XI | Thromboembolic prophylaxis (e.g. after TKA) | Phase 2, first patient dosed |
| Regenerative T1D | Gene-edited iPSC-derived beta cells | Type 1 diabetes | Early clinical / preclinical next-gen |
The picture that emerges is a broad platform with several high-value “spokes”: curative hemoglobinopathies anchored by Casgevy, next-generation autoimmune and oncology via allogeneic CAR T, and in vivo hepatic editing aimed at transforming chronic cardiovascular risk management into one-time interventions.
Catalyst and timeline overview (late 2025 – 2027)
Q4 2025
Casgevy pediatrics / ASH data
Initial data for pediatric Phase 3 Casgevy in 5–11 year-olds with SCD/TDT presented at ASH 2025, following completion of enrollment and dosing. These data underpin potential label expansion to younger ages and longer-term uptake beyond the initial adult launch.
Late 2025 – 2026
Zugo-cel expansion
Ongoing Phase 1/2 trials in R/R B-cell malignancies and refractory autoimmune disease with a recommended Phase 2 dose now selected in LBCL and early remission signals in SLE. The company has guided to broader updates on oncology and autoimmune indications and is layering a new Lilly combination trial for aggressive B-cell lymphomas.
2026
In vivo cardiovascular readouts
CTX310 Phase 1 results already show large, dose-dependent reductions in ANGPTL3, triglycerides and LDL cholesterol; the program is moving into Phase 1b focused on the highest-risk lipid patients. CTX320 for Lp(a) is expected to generate its first clinical update in the first half of 2026, with CTX340 hypertension data from non-clinical models already pointing to deep AGT knockdown and durable blood pressure reductions.
Mid 2026
First SyNTase in-human trial
CTX460, the first SyNTase-based in vivo correction program for AATD, is planned to enter the clinic around mid-2026, aiming to move beyond gene knock-out and into precise single-dose correction in humans.
2026–2027
Commercial maturation
The Casgevy franchise is expected to scale as referral pathways, ATCs and reimbursement mature, with Vertex already signalling a clear path to over USD 100M in 2025 revenues and significantly higher figures in 2026. For CRISPR Therapeutics, this means a shift from purely development-stage economics toward recurring collaboration revenue and, potentially, a partial self-funding model for the broader pipeline.
Financial snapshot and runway
As of 30 September 2025, CRISPR Therapeutics reported roughly USD 286M in cash and around USD 1.66B in marketable securities (current and non-current), for a total liquidity buffer close to USD 1.9B. Total assets are around USD 2.25B and total shareholders’ equity stands just below USD 1.92B.
For the first nine months of 2025 the company booked about USD 2.6M in grant revenue and no collaboration revenue, while total operating expenses exceeded USD 512M, dominated by R&D and collaboration expense related to the Vertex agreements and platform build-out. Net loss for the period was approximately USD 451M.
At a very rough, linear extrapolation, this suggests 3–4 years of cash runway at the current burn rate, excluding any potential future collaboration milestones, Casgevy profit share ramp, or changes in spending. In practice, cash usage is likely to be lumpy, with peaks around manufacturing scale-up, new indications and larger late-stage trials.
Key point: the balance sheet is a strategic asset here. It gives the company room to run multiple ambitious programs in parallel, but investors are implicitly expecting this capital to be converted into durable value rather than a prolonged series of expensive early-stage experiments.
Management and strategic posture
The company is led by CEO Samarth Kulkarni, who has been the public face of CRISPR Therapeutics throughout the Casgevy journey and the expansion into in vivo editing. Under his tenure the company has consciously shifted from a single-program “optionality on sickle cell” to a diversified platform with multiple modalities: autologous HSC editing, allogeneic CAR T, in vivo LNP editing and siRNA.
Strategically, the Q3 2025 update highlights a few consistent themes:
- Double down on Casgevy with Vertex as the commercial engine, including geographic expansion, pediatric data and treatment pathway optimization.
- Use the Casgevy cash flows (once they are large enough) to partially de-risk the more experimental parts of the pipeline, especially in vivo cardiovascular and SyNTase-based gene correction.
- Maintain internal cell therapy manufacturing capacity to keep control over CAR T supply and quality while expanding autoimmune and lymphoma indications.
On communication, the company has become more deliberate about grouping updates (for example, promising broad zugo-cel readouts and in vivo updates at specific conferences), which reflects both regulatory sensitivity around early data and market fatigue with incremental, fragmentary news.
Sentiment: analysts and retail
Sentiment – non-professional traders
Analyst coverage on CRSP remains mixed but broadly constructive: some houses frame the stock as a high-risk, high-optionality way to participate in the next wave of gene editing beyond Casgevy, while others emphasise the long timelines and the complexity of turning early-stage programs into commercial products. Several recent notes explicitly point to the combination of a solid cash runway and volatile share price as characteristic of “platform stories” in this space.
On the retail side, CRSP has become one of the more visible gene-editing tickers on Stocktwits and Reddit, particularly after the CTX310 lipid data and the recent zugo-cel headlines. A widely shared Stocktwits article described the CTX310 Phase 1 results as a breakthrough, highlighting around 70 percent reductions in certain lipid markers at the highest dose and capturing bulls who see the stock as “undervalued” relative to the breadth of the pipeline.
As usual, this sentiment cuts both ways: strong enthusiasm for “one-shot” gene editing solutions and potential cardiovascular disruption on the upside, and deep scepticism around safety, durability, pricing and real-world adoption on the downside. Day-to-day trading often reflects this tension more than the slow-moving fundamentals.
Note: the sentiment summary above is drawn from public comments on platforms like Reddit, Stocktwits and X. These are opinions by non-professional traders and should never be treated as investment advice or as a substitute for independent analysis.
Scenario map: what could go right or wrong
Upside scenario (conceptual, not a prediction)
In a constructive scenario, Casgevy achieves broad reimbursement and operational maturity, with steady growth in patient flow through 2026–2028, including younger age groups. Zugo-cel proves both safe and durably effective in larger autoimmune and lymphoma cohorts, with the Lilly collaboration helping to define combination strategies for aggressive B-cell disease. The in vivo cardiovascular programs confirm durable lipid and Lp(a) lowering with acceptable safety, paving the way for pivotal development in well-defined high-risk populations.
In this world, CRISPR Therapeutics transitions from a single-product royalty story into a multi-asset platform, with several programs capable of generating significant long-term cash flows and supporting further innovation.
Base-case execution path
A more neutral view assumes a continued but measured Casgevy ramp, with some bottlenecks around centre capacity, patient selection and payor policies, while zugo-cel and CTX310/320 progress through early- and mid-stage development with inevitable pauses, protocol amendments and competing data from other players. Timelines extend, but the overall strategic direction remains intact.
Downside / risk-intensive scenario
On the negative side, several things could go wrong at once: safety signals in autoimmune or in vivo programs, regulatory pushback around long-term follow-up and durability, slower-than-expected Casgevy uptake, or pricing headwinds that limit real-world adoption. Any major adverse event in the gene editing space could also reset risk appetite for the entire class and compress valuations across the board, irrespective of CRISPR Therapeutics’ own data.
None of these scenarios are certainties; they illustrate the range of outcomes that long-term holders need to keep in mind in a field that is both scientifically exciting and structurally high risk.
Risk map
Regulatory and safety
Gene editing and CAR T remain under intense scrutiny. Long-term safety follow-up, insertional events, off-target effects, prolonged cytopenias or secondary malignancies could all trigger regulatory pauses or label restrictions.
Execution and manufacturing
Casgevy and cell therapies require complex logistics and manufacturing. Any supply disruption, quality issue or bottleneck at authorized centres could slow ramp-up and weaken the commercial narrative.
Competition and economics
CRISPR Therapeutics competes not only with other gene-editing players but also with small molecules, antibodies and RNA-based therapies. Pricing pressure, alternative options and payor strategies will heavily influence real-world penetration and margins.
Bottom line
CRISPR Therapeutics sits in a rare position: one foot in the present, via Casgevy, and one foot deep in the future, via autoimmune CAR T, in vivo cardiovascular editing and regenerative medicine for T1D. The Q3 2025 data show a company that is still loss-making but well funded, with a broad set of technical tools and a clear desire to move beyond a single-asset narrative.
Whether this ultimately justifies today’s valuation is a separate question and depends on time horizon, risk tolerance and views on gene-editing as a whole. What can be said from the data alone is that the core elements are real: an approved product with growing adoption, early but promising signals in autoimmune disease and lipid disorders, and a balance sheet capable of supporting several major clinical bets in parallel.
This report is not a recommendation to buy or sell CRSP. It is an attempt to map out the factual landscape so that traders and investors can decide for themselves how, or if, this story fits into their own approach.
Key sources and links
- CRISPR Therapeutics – Q3 2025 business update and financial results (Casgevy metrics, CTX310 data, pipeline status, cash and loss figures).
- CRISPR Therapeutics – Q3 2025 Form 10-Q filed with the US SEC (balance sheet, income statement, risk factors, collaboration details with Vertex, program descriptions).
- Company press release and news coverage on the December 2025 zugo-cel update (autoimmune cohort, LBCL response rates, collaboration with Eli Lilly).
- Stocktwits news article summarising CTX310 Phase 1 data and retail reaction after the American Heart Association presentation and NEJM publication.
- Additional context from major financial and biotech media on gene-editing clinical trials, Casgevy real-world roll-out and the evolving competitive landscape.
Some external links used for charts or data access (for example Finviz, Seeking Alpha, Stocktwits or broker tools) may include affiliate or referral parameters for Merlintrader. These do not change the content you see or the price you pay, and they never influence the conclusions of the analysis.
Legal and risk disclaimer
Informational only, not investment advice. This report is based on public information from company filings, regulatory documents, and reputable news outlets at the time of writing. It may contain errors, omissions or outdated data as new information emerges.
Nothing in this text is a recommendation to buy, sell or hold any security, nor a solicitation to do so. The author is not a registered investment adviser or a licensed financial professional. Any reference to potential scenarios, upside, downside or market behaviour is purely illustrative and not a prediction.
Readers should carry out their own due diligence, consider their personal risk tolerance and financial situation, and, where appropriate, consult a qualified financial professional. Markets can move quickly, gene-editing programs carry significant scientific and regulatory uncertainty, and capital can be lost, including the entire amount invested.
This content is intended for an international audience that includes readers in both the European Union and the United States. The language and structure are designed to be consistent with the spirit of applicable guidance from regulators such as CONSOB and the SEC for purely informational, non-promotional commentary.
Authors: Merlintrader and Jane.
For full legal notes and privacy information, please refer to:
Disclaimer
Termini di Servizio, Privacy, Cookie Policy // Term of Service, Privacy, Cookie Policy
Biotech Catalyst Calendar
For an updated overview of upcoming biotech catalysts across PDUFA dates, clinical readouts and major regulatory events, you can always refer to the dedicated Merlintrader Biotech Catalyst Calendar page.
CRISPR Therapeutics (CRSP) – Casgevy, Zugo-cel e la nuova ondata di gene editing
Analisi estesa, basata su documenti ufficiali, su dove si trova CRISPR Therapeutics a fine 2025: dalla prima terapia CRISPR in commercio all’espansione in autoimmuni, linfomi e malattie cardiovascolari.
CRSP
Nasdaq | CRISPR Therapeutics AG
News del giorno – 22 dic 2025
Aggiornamento zugo-cel: primi segnali in autoimmuni e risposte forti in LBCL
CRISPR Therapeutics ha pubblicato un aggiornamento ampio su zugocaptagene geleucel (zugo-cel, ex CTX112) nelle malattie autoimmuni e nelle neoplasie a cellule B.
- Nel braccio autoimmune (Phase 1 iniziale), quattro pazienti trattati alla dose da 100 milioni di cellule mostrano una deplezione rapida e profonda dei linfociti B, con il primo paziente SLE riportato in remissione secondo criteri DORIS a 6 mesi.
- Nei LBCL recidivati/refrattari, alla dose raccomandata di 600 milioni di cellule si osservano tassi di risposta globale intorno al 90 percento e di risposta completa nell’ordine del 70 percento sul gruppo valutabile, con un profilo di tollerabilità iniziale favorevole per un prodotto allogenico.
- L’azienda annuncia anche una collaborazione con Eli Lilly per testare zugo-cel in combinazione con pirtobrutinib nei linfomi B aggressivi e segnala l’espansione verso citopenie autoimmuni come ITP e wAIHA.
Executive summary
CRISPR Therapeutics entra nel 2026 come storia ibrida: in parte partner “quasi-royalty” su una terapia CRISPR ormai approvata (Casgevy per SCD/TDT), in parte piattaforma ad alto rischio che spinge il gene editing in autoimmuni, oncologia, cardiovascolare e rigenerativa.
Sul lato relativamente de-rischizzato, Casgevy sta crescendo con una rete in espansione di centri autorizzati e decine di pazienti già infusi, mentre gli studi pediatrici globali in età 5–11 anni sono completati e puntano a dati e possibile estensione d’indicazione. Sul lato a più alto beta, zugo-cel e i programmi in vivo ANGPTL3/Lp(a) generano dati molto forti ma ancora iniziali, che richiedono conferme su coorti più grandi e follow-up più lungo.
A livello finanziario, l’azienda abbina una cassa molto ampia e nessun ricavo “pieno” di prodotto contabilizzato direttamente (Casgevy passa tramite Vertex), con una perdita operativa importante guidata da R&D e costi di collaborazione. La cassa offre alcuni anni di runway ai ritmi attuali, ma il mercato ha chiaramente prezzato l’aspettativa che questa liquidità venga trasformata in valore strutturale attraverso l’esecuzione della pipeline.
In questa analisi ci concentriamo su: (1) dove è davvero il lancio di Casgevy; (2) struttura e profilo di rischio di zugo-cel in autoimmuni e linfomi; (3) i programmi cardiovascolari in vivo CTX310/320 e il progetto SyNTase CTX460; (4) cassa e conto economico; (5) come analisti e retail stanno leggendo oggi la storia CRSP.
Panoramica aziendale
CRISPR Therapeutics AG è una biotech focalizzata sul gene editing con sede a Zug e hub operativo a Boston. Il core tecnologico è l’uso di CRISPR/Cas9 in modalità ex vivo e in vivo, con una pipeline che oggi copre emoglobinopatie, oncologia, malattie autoimmuni, disturbi cardiovascolari e metabolici, deficit di alfa-1 antitripsina, ipertensione resistente, porfiria epatica acuta e diabete di tipo 1.
Il primo prodotto in commercio, Casgevy (exagamglogene autotemcel), è co-sviluppato con Vertex per anemia falciforme e beta-talassemia trasfusione-dipendente. È già approvato in Stati Uniti, Europa e diversi paesi del Medio Oriente, con una popolazione potenziale complessiva superiore alle sessantamila unità e un numero crescente di centri autorizzati che gestiscono invii, raccolte cellulari e infusioni.
Oltre Casgevy, il management sta costruendo una piattaforma volutamente ampia: editing in vivo del fegato (CTX310/320), CAR T allogeniche (zugo-cel/CTX112 e CTX131), un programma siRNA con Sirius Therapeutics (SRSD107) e iniziative di medicina rigenerativa per il T1D, supportate da un impianto GMP di proprietà per la produzione di terapie cellulari.
Pipeline e programmi principali
| Programma | Modalità / target | Indicazioni | Stadio |
|---|---|---|---|
| Casgevy (exa-cel) | HSC autologhe editate ex vivo | Sickle cell disease, beta-talassemia TDT | Approvato, Phase 3 pediatrica |
| Zugo-cel (CTX112) | CAR T allogenica anti-CD19 | Neoplasie B recidive/refrattarie, malattie autoimmuni severe | Phase 1/2, designazione RMAT in alcuni linfomi |
| CTX310 | CRISPR in vivo, ANGPTL3 | Dislipidemie gravi, sHTG, mixed dyslipidemia | Phase 1, in transizione a Phase 1b |
| CTX320 | CRISPR in vivo, LPA | Lp(a) elevata, rischio cardiovascolare | Phase 1, aggiornamento atteso 1H 2026 |
| CTX460 (SyNTase) | Correzione in vivo, SERPINA1 | Deficit di alfa-1 antitripsina | Preclinico, avvio studio previsto a metà 2026 |
| CTX340 | CRISPR in vivo, AGT | Ipertensione resistente | IND/CTA-enabling |
| SRSD107 | siRNA, FXI | Prevenzione TEV post chirurgia ortopedica e oltre | Phase 2 |
| Medicina rigenerativa T1D | Beta-cellule derivate da iPSC editate | Diabete di tipo 1 | Clinico iniziale / preclinico avanzato |
Il quadro è quello di una piattaforma con più assi di creazione valore: emoglobinopatie curative basate su Casgevy, autoimmuni/oncologia via CAR T allogeniche e un blocco cardiovascolare/metabolico che mira a trasformare la gestione del rischio a lungo termine con interventi una tantum.
Catalyst e tempistiche (fine 2025 – 2027)
Q4 2025
Casgevy pediatrico / dati ASH
Presentazione dei primi dati degli studi Phase 3 pediatrici di Casgevy nei bambini 5–11 anni con SCD/TDT al congresso ASH 2025, dopo il completamento di arruolamento e dosing. Questi dati sono la base per un’estensione di età in etichetta e per una crescita più strutturale della franchise.
Fine 2025 – 2026
Espansione zugo-cel
Proseguono gli studi Phase 1/2 nei linfomi B recidivi/refrattari e nelle malattie autoimmuni refrattarie, con dose raccomandata definita nei LBCL e segnali iniziali di remissione in SLE. L’accordo con Lilly apre un fronte combinatorio nei linfomi aggressivi, mentre i nuovi target autoimmuni (ITP, wAIHA) ampliano ulteriormente il perimetro.
2026
Programmi cardiovascolari in vivo
CTX310 ha già mostrato riduzioni marcate e dose-dipendenti di ANGPTL3, trigliceridi e LDL, con passaggio a un Phase 1b focalizzato sui pazienti a rischio più alto. CTX320 su Lp(a) dovrebbe avere le prime letture cliniche nella prima metà del 2026; CTX340 ha alle spalle dati preclinici con knockdown profondo di AGT e riduzioni pressorie durature in modelli animali.
Metà 2026
Primo trial SyNTase in Human
CTX460, primo programma basato sulla piattaforma SyNTase per la correzione di SERPINA1 nell’AATD, è previsto in ingresso in clinica intorno a metà 2026, con l’obiettivo dichiarato di dimostrare correzione precisa “one shot” in vivo.
2026–2027
Maturazione commerciale
La franchise Casgevy dovrebbe crescere man mano che percorsi, rimborsi e capacità dei centri si stabilizzano. Vertex ha già guidato verso oltre 100 milioni di dollari di ricavi nel 2025 con ulteriore crescita nel 2026. Per CRISPR Therapeutics questo significa passare da pura “story di sviluppo” a modello ibrido con flussi ricorrenti che possono finanziare una parte rilevante della pipeline.
Situazione finanziaria e runway
Al 30 settembre 2025, CRISPR Therapeutics riportava circa 286 milioni di dollari di cassa e circa 1,66 miliardi in titoli negoziabili (correnti e non), per una “liquidità” complessiva intorno a 1,9 miliardi. L’attivo totale è circa 2,25 miliardi, con patrimonio netto vicino a 1,92 miliardi.
Nei primi nove mesi del 2025 i ricavi si limitano a circa 2,6 milioni di dollari da grant, senza ancora contributi di collaborazione, mentre le spese operative superano i 512 milioni, principalmente per R&D e costi legati agli accordi con Vertex e alla costruzione della piattaforma. La perdita netta 9M 2025 è intorno ai 451 milioni.
In modo grossolano, questo implica 3–4 anni di runway se il burn restasse sugli attuali livelli e se non ci fossero milestone, cambi di spesa o un contributo crescente dai flussi economici di Casgevy. Nella realtà il profilo sarà più irregolare, con picchi legati a espansioni produttive e a studi avanzati di maggiori dimensioni.
Punto centrale: la cassa è una parte essenziale della tesi. Permette a CRSP di correre più programmi in parallelo rispetto a molte small/mid cap, ma al tempo stesso crea aspettative: il mercato si aspetta che questo capitale venga trasformato in asset con valore misurabile, non solo in sperimentazioni early-stage.
Management e impostazione strategica
L’azienda è guidata dal CEO Samarth Kulkarni, figura centrale sin dalle prime fasi di Casgevy e della successiva espansione verso editing in vivo. Sotto la sua guida CRISPR Therapeutics è passata da “scommessa singola sul sickle cell” a piattaforma multi-asset con modalità diverse: HSC autologhe, CAR T allogeniche, editing epatico in vivo e siRNA.
La comunicazione strategica negli ultimi trimestri insiste su tre direttrici:
- Massimizzare il valore di Casgevy insieme a Vertex (nuovi paesi, pediatrico, ottimizzazione dei percorsi e dei centri).
- Usare il potenziale flusso di cassa di Casgevy per finanziare in parte i blocchi a rischio più alto (autoimmuni, cardiovascolare in vivo, SyNTase).
- Mantenere capacità produttiva interna per le terapie cellulari, così da non dipendere interamente da terzi su supply e qualità.
Anche sul piano del newsflow, l’azienda sembra preferire “pacchetti” di aggiornamenti aggregati (per esempio zugo-cel e in vivo CTX310/320 in date precise), segno che vuole evitare sia eccesso di hype, sia aggiornamenti troppo frammentari su numeri piccoli di pazienti.
Sentiment: analisti e retail
Sentiment – trader non professionisti
Il consenso degli analisti è misto ma tendenzialmente costruttivo: molti descrivono CRSP come una “piattaforma da opzionalità”, dove la parte relativamente più visibile è Casgevy, mentre il resto della pipeline rappresenta una serie di call opzionali su autoimmuni, cardiovascolare e T1D. Altri report sono più cauti e sottolineano la combinazione di tempi lunghi, barriere regolatorie e concorrenza crescente.
Sul fronte retail, CRSP è diventato uno dei ticker CRISPR più discussi su Stocktwits e Reddit, soprattutto dopo i dati di CTX310 presentati all’AHA con pubblicazione su NEJM e ora con il nuovo aggiornamento su zugo-cel. Un articolo molto citato su Stocktwits definisce le riduzioni di ANGPTL3, trigliceridi e LDL “senza precedenti” e riporta commenti di utenti che vedono il titolo “sottovalutato” rispetto all’ampiezza della pipeline.
Tutto questo, come sempre, va letto con cautela: l’entusiasmo per “cure one-shot” e per il potenziale disruption cardiovascolare convive con dubbi profondi su sicurezza di lungo termine, durabilità, prezzi e rimborsabilità. Molti movimenti di breve su CRSP riflettono più questa tensione di sentiment che i lenti cambiamenti dei fondamentali.
Nota: il riassunto del sentiment si basa su commenti pubblici di trader retail su Reddit, Stocktwits e X. Si tratta di opinioni non professionali, che non devono essere considerate consulenza finanziaria né sostituto di un’analisi autonoma.
Mappa scenari: cosa può andare bene o male
Scenario “positivo” (concettuale, non una previsione)
Nello scenario favorevole, Casgevy ottiene una traiettoria stabile di adozione, con estensione pediatrica, percorsi rodati e maggior visibilità sui ricavi ricorrenti. Zugo-cel dimostra sicurezza e durata anche con numeri più grandi sia in autoimmuni che in oncologia, e la collaborazione con Lilly aiuta a definire regimi combinati credibili nei linfomi aggressivi. CTX310/320 si confermano in grado di ridurre in modo duraturo lipidi e Lp(a) in sottogruppi ad alto rischio con profili di safety accettabili, aprendo la strada a studi registrativi.
Scenario “di esecuzione”
Un percorso più neutro vede Casgevy crescere ma con frizioni (centri limitati, complessità logistiche, payor esigenti), zugo-cel proseguire con alti e bassi tipici degli early-stage (aggiornamenti limitati, revisioni di protocollo, concorrenza) e i programmi in vivo avanzare in modo più graduale, sotto la lente di FDA e dei comitati etici.
Scenario negativo / ad alto rischio
Sul lato downside, eventuali segnali di safety seri in autoimmuni, CAR T o program in vivo, una frenata regolatoria sul gene editing o problemi di pricing e accesso su Casgevy potrebbero comprimere in fretta la tesi. Anche eventi negativi su altri programmi CRISPR del settore potrebbero avere un effetto “macro” sul sentiment e sulle valutazioni, indipendentemente dai dati specifici di CRSP.
Non si tratta di probabilità assegnate, ma del ventaglio di possibilità che chi guarda il titolo con orizzonte multi-anno deve tenere in mente.
Mappa rischi
Rischio regolatorio/sicurezza
Il gene editing resta sotto lente stretta. Eventuali eventi avversi gravi, problemi di off-target o segnali sospetti in follow-up di lungo periodo potrebbero rallentare o bloccare programmi chiave.
Esecuzione e produzione
Casgevy e le terapie cellulari richiedono logistica complessa e impianti affidabili. Qualsiasi intoppo produttivo o operativo può rallentare la curva di adozione e danneggiare la credibilità del modello.
Competizione ed economia
CRSP compete con altre piattaforme CRISPR ma anche con farmaci tradizionali, anticorpi e RNA. Prezzi, rimborsabilità e comparatori efficaci possono limitare molto la penetrazione reale anche in presenza di buoni dati clinici.
In sintesi
CRISPR Therapeutics oggi è a metà strada tra presente e futuro: da un lato un prodotto reale, approvato, con percorsi di cura e rimborsi che si stanno consolidando; dall’altro una serie di programmi che, se funzionassero, cambierebbero pesantemente il modo di trattare autoimmuni, linfomi e rischio cardiovascolare.
Il quadro numerico attuale è quello di una biotech ancora in perdita, ma molto ben capitalizzata e con una pipeline ampia. Quanto questo giustifichi o meno la valutazione di mercato dipende dall’orizzonte di chi guarda, dalla tolleranza al rischio e dal giudizio personale sul gene editing come classe.
Qui l’obiettivo non è dire se il titolo “merita” di salire o scendere, ma offrire una mappa dei fatti disponibili e dei principali nodi aperti, così che ogni lettore possa farsi la propria idea.
Fonti principali
- Comunicati stampa CRISPR Therapeutics (Q3 2025, aggiornamenti su Casgevy, CTX310 e zugo-cel) e documenti SEC (Form 10-Q).
- Abstract, presentazioni congressuali e comunicazioni su CTX310/320 e SyNTase, inclusi dati AHA e NEJM per CTX310.
- Notizie e coverage su zugo-cel in autoimmuni e linfomi, inclusa la nuova collaborazione con Eli Lilly.
- Articolo Stocktwits sul sentiment retail dopo i dati CTX310 e flusso di messaggi su CRSP su Reddit/Stocktwits/X.
- Altre fonti di settore (media biotech e finanziari primari) per contesto competitivo e trend generali sul gene editing.
Alcuni link esterni utilizzati per grafici o dati (per esempio Finviz, Seeking Alpha, Stocktwits o strumenti di broker) possono contenere parametri di referral affiliati a Merlintrader. Questo non modifica il contenuto che vedi né il prezzo dei servizi, e non influenza in alcun modo le conclusioni dell’analisi.
Disclaimer legale e di rischio
Contenuto puramente informativo, non è una raccomandazione. Questo testo si basa su informazioni pubbliche disponibili al momento della stesura (filings, documenti regolatori, comunicati ufficiali, media di primaria affidabilità) e può contenere errori, omissioni o dati nel frattempo superati.
Nulla di quanto scritto costituisce invito o sollecitazione ad acquistare, vendere o detenere strumenti finanziari, né consulenza personalizzata. L’autore non è un consulente finanziario abilitato. Eventuali riferimenti a scenari, upside/downside o comportamenti di mercato sono solo esempi concettuali e non previsioni.
Chi legge deve svolgere la propria due diligence, valutare il proprio profilo di rischio e, se necessario, confrontarsi con un professionista abilitato. Le biotech ad alto contenuto innovativo, e in particolare il gene editing, comportano rischi elevati e la possibilità di perdere anche l’intero capitale.
Questo report è pensato per un pubblico internazionale, inclusi lettori in UE e USA, e adotta un linguaggio coerente con lo spirito delle linee guida CONSOB e SEC per contenuti informativi non promozionali.
Authors: Merlintrader and Jane.
Per note legali e privacy complete:
Disclaimer
Termini di Servizio, Privacy, Cookie Policy // Term of Service, Privacy, Cookie Policy
Biotech Catalyst Calendar
Per una panoramica aggiornata di PDUFA, letture di dati clinici e altri eventi regolatori chiave su biotech e healthcare, puoi fare riferimento alla pagina dedicata del Biotech Catalyst Calendar di Merlintrader.
Link diretto: https://merlintrader.com/calendario-catalyst/
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


