DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
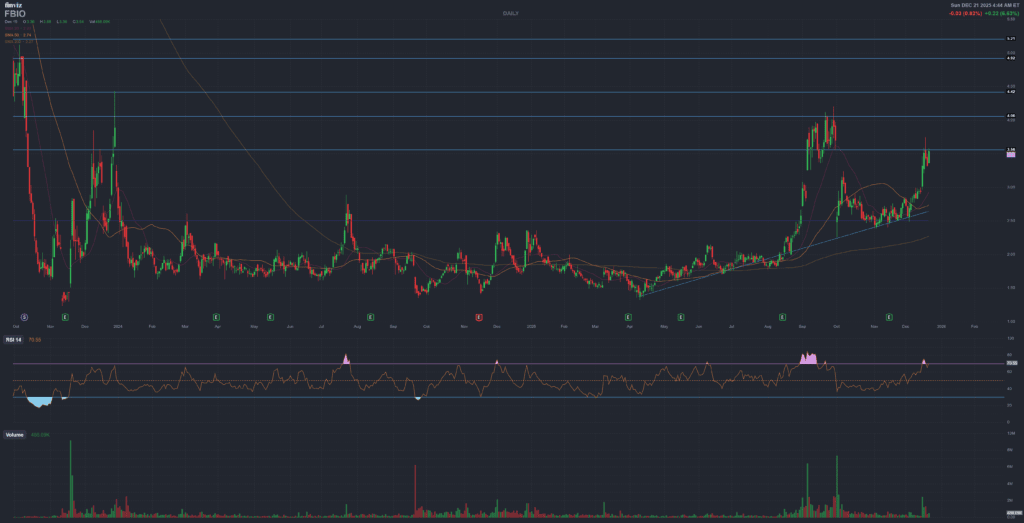
FBIO · Biotech · CUTX-101
Fortress Biotech (FBIO): 2025 Deep Dive on CUTX-101 and Opportunity
Bilingual report (EN/IT) with a full 2025 deep dive on Fortress Biotech, CUTX-101 for Menkes disease, the FDA CRL and new PDUFA date, financial profile, governance, analyst views, retail sentiment and market prospects, plus a clearly labeled personal speculative view (not investment advice).
Language / Lingua:
Company Overview and Pipeline
Fortress Biotech, Inc. (NASDAQ: FBIO) is a biopharmaceutical company operating with a multi-subsidiary, multi-partner model. The company acquires, develops and commercializes drugs through controlled or partnered entities, creating value via product revenues, equity stakes and royalties.
Fortress and its affiliates currently have eight prescription products on the market (mainly through dermatology arm Journey Medical) and several clinical and preclinical programs in oncology, rare diseases and gene therapy.
Key pipeline components (with a strong focus on CUTX-101):
- CUTX-101 (copper histidinate) – Copper replacement therapy for Menkes disease, an ultra-rare pediatric condition. Developed by Cyprium Therapeutics (a Fortress subsidiary), it is the flagship program right now: clinical data showed meaningful survival benefits when treatment is initiated early in life. The NDA has been filed with the FDA and granted Priority Review, now in the final regulatory phase.
- AAV-ATP7A gene therapy – A preclinical gene therapy approach for Menkes, designed to deliver a functional copy of the defective ATP7A gene. Cyprium holds exclusive rights to this AAV-based therapy (already granted orphan designation) and plans to combine it with CUTX-101 in the future.
- Dotinurad (Urica / Crystalys Therapeutics) – Next-generation oral URAT1 inhibitor for gout. Fortress licensed it out to startup Crystalys Therapeutics for equity plus royalties. In 2025 the program entered global phase 3 after Crystalys raised a 205 million dollar Series A round.
- Oncology (Mustang Bio and others) – Fortress owns stakes in companies like Mustang Bio, focused on CAR-T and gene therapies for cancer. Mustang’s MB-101, a CAR-T targeting IL13Rα2 for glioblastoma and other brain tumors, received Orphan Drug Designation from the FDA in July 2025.
- Dermatology (Journey Medical) – Subsidiary Journey markets several dermatology brands (Accutane®, Qbrexza®, Amzeeq®, Zilxi® and others). In 2025 it launched Emrosi™ (DFD-29), modified-release minocycline capsules for rosacea, which showed superior efficacy versus the standard of care (doxycycline/Oracea®).
In short, Fortress Biotech is a diversified platform with current revenue streams (primarily dermatology) and multiple future drivers from high-value clinical programs. The central focus today is CUTX-101 for Menkes disease, which could become the first approved treatment for this lethal pediatric disorder and unlock a valuable Rare Pediatric Disease Priority Review Voucher if approved.
Key 2025 Events: Detailed Timeline
March 2025 – Sun Pharma deal for Checkpoint Therapeutics
Fortress announces that subsidiary Checkpoint Therapeutics will be acquired by Sun Pharmaceutical. The deal (early March) includes $4.10 per share in cash plus a contingent value right (CVR) of $0.70 per share tied to future approvals, for a potential total value in the ~$255–355 million range.
Checkpoint had just received FDA approval for its anti-PD-L1 antibody cosibelimab (UNLOXCYT™) in December 2024. As majority shareholder, Fortress expects roughly $28 million upfront and a 2.5% royalty on future cosibelimab sales, plus up to $4.8 million via CVRs.
15 April 2025 – Governance change
Board member Lucy Lu, M.D. resigns from the Fortress Board to take up an operational role. As of 21 April 2025 she becomes the company’s Chief Strategy Officer (CSO). This is not a dispute but a move to strengthen internal strategic leadership at a key moment.
Late May 2025 – Checkpoint closing and PDUFA preparation
On 30 May 2025 the Checkpoint acquisition by Sun Pharma formally closes, following shareholder approval on 28 May. Fortress highlights the next major milestone on the horizon: the 30 September 2025 PDUFA date for CUTX-101.
At the same time, Fortress announces AI-related initiatives (Partex collaboration) to leverage machine learning platforms for future asset discovery.
June 2025 – Index rebalancing
FBIO is removed from some indices (for example the Russell Microcap). As usual, this triggers some mechanical selling and trading pressure but does not affect business fundamentals.
July 2025 – Orphan designation for MB-101
Subsidiary Mustang Bio receives Orphan Drug Designation from the FDA for CAR-T candidate MB-101, targeting brain tumors such as glioblastoma and diffuse astrocytoma. The designation grants benefits like tax credits and seven years of post-approval market exclusivity.
14 August 2025 – Q2 results and PDUFA coming into view
Fortress reports Q2 2025 results with growing revenues and reiterates the 30 September 2025 PDUFA for CUTX-101. Journey Medical begins the commercial launch of Emrosi™.
Management expresses confidence, pointing to the strength of the Fortress model and the contribution of the Checkpoint deal.
30 September 2025 – FDA CRL on CUTX-101
On the expected decision date, the FDA does not grant immediate approval and instead issues a Complete Response Letter (CRL). The news is made public on 1 October 2025.
Crucial point: the CRL does not challenge the efficacy or safety data. FDA comments are limited to cGMP observations at the manufacturing site for CUTX-101. No additional clinical trials are requested.
Cyprium and partner Sentynl Therapeutics state they will address the observations quickly and prepare a resubmission.
October 2025 – Dotinurad progress
Fortress and subsidiary Urica Therapeutics announce first patient dosed in global phase 3 studies of dotinurad for gout, following the 205 million dollar Series A financing at Crystalys. Fortress benefits through equity and future royalties without directly funding phase 3.
6 November 2025 – CNS asset monetization (Baergic/Axsome)
Avenue Therapeutics announces the sale of subsidiary Baergic Bio to Axsome Therapeutics. The deal includes a small upfront payment (around $0.3M) plus milestones up to roughly $79M linked to clinical and commercial success. Another example of Fortress monetizing non-core assets.
14 November 2025 – Q3 results and cash position
Fortress reports Q3 2025 results: consolidated net revenue grows +20.5% year-on-year to $17.6 million.
Thanks largely to the Checkpoint gain, the company posts a net profit attributable to common shareholders of $3.7 million ($0.13 per share) versus a $15 million loss a year earlier. Consolidated cash at 30 September 2025 stands at $86.2 million (up from $57.3 million at year-end 2024), of which roughly $38.6 million is directly attributable to Fortress (holding) and non-listed subsidiaries.
15 December 2025 – Resubmission and new PDUFA (14 January 2026)
In short order, Sentynl and Cyprium/Fortress announce that the CUTX-101 NDA resubmission has been filed and the FDA formally accepts it on 15 December.
The resubmission is classified as Class 1, implying a rapid two-month review, and a new PDUFA date of 14 January 2026 is set.
The FDA reiterates that the original CRL was driven solely by manufacturing issues and that responses and corrective actions have already been provided. No additional approvability concerns or deficiencies in the clinical package are raised.
The CRL for CUTX-101: Details and Implications
The Complete Response Letter (CRL) dated 30 September 2025 is central to the risk/reward angle around CUTX-101.
CRL rationale: manufacturing only, not the clinical data
The CRL focuses exclusively on cGMP deficiencies at the CUTX-101 manufacturing site.
No issues were identified in the efficacy or safety data: the CRL does not request new clinical trials and does not question the clinical benefit of copper histidinate in Menkes.
Corrective actions and Sentynl’s role
Even before the CRL, the manufacturer had submitted written responses to FDA inspection observations. After the CRL, Sentynl Therapeutics confirmed it would work closely with the Agency to address all matters promptly.
The Class 1 resubmission with a two-month review window is a strong signal that the regulator views the fixes as straightforward and well-documented.
New PDUFA and approval probabilities
The new PDUFA timing is 14 January 2026. Class 1 resubmissions typically do not require new Advisory Committees or long delays; the focus is on verifying updated manufacturing compliance.
Given that:
- the CRL does not touch efficacy/safety,
- no new trials are required,
- the review is fast-tracked (Class 1),
many observers consider the probability of approval on the second attempt to be high.
Impact on patients and strategic value
At present, Menkes patients have no approved therapy; the classic form has a life expectancy of roughly 2–3 years without treatment.
CUTX-101 would be the first approved treatment. Approval would also trigger a Rare Pediatric Disease Voucher, transferable and monetizable, often valued in the 90–110 million dollar range in secondary transactions.
Financial Profile and Dilution Risk
By the end of 2025, Fortress Biotech is financially stronger than in 2024, mainly thanks to the Checkpoint sale and better performance at Journey.
Cash and P&L snapshot
- Consolidated cash at 30 September 2025: $86.2 million, up from $57.3 million at year-end 2024.
- Of that, roughly $38.6 million is attributable directly to Fortress (holding) and private subsidiaries.
- Q3 2025 revenue: $17.6 million, +20.5% year-on-year.
- Q3 2025 net income: $3.7 million ($0.13 per share), driven primarily by the Checkpoint gain.
Journey Medical’s revenue base covers a good portion of operating expenses; the Checkpoint sale provided a one-off profit. On an underlying basis Fortress is still loss-making, but the cash burn is materially lower than at many pure-play R&D micro-cap biotechs.
Pre-PDUFA dilution risk
Analyst estimates suggest Fortress has roughly a 12-month cash runway, which reduces the need for immediate capital raises. That time frame comfortably covers the January 2026 PDUFA for CUTX-101.
Dilution risk is not zero: Fortress has flexible funding tools (ATM programs, warrants, convertible structures, etc.). A concrete example is the term loan amendment with Oaktree in December 2025: maturity pushed out to 2028, but Fortress granted warrants for 600,000 shares at $2.62.
Overall, however, there is no clear need for a large equity raise before PDUFA: the combination of cash, Journey revenues and potential milestones/royalties makes it plausible for Fortress to reach the regulatory decision using existing resources.
Governance and Recent Changes
Fortress Biotech is led by co-founder Dr. Lindsay A. Rosenwald (Chairman and CEO) and Michael S. Weiss (Executive Vice Chairman).
The Board in 2025 comprises seven members with scientific, financial and legal backgrounds. The main change is the move by Lucy Lu, M.D. from independent director to Chief Strategy Officer in April 2025.
Insider and long-term holders own a meaningful stake. At the 2025 annual meeting, all proposals, including director re-elections, were approved, signalling continued investor confidence in the leadership team.
Analyst Coverage and Target Prices
Analyst coverage is relatively narrow but clearly skewed to the Buy side. Key players include:
- H.C. Wainwright – Rating Buy. Target price cut from $26 to $17 in August 2025, while maintaining a constructive view on the business model and pipeline.
- Roth MKM – Rating Buy. Target lowered from $15 to $12 to account for more shares outstanding and revisions on some legacy assets (e.g. CAEL-101).
- Alliance Global Partners – Rating Buy, but more conservative. Target at $4.50 (from $4.00) after Q3 2025.
The 12-month target price average sits around $10–11 per share, implying roughly 200–300% upside versus prices around $3 at year-end 2025.
All firms highlight the same key driver: the CUTX-101 regulatory outcome. None of the active analysts recommend selling the stock; consensus is firmly in the Buy camp.
Retail Sentiment: Forums, Reddit and Fintwit
Before 30 September 2025 (PDUFA run-up)
On Reddit (r/pennystocks, r/biotech) and on Fintwit, sentiment was strongly bullish as the PDUFA approached. Several user DD posts highlighted:
- FDA Priority Review status and total unmet need in Menkes.
- Street price targets in the 12–16 dollar range as a reference for upside.
- Asymmetric risk/reward: small speculative positions for potential multi-bagger outcomes.
Users often warned against “betting the house on a biotech”, but the skew was clearly optimistic.
After the CRL (October 2025)
The CRL triggered shock and an immediate sell-off (over −30% intraday). Some retail traders capitulated in frustration, while others quickly pointed out that the CRL was manufacturing-only.
Discussion threads compared this to historical “technical CRL” cases that later ended in approvals. Many users reported adding to positions on the drop, viewing the reaction as overdone relative to the actual issue.
Resubmission and the new PDUFA
The acceptance of the resubmission with a new PDUFA on 14 January 2026 re-ignited optimism. Within the community, FBIO is now seen as:
- a “second chance” setup on a drug that works, with only administrative hurdles;
- a stock still trading below pre-CRL levels, effectively “discounted” pre-catalyst;
- a story with a somewhat lower financial risk than many micro-cap biotechs, thanks to Journey and the 2025 asset sales.
Overall mood is one of cautious optimism: rising confidence that the CRL was a technical bump, but full awareness that the upcoming FDA decision remains a binary event.
Market Prospects for CUTX-101 (Menkes)
Market size: ultra-rare but high-value
Menkes disease is extremely rare: estimated incidence between 1/34,800 and 1/8,700 live male births. In absolute terms that translates into just a few dozen new cases per year in the United States, with prevalence potentially rising as survival improves under treatment.
Taking into account:
- an ultra-rare disease setting,
- no approved therapies today,
- a very meaningful clinical impact,
it is reasonable to expect a very high annual price per patient (often 150–200k dollars or more for ultra-orphan biologics). With 100–200 patients on therapy across the US and other developed markets, annual peak sales could land in the $50–100 million range.
Competition and first-mover edge
At this point there are no approved competitors. Current approaches are purely supportive or investigational, with clearly inferior efficacy.
CUTX-101 (copper histidinate) is engineered to optimize copper delivery into the nervous system. Clinical data show a marked survival benefit when treatment is started early.
Fortress/Cyprium have:
- Orphan Drug Designation and associated market exclusivity;
- established ties with Menkes centres of excellence (NIH and leading specialists);
- a dedicated commercial partner (Sentynl) with rare-disease experience.
Potential future competitors
There are early programs in gene therapy (including Cyprium’s own AAV-ATP7A project) and academic work on copper-transporting molecules (e.g. elesclomol plus copper, still preclinical).
These approaches are years away and, if successful, are likely to be complementary rather than fully substitutive to CUTX-101.
Rare Pediatric Disease Voucher (PRV)
With CUTX-101 approval, Cyprium would receive a Rare Pediatric Disease Voucher, transferable and saleable. Historically these vouchers have changed hands in the roughly 90–110 million dollar range.
Fortress/Cyprium can either:
- sell it and immediately secure a nine-figure cash inflow; or
- use it internally to fast-track a future NDA.
In both cases, the PRV is a central part of the value equation of CUTX-101, often worth almost as much as the discounted value of future Menkes sales.
Other Relevant Details and Secondary Events
Monetisation and strategic disposals
2025 saw two major exit events:
- Sale of Checkpoint Therapeutics to Sun Pharma (cosibelimab/UNLOXCYT™), with upfront cash and future royalties.
- Sale of Baergic Bio to Axsome (CNS asset) with a small upfront but milestones potentially up to $79 million.
These transactions validate the Fortress model: develop, de-risk and monetise assets through larger partners.
Journey Medical (DERM): commercial performance
Journey continues to expand its dermatology portfolio (Accutane®, Qbrexza®, Amzeeq®, Zilxi®, Emrosi™). In 2025:
- Launch of Emrosi™ with efficacy data superior to the standard of care.
- Broader payer coverage and revenue growth, contributing meaningfully to Fortress’ consolidated top line.
Additional R&D programs
- Caelum / CAEL-101: now heavily de-risked downward after disappointing clinical results; some analysts like Roth effectively write this out of their models.
- Mustang Bio: restructuring and refocus on gene therapy for SCID and CAR-T; cash appears adequate to run current trials.
- Other internal assets (Helocyte, Cellvation, etc.) are quiet for now, representing long-dated option value.
Preferred shares FBIOP
Fortress also has preferred shares (FBIOP) outstanding with a 9.375% coupon. In 2025 these traded at a discount to par but staged a strong rally into December, suggesting that credit-sensitive investors are starting to price a lower perceived risk of missed distributions.
Post-approval strategy (hypothetical)
If CUTX-101 is approved, Fortress could:
- sell the PRV and effectively solve the “cash problem” for several years;
- consider spinoffs or further integration across subsidiaries (Cyprium, Journey, etc.);
- increase stakes in promising affiliates like Mustang if risk/reward is attractive;
- reduce debt (e.g. Oaktree loan) and de-risk the capital structure.
All of this, however, hinges on the central assumption: CUTX-101 approval.
Personal speculative view on FBIO
The following is purely personal and speculative. It is not, in any way, investment advice.Based on publicly available information, the 30 September 2025 CRL on CUTX-101 appears “light” and focused only on manufacturing (cGMP) aspects, without challenging the efficacy or safety data.
Considering:
- the technical and fixable nature of FDA’s requests,
- the speed of the Class 1 resubmission (two-month review window),
- the very high unmet need (no approved Menkes therapies),
my personal view is that the probability of CUTX-101 approval on 14 January 2026 is high.
If the FDA approves the drug:
- Fortress/Cyprium will receive a PRV that alone could be worth close to the current market cap.
- The market will start to price in a recurring revenue stream from CUTX-101 (ultra-rare but high price per patient).
- The perceived risk profile shifts from “speculative micro-cap” to “platform with an approved product and strengthened balance sheet”.
Speculatively, in an approval scenario, I can imagine FBIO:
- at least revisiting the pre-CRL highs,
- and, if the market fully values PRV plus expected sales and the multi-asset model, potentially moving materially higher over the medium term.
This is only a personal, illustrative view. I am not a financial advisor, this is not a recommendation, and anyone considering the stock should perform their own analysis and always factor in the possibility of a total loss on any single biotech position.
Note: this deep dive is meant as a study and information base. Data and interpretations can change as new company or FDA communications emerge; for any trading or investment decisions, always rely on up-to-date sources and your own risk assessment.
Panoramica dell’Azienda e Pipeline
Fortress Biotech, Inc. (NASDAQ: FBIO) è una società biofarmaceutica con un modello particolare basato su più partner company e sussidiarie. L’azienda acquisisce, sviluppa e commercializza farmaci attraverso entità controllate o partecipate, generando valore tramite ricavi da prodotti, partecipazioni azionarie e royalty.
Attualmente Fortress e le sue controllate hanno otto farmaci da prescrizione già sul mercato (soprattutto in dermatologia, tramite la controllata Journey Medical), e diversi candidati in sviluppo in aree come oncologia, malattie rare e terapie geniche.
Componenti chiave della pipeline (con focus su CUTX-101):
- CUTX-101 (rame istidinato) – Terapia sostitutiva del rame per la malattia di Menkes, patologia pediatrica ultra-rara. Sviluppato da Cyprium Therapeutics (controllata Fortress), è il programma di punta attuale: ha completato gli studi clinici mostrando miglioramenti significativi nella sopravvivenza se il trattamento inizia precocemente. Il farmaco ha ricevuto Priority Review dalla FDA ed è in fase regolatoria avanzata.
- AAV-ATP7A (terapia genica) – Approccio genico sperimentale per Menkes in sviluppo preclinico, destinato a fornire ai pazienti una copia funzionante del gene difettoso ATP7A. Cyprium possiede i diritti esclusivi su questa terapia AAV (già designata orphan drug dalla FDA) e prevede in futuro un utilizzo combinato con CUTX-101.
- Dotinurad (Urica / Crystalys Therapeutics) – Farmaco orale (inibitore URAT1) di nuova generazione per la goccia. Fortress ne ha ceduto la licenza alla startup Crystalys Therapeutics in cambio di equity e royalty. Nel 2025 il programma è entrato in fase 3 globale grazie a un round Serie A da 205 milioni di dollari.
- Terapie oncologiche (Mustang Bio e altre) – Fortress detiene partecipazioni in società come Mustang Bio, focalizzata su CAR-T e terapie geniche oncologiche. Mustang sta sviluppando, ad esempio, MB-101, una CAR-T contro IL13Rα2 per il glioblastoma e altri tumori cerebrali, che ha ottenuto la designazione di farmaco orfano dalla FDA a luglio 2025.
- Dermatologia (Journey Medical) – La controllata Journey commercializza vari farmaci dermatologici (Accutane®, Qbrexza®, Amzeeq®, Zilxi® e altri). Nel 2025 Journey ha lanciato Emrosi™ (DFD-29), capsule orali (minociclina a rilascio modificato) per la rosacea, con dati clinici superiori rispetto alla terapia standard (doxiciclina/Oracea®).
In sintesi, Fortress Biotech presenta un portafoglio diversificato con ricavi attuali (dal business dermatologico) e opportunità future legate a farmaci innovativi in fase avanzata. L’enfasi maggiore è su CUTX-101 per il Morbo di Menkes, che può diventare il primo trattamento approvato per questa malattia devastante e generare anche un prezioso Priority Review Voucher pediatrico in caso di approvazione.
Eventi Significativi del 2025: Timeline Dettagliata
Marzo 2025 – Accordo con Sun Pharma per Checkpoint Therapeutics
Fortress annuncia che la controllata Checkpoint Therapeutics sarà acquisita da Sun Pharmaceutical. L’accordo (inizio marzo) prevede 4,10 dollari per azione Checkpoint in contanti, più un diritto a valore contingente di 0,70 dollari per azione legato a future approvazioni, per un valore complessivo fino a circa 255–355 milioni di dollari.
Checkpoint era reduce dall’approvazione FDA del proprio farmaco anti-PD-L1 cosibelimab (UNLOXCYT™) a dicembre 2024. Fortress, come azionista di maggioranza, incassa circa 28 milioni di dollari upfront e avrà una royalty del 2,5% sulle vendite future di cosibelimab, oltre a CVR fino a 4,8 milioni.
15 aprile 2025 – Cambio nella Governance
La Dott.ssa Lucy Lu, membro del CdA di Fortress Biotech, rassegna le dimissioni dal Board per assumere un ruolo operativo. Dal 21 aprile 2025 entra in azienda come Chief Strategy Officer (CSO). Non si tratta di un disaccordo, ma di un rafforzamento della leadership strategica.
Fine maggio 2025 – Chiusura vendita Checkpoint e preparazione PDUFA
Il 30 maggio 2025 viene perfezionata la cessione di Checkpoint a Sun Pharma, dopo il voto favorevole degli azionisti del 28 maggio. Fortress ribadisce l’importanza della prossima data chiave: PDUFA 30 settembre 2025 per CUTX-101.
Contestualmente vengono annunciate iniziative in ambito AI (collaborazione con Partex) per sfruttare piattaforme di intelligenza artificiale nella scoperta di nuovi asset.
Giugno 2025 – Movimenti di indice
Il titolo FBIO esce dalla composizione di alcuni indici (ad esempio il Russell Microcap). Come spesso accade nei ribilanciamenti, ciò genera un po’ di pressione tecnica in vendita, ma non incide sui fondamentali dell’azienda.
Luglio 2025 – Designazione Orfana per MB-101
La controllata Mustang Bio riceve dalla FDA la Orphan Drug Designation per la CAR-T MB-101 rivolta ai tumori cerebrali (glioblastoma e astrocitomi diffusi). Il riconoscimento porta benefici come esenzioni fiscali e 7 anni di esclusività post-approvazione.
14 agosto 2025 – Risultati Q2 e PDUFA in vista
Fortress pubblica i risultati del secondo trimestre 2025, con ricavi in crescita e promemoria della PDUFA del 30 settembre 2025 per CUTX-101. Journey Medical avvia il lancio commerciale di Emrosi™.
Il management si mostra fiducioso, sottolineando le basi solide del modello Fortress e il contributo della vendita di Checkpoint.
30 settembre 2025 – CRL FDA su CUTX-101
Alla data attesa, la FDA non approva immediatamente CUTX-101 e invia una Complete Response Letter (CRL). La notizia viene resa pubblica il 1º ottobre 2025.
Punto chiave: la CRL non mette in dubbio efficacia o sicurezza del farmaco. Le richieste dell’FDA sono legate solo a osservazioni cGMP (Good Manufacturing Practice) presso il sito produttivo di CUTX-101. Non vengono richiesti studi clinici aggiuntivi.
Cyprium e il partner Sentynl Therapeutics dichiarano di voler affrontare rapidamente le osservazioni e preparare una nuova sottomissione.
Ottobre 2025 – Avanzamento dotinurad
Fortress e la controllata Urica Therapeutics annunciano il dosaggio dei primi pazienti negli studi globali di fase 3 su dotinurad per la goccia, dopo il finanziamento Serie A da 205 milioni di dollari ottenuto da Crystalys. Fortress beneficerà di equity e royalty senza finanziare direttamente la fase 3.
6 novembre 2025 – Monetizzazione asset CNS (Baergic/Axsome)
Avenue Therapeutics annuncia la vendita della controllata Baergic Bio ad Axsome Therapeutics. L’accordo prevede un pagamento upfront di circa 0,3 milioni di dollari più milestone fino a 79 milioni complessivi, legate a esiti clinici e commerciali. È un ulteriore esempio di monetizzazione di asset non-core.
14 novembre 2025 – Risultati Q3 e posizione di cassa
Fortress pubblica i risultati del terzo trimestre 2025: il fatturato netto consolidato cresce del +20,5% anno su anno a 17,6 milioni di dollari.
Grazie soprattutto alla plusvalenza per la vendita di Checkpoint, la società registra un utile netto attribuibile agli azionisti comuni di 3,7 milioni di dollari (0,13 dollari per azione), contro una perdita di 15 milioni l’anno prima. La cassa consolidata al 30/9/2025 è di 86,2 milioni, rispetto ai 57,3 milioni di fine 2024, di cui circa 38,6 milioni attribuibili direttamente a Fortress e sussidiarie non quotate.
15 dicembre 2025 – Resubmission e nuova PDUFA (14 gennaio 2026)
A tempo record, Sentynl e Cyprium/Fortress annunciano che la resubmission della NDA per CUTX-101 è stata inviata e la FDA la accetta ufficialmente il 15 dicembre.
La resubmission viene classificata come Classe 1 (review rapida in 2 mesi) e viene fissata la nuova data PDUFA al 14 gennaio 2026.
Viene ribadito che la CRL del 30 settembre era dovuta esclusivamente a problemi di produzione e che le risposte correttive sono state già fornite alla FDA. La CRL non citava altre problematiche di approvabilità né deficit nei dati clinici.
La Complete Response Letter per CUTX-101: Dettagli e Implicazioni
La Complete Response Letter (CRL) del 30 settembre 2025 su CUTX-101 è centrale per capire il rischio/opportunità dell’investimento.
Motivazione della CRL: solo produzione, non i dati clinici
La CRL cita esclusivamente carenze relative alle norme di Buona Fabbricazione (cGMP) nel sito produttivo di CUTX-101.
Nessun problema è stato riscontrato nei dati di efficacia o sicurezza: la CRL non richiede nuovi studi e non mette in dubbio l’impatto clinico della terapia.
Interventi correttivi e ruolo di Sentynl
Già prima della CRL il produttore aveva inviato risposte scritte alla FDA sulle osservazioni emerse. Dopo la CRL, Sentynl Therapeutics ha comunicato di voler lavorare a stretto contatto con l’Agenzia per sistemare tutto in tempi rapidi.
La classificazione della resubmission come Classe 1 con review di 2 mesi è un segnale che le correzioni sono considerate semplici e ben documentate.
Nuova PDUFA e probabilità di approvazione
La nuova PDUFA è fissata al 14 gennaio 2026. Una resubmission di Classe 1 di solito non comporta ulteriori comitati o ritardi, trattandosi soprattutto di verificare la conformità produttiva aggiornata.
Dato che:
- la CRL non tocca efficacia/sicurezza,
- non sono richiesti nuovi trial,
- la review è rapida (Classe 1),
molti osservatori ritengono che le probabilità di approvazione al secondo tentativo siano elevate.
Impatto sui pazienti e sul valore strategico
Attualmente i pazienti con malattia di Menkes non hanno alcun trattamento approvato, e l’aspettativa di vita nella forma classica è di 2–3 anni senza terapia.
CUTX-101 sarebbe il primo trattamento disponibile. L’approvazione porterebbe anche a un Rare Pediatric Disease Voucher, trasferibile e monetizzabile, di valore potenzialmente vicino ai 90–110 milioni di dollari.
Situazione Finanziaria di Fortress Biotech e Rischio di Diluizione
A fine 2025, Fortress Biotech è finanziariamente più solida rispetto al 2024 grazie a varie operazioni (soprattutto la vendita di Checkpoint).
Posizione di cassa e conto economico
- Cassa consolidata al 30/9/2025: 86,2 milioni di dollari, rispetto ai 57,3 milioni di fine 2024.
- Di questi, circa 38,6 milioni sono attribuibili direttamente a Fortress (holding) e a sussidiarie non quotate.
- Ricavi Q3 2025: 17,6 milioni di dollari, +20,5% anno su anno.
- Utile netto Q3 2025: 3,7 milioni di dollari (0,13 dollari per azione), grazie in gran parte alla plusvalenza Checkpoint.
I ricavi di Journey Medical coprono buona parte dei costi operativi; la vendita di Checkpoint ha dato un boost straordinario. Al netto degli eventi una tantum, Fortress sarebbe comunque in perdita, ma con cash burn ridotto rispetto a molte biotech puramente R&D.
Rischio di diluizione pre-PDUFA
Stime di analisti indicano che Fortress ha una runway di circa 12 mesi, riducendo l’urgenza di raccogliere capitale nel brevissimo termine. Questo copre comodamente l’orizzonte della PDUFA di gennaio 2026.
Il rischio di diluizione non è azzerato: la società dispone di strumenti flessibili (ATM, warrant, debito convertibile, ecc.). Un esempio è l’emendamento del term loan con Oaktree a dicembre 2025: estensione della scadenza al 2028, ma con concessione di warrant per 600.000 azioni a 2,62 dollari.
In generale, però, nel breve pre-PDUFA non sembra necessaria una grossa emissione: la combinazione di cassa, ricavi Journey e possibili milestone/royalty rende plausibile arrivare fino all’evento regolatorio con le risorse esistenti.
Governance e Cambiamenti Recenti
Fortress Biotech è guidata dal co-fondatore Dr. Lindsay A. Rosenwald (Presidente e CEO) e da Michael S. Weiss (Executive Vice Chairman).
Il Board nel 2025 è composto da 7 membri con background scientifico, finanziario e legale. Il cambiamento principale è la transizione di Lucy Lu, M.D., da consigliere indipendente a Chief Strategy Officer ad aprile 2025.
L’assetto azionario vede una quota rilevante in mano a insider e investitori di lungo periodo. Nel 2025 tutte le proposte all’assemblea annuale sono state approvate, inclusa la rielezione degli amministratori, segno di fiducia nella leadership.
Opinioni degli Analisti e Target Price sul Titolo FBIO
La copertura analisti su FBIO è limitata ma orientata al “Buy”. Tra le principali case:
- H.C. Wainwright – Rating Buy. Target price rivisto da 26 a 17 dollari ad agosto 2025, pur mantenendo una view molto positiva su modello e pipeline.
- Roth MKM – Rating Buy. Target ridotto da 15 a 12 dollari per tenere conto di più azioni in circolazione e di revisioni su altri asset (come CAEL-101).
- Alliance Global Partners – Rating Buy, approccio più prudente. Target a 4,50 dollari (da 4,00) dopo Q3 2025.
La media dei target a 12 mesi si aggira intorno a 10–11 dollari, corrispondenti a un potenziale upside di circa 200–300% rispetto ai livelli intorno a 3 dollari di fine 2025.
Tutti sottolineano che il catalizzatore chiave è l’esito regolatorio di CUTX-101. Nessun analista coprente consiglia vendita; il consenso è chiaramente orientato su “comprare”.
Sentiment del Retail: Forum, Reddit e “Fintwit”
Prima del 30 settembre 2025 (attesa PDUFA)
Su Reddit (r/pennystocks, r/biotech) e su Fintwit, il sentiment era molto positivo man mano che ci si avvicinava alla PDUFA. Diverse due diligence evidenziavano:
- Priority review FDA e contesto di unmet need totale in Menkes.
- Price target elevati (12–16 dollari) come riferimento di upside.
- Profilo di rischio/rendimento “asimettrico”: piccola posizione per potenziale multi-bagger.
Non mancavano avvertimenti tipo “non scommettere la casa su una biotech”, ma il bias era nettamente rialzista.
Dopo la CRL (ottobre 2025)
La CRL ha causato shock e sell-off immediato (calo di oltre il 30% intraday). Alcuni retail hanno abbandonato la posizione in perdita, altri però hanno fatto notare subito che la CRL era legata solo alla produzione, non al farmaco.
Sui forum sono comparsi confronti con altri casi storici di CRL “tecniche” poi seguite da approvazioni. Molti hanno dichiarato di aver aumentato la posizione sul crollo, considerandolo un eccesso di reazione.
Con la resubmission e la nuova PDUFA
L’accettazione della resubmission con nuova PDUFA al 14 gennaio 2026 ha riacceso l’ottimismo. La community vede ora FBIO come:
- “second chance” su un farmaco che funziona, con problemi solo amministrativi;
- titolo ancora sotto i livelli pre-CRL, quindi “a sconto” pre-catalyst;
- profilo finanziario meno rischioso di molte altre micro-cap biotech (grazie a Journey e alle exit).
Il sentiment attuale è di cauto ottimismo: fiducia crescente sul fatto che la CRL fosse un intoppo tecnico, ma consapevolezza del rischio binario fino alla decisione FDA.
Prospettive di Mercato per CUTX-101 (Menkes)
Dimensione del mercato: ultra-raro ma ad alto valore
La malattia di Menkes è rarissima: incidenza stimata tra 1/34.800 e 1/8.700 nati maschi. In termini assoluti si parla di poche decine di casi l’anno negli Stati Uniti, ma con potenziale incremento della prevalenza se la terapia prolunga la sopravvivenza.
Considerando:
- malattia ultra-rara,
- nessuna terapia approvata,
- impatto clinico molto importante,
è realistico ipotizzare un prezzo annuo molto elevato per paziente (tipicamente 150–200k dollari o più). Con 100–200 pazienti in terapia tra USA e altre regioni sviluppate, il mercato potenziale potrebbe essere nell’ordine di 50–100 milioni di dollari l’anno.
Concorrenza e vantaggio first-mover
Attualmente non esistono terapie approvate concorrenti. Gli approcci in uso sono solo supportivi o sperimentali, con efficacia molto inferiore.
CUTX-101 (rame istidinato) è progettato per massimizzare l’assorbimento del rame nel sistema nervoso. Nei trial ha dimostrato un miglioramento netto della sopravvivenza se somministrato precocemente.
Fortress/Cyprium dispongono di:
- Orphan Drug Designation e relativa esclusività commerciale;
- collaborazioni con centri di eccellenza (NIH, specialisti Menkes);
- un partner commerciale dedicato (Sentynl) con esperienza in malattie rare.
Possibili futuri competitor
Esistono progetti in campo terapia genica (incluso il programma AAV-ATP7A interno a Cyprium) e ricerche accademiche su molecole trasportatrici di rame (es. elesclomol+copper, ancora in fase preclinica).
Questi approcci sono distanti dal mercato e, in ogni caso, potrebbero risultare complementari a CUTX-101 più che sostitutivi.
Rare Pediatric Disease Voucher (PRV)
Con l’approvazione di CUTX-101, Cyprium otterrà un Rare Pediatric Disease Voucher, trasferibile e vendibile. Storicamente questi voucher vengono scambiati in un range di circa 90–110 milioni di dollari.
Fortress/Cyprium potranno:
- venderlo per incassare subito una cifra a nove zeri;
- oppure usarlo internamente su un’altra NDA futura.
In entrambi i casi, il PRV è un pezzo rilevante della equation di valore di CUTX-101, spesso quasi grande quanto il valore attuale dei ricavi del farmaco stesso.
Altri Dettagli Rilevanti e Eventi Secondari
Monetizzazione e cessioni strategiche
Il 2025 ha visto due exit importanti:
- Vendita di Checkpoint Therapeutics a Sun Pharma (cosibelimab/UNLOXCYT™) con incasso upfront e royalty future.
- Vendita di Baergic Bio ad Axsome (asset CNS) con upfront ridotto ma milestone potenzialmente fino a 79 milioni di dollari.
Queste operazioni confermano il modello Fortress: sviluppare, valorizzare e monetizzare asset tramite partner più grandi.
Journey Medical (DERM): performance commerciale
Journey continua ad ampliare la sua gamma in dermatologia (Accutane®, Qbrexza®, Amzeeq®, Zilxi®, Emrosi™). Nel 2025:
- Lancio di Emrosi™ con dati di efficacia superiori allo standard.
- Crescita della copertura assicurativa e dei ricavi, contribuendo in modo significativo al fatturato Fortress.
Altri programmi R&D
- Caelum / CAEL-101: opzione ora molto ridimensionata dopo dati clinici deludenti; analisti come Roth hanno sostanzialmente azzerato questa voce nei modelli.
- Mustang Bio: ristrutturazione e focus su terapie geniche per SCID e CAR-T; cassa adeguata per i trial in corso.
- Altri asset interni (Helocyte, Cellvation, ecc.) sono per ora più silenziosi, con potenziale valore opzionale di lungo termine.
Azioni preferenziali FBIOP
Fortress ha in circolazione anche azioni preferred (FBIOP) con cedola 9,375%. Nel 2025 hanno tradato a sconto rispetto alla parità, con un forte rally a dicembre, segnale che il mercato sta iniziando a prezzare in modo più positivo la capacità di Fortress di sostenere i pagamenti cedolari.
Strategie post-approvazione (ipotetiche)
In caso di approvazione di CUTX-101, Fortress potrebbe:
- vendere il PRV e azzerare di fatto il problema “cassa” per anni;
- valutare spinoff o integrazione di alcune controllate (es. Cyprium, Journey);
- rafforzare il buy-in su Mustang o altre affiliate con progetti interessanti;
- ridurre debito (es. loan con Oaktree) e alleggerire il rischio di struttura di capitale.
Tutto questo poggia però sul presupposto fondamentale: approvazione di CUTX-101.
Speculazione personale sull’opportunità FBIO
Quanto segue è una valutazione puramente personale e speculativa. Non è, in nessun modo, un consiglio di investimento.Alla luce della documentazione disponibile, la CRL del 30 settembre 2025 su CUTX-101 è stata “leggera” e focalizzata solo su aspetti produttivi (cGMP), senza mettere in discussione i dati di efficacia o sicurezza del farmaco.
Considerando:
- la natura tecnica e risolvibile delle richieste FDA,
- la rapidità con cui è stata accettata la resubmission (Classe 1, review di 2 mesi),
- i bisogni clinici enormi (nessuna terapia approvata per Menkes),
ritengo personalmente che le probabilità di approvazione di CUTX-101 il 14 gennaio 2026 siano molto alte.
Se la FDA approverà il farmaco:
- Fortress/Cyprium otterranno un PRV rivendibile, che da solo potrebbe valere quasi quanto l’attuale capitalizzazione di mercato.
- Il mercato inizierà a prezzare un flusso di ricavi ricorrenti da CUTX-101 (malattia ultra-rara ma prezzo/paziente elevato).
- La percezione del rischio su Fortress cambierà radicalmente: da “micro-cap speculativa” a “piattaforma con prodotto approvato e cassa rafforzata”.
Speculativamente, in uno scenario di approvazione vedo plausibile che il titolo FBIO possa:
- tornare almeno in area massimi pre-CRL,
- e, se il mercato valuta pienamente PRV più vendite attese e modello multi-asset, spingersi anche sensibilmente oltre nel medio periodo.
Questa è solo una lettura speculativa, condivisa nel report a fini informativi. Non sono un consulente finanziario, non si tratta di una raccomandazione, e chiunque valuti il titolo dovrebbe fare le proprie analisi e considerare sempre la possibilità di perdita totale del capitale investito in un singolo titolo biotech.
Nota: questo report è pensato come base informativa e di studio. Dati e interpretazioni possono cambiare con nuove comunicazioni da parte della società o dell’FDA; per decisioni operative vanno sempre considerate fonti aggiornate e un’analisi personale del profilo di rischio.
Biotech Catalyst Calendar
EN: For an updated overview of upcoming FDA catalysts, clinical readouts and key dates in the biotech space, you can check the dedicated page: Biotech Catalyst Calendar – full overview
IT: Per una panoramica aggiornata dei prossimi catalyst FDA, dati clinici e date chiave nel biotech, puoi consultare la pagina dedicata: Biotech Catalyst Calendar – panoramica completa
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


