DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
Single-Ticker Deep Dive – SGMO
Sangamo Therapeutics (SGMO) – Fabry BLA vs. Cash Crunch
Full dossier on Sangamo Therapeutics (NASDAQ: SGMO) as of 18 December 2025: Fabry gene therapy ST-920, neurology pivot, cash and dilution, Nasdaq listing risk, analyst and retail sentiment, and scenario analysis including a hypothetical bullish path if the Fabry BLA is accepted for review.
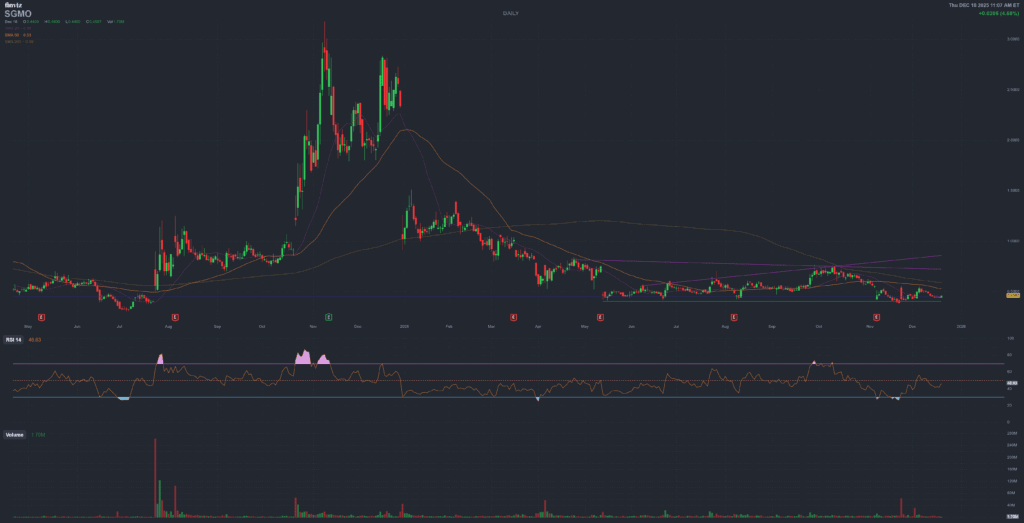
Price & Technical Snapshot
Intraday reference
Chart source: Finviz , intraday snapshot around 18 December 2025. For updated data always refer to live sources.
1. Executive Summary
Sangamo Therapeutics is a genomic medicine company whose current equity story is highly concentrated on a single near-term driver: ST-920, a gene therapy for Fabry disease now in a rolling Biologics License Application (BLA) submission to the U.S. FDA. On 18 December 2025 the company announced that it has initiated the rolling submission of the BLA for ST-920 and expects to complete it by the second quarter of 2026.
At the same time, Sangamo sits in a fragile financial position: cash and equivalents were $29.6M at 30 September 2025, with management stating that this runway extends only into the first quarter of 2026, helped by a $6M payment from Pfizer and proceeds from an at-the-market program. The company recently obtained an extension from Nasdaq until 27 April 2026 to cure its minimum bid price deficiency, after trading below $1.00 per share for an extended period.
The neurology pivot (ST-503 for small fiber neuropathy and ST-506 for prion disease) plus the STAC-BBB blood-brain barrier capsid platform with partners such as Genentech, Astellas and Eli Lilly represent medium- to long-term optionality, but they are not near-term cash generators at current stages.
The key question is therefore simple and binary: can Sangamo navigate the next 12–24 months without destroying shareholder value through aggressive financing or losing its listing, while advancing ST-920 through BLA acceptance and review. A scenario where the BLA is fully accepted for review and the company secures a Fabry commercialization partner would represent a clearly more bullish setup than today, but this remains hypothetical at this stage and subject to both regulatory and execution risk.
2. Company Snapshot & Business Model
Sangamo Therapeutics (NASDAQ: SGMO) describes itself as a genomic medicine company developing gene therapies and epigenetic regulators mainly for rare diseases and neurology indications.
Core business pillars
- Fabry gene therapy – ST-920: wholly owned AAV-based liver-directed gene therapy designed to durably increase alpha-galactosidase A (α-Gal A) levels, with the goal of replacing chronic enzyme replacement therapy and modifying multi-organ Fabry disease.
- Neurology portfolio – ST-503 and ST-506: epigenetic regulators targeting small fiber neuropathy (ST-503) and prion disease (ST-506), delivered using the proprietary STAC-BBB capsid platform.
- Platform monetization – STAC-BBB capsid & legacy collaborations: out-licensing and capsid-based partnerships with major pharma companies (Genentech, Astellas, Eli Lilly) with large potential milestones, alongside legacy collaborations and licenses.
The current revenue profile is dominated by collaboration revenues, which dropped sharply in 2025 due to the winding down of prior large collaborations. Q3 2025 revenues were only about $0.6M, versus $49.4M in the same quarter of 2024 when Genentech revenue was still recognized.
4. Pipeline & Key Programs
4.1 ST-920 (Fabry disease) – registrational program and BLA
ST-920 is Sangamo’s wholly owned gene therapy candidate for adults with Fabry disease. It delivers a functional GLA gene to the liver with the goal of driving sustained α-Gal A expression and reducing or eliminating the need for enzyme replacement therapy (ERT).
The registrational Phase 1/2 STAAR study has generated extensive data presented in 2025, including:
- Positive mean annualized eGFR slope at 52 weeks across all 32 dosed patients, with supportive slopes at 104 weeks in the subset with longer follow-up.
- Stable cardiac parameters (LVM, LVMI, GLS, T1/T2 mapping, volumetric measures) over at least one year.
- Durable elevation of α-Gal A activity, with the longest treated patient followed for up to 4.5 years.
- Withdrawal from ERT in all patients who started the study on ERT, with plasma lyso-Gb3 levels remaining generally stable after withdrawal.
- Improvement in Fabry Outcome Survey–adapted Mainz Severity Score Index (FOS-MSSI) and quality-of-life scores (SF-36, GSRS) for many patients.
- Favorable safety and tolerability profile without the need for preconditioning.
The FDA agreed to use eGFR slope at 52 weeks as the primary endpoint to support an accelerated approval pathway for ST-920 in Fabry, and this was reconfirmed in 2025 meeting minutes.
On 18 December 2025, Sangamo announced that it has initiated a rolling BLA submission to the U.S. FDA for ST-920 and expects to complete the submission by Q2 2026. A rolling BLA allows sections of the application to be submitted and reviewed as they are ready, but does not, by itself, mean that the BLA has been accepted for full review.
4.2 ST-503 – chronic neuropathic pain (small fiber neuropathy)
ST-503 is an investigational epigenetic regulator targeting voltage-gated sodium channel Nav1.7 and is being developed for intractable pain due to small fiber neuropathy (SFN).
- Phase 1/2 STAND study in chronic neuropathic pain: clinical sites activated and patient recruitment ongoing.
- Nonclinical data in 2025 demonstrate durability, potency and selectivity in non-human primates with a favorable safety profile.
- On 3 December 2025 the FDA granted Fast Track designation to ST-503 for SFN.
Sangamo expects first patient dosing soon and does not anticipate meaningful efficacy readouts before late 2026, making this a medium-term rather than near-term catalyst.
4.3 ST-506 – prion disease
ST-506 is an epigenetic regulator for prion disease using the STAC-BBB capsid to deliver treatment across the blood-brain barrier.
- CTA-enabling work ongoing with alignment on CMC strategy from the UK MHRA.
- Preclinical data in prion models show profound survival extension and robust prion reduction.
- CTA submission is targeted for mid-2026, according to company guidance.
4.4 STAC-BBB platform and partnered programs
Sangamo’s STAC-BBB capsid technology underpins multiple partnered initiatives with companies such as Genentech, Astellas and Eli Lilly. Management highlights significant upfront and research funding already received and several billion dollars of potential milestones across the portfolio, although realization of those amounts is uncertain and contingent on long-term success.
5. Regulatory & Event Timeline (Last 12 Months and Forward)
- Oct 2024 – FDA and Sangamo agree that eGFR slope at 52 weeks can support an accelerated approval pathway for ST-920 in Fabry disease.
- Dec 2024 – Pfizer terminates the hemophilia A gene therapy collaboration, removing a large potential milestone stream and hitting the share price.
- May 2025 – Nasdaq deficiency notice for minimum bid price below $1.00; initial deadline set for 27 October 2025.
- Jun 2025 – ST-920 STAAR registrational data released, showing positive mean annualized eGFR slopes and multi-organ benefits versus current standard therapy.
- Sep 2025 – Detailed STAAR data presented at ICIEM 2025 in Kyoto.
- Nov 6, 2025 – Q3 2025 results: cash $29.6M; net loss $34.9M; revenues $0.6M. Nasdaq grants extension until 27 April 2026; Pfizer pays $6M for zinc-finger cell line license.
- Nov 2025 – Company reiterates plans to submit a BLA for ST-920 as early as Q1 2026 and continues Fabry partnering discussions.
- Dec 3, 2025 – FDA grants Fast Track to ST-503 for SFN; STAND study sites active.
- Dec 18, 2025 – Rolling BLA submission initiated for ST-920; completion targeted by Q2 2026.
- Q1–Q2 2026 (planned) – Completion of rolling BLA for ST-920; potential updates on partnering.
- Mid-2026 (planned) – Target for ST-506 CTA submission for prion disease.
- By 27 Apr 2026 – Deadline to restore compliance with Nasdaq $1.00 minimum bid requirement.
6. Financial Position & Dilution
6.1 Income statement and revenues
For Q3 2025, Sangamo reported a net loss of $34.9M versus net income of $10.7M in Q3 2024, with revenues dropping to $0.6M from $49.4M as Genentech collaboration revenue fell away.
6.2 Cash and runway
As of 30 September 2025, cash and cash equivalents were $29.6M. Including the $6M payment from Pfizer in October 2025 and ATM proceeds, management guides runway only into Q1 2026. This implies a high likelihood of additional financing, partnering or restructuring actions.
7. Analyst Coverage & “Street” View
Consensus from major aggregators shows SGMO rated on average as a Hold, with a split between Buy, Hold and Sell opinions. Average 12-month target prices cluster in the $3.8–4.0 range, far above the current sub-$1.00 trading level, but with wide dispersion and clear dependence on Fabry success and financing outcomes.
9. Scenario Map – Including a Hypothetical Bullish Case if the BLA Is Accepted
The value of SGMO’s equity over the next 12–24 months hinges on three axes: (1) the Fabry ST-920 BLA, (2) the ability to secure funding or a partner without excessive dilution, and (3) Nasdaq compliance.
Bull case – BLA accepted and de-risked
- The rolling BLA for ST-920 is completed by Q2 2026 and the FDA formally accepts the BLA for review.
- During or shortly after acceptance, Sangamo signs a Fabry commercialization partnership with meaningful upfront and near-term milestones.
- New funding is largely partner-driven rather than pure equity issuance, limiting further dilution.
- The share price moves and stays above $1.00, solving Nasdaq compliance without an extreme reverse split.
- Neurology programs progress in the background, adding optional upside rather than being required to rescue the story.
In this hypothetical configuration the setup is clearly more bullish than today: regulatory risk on Fabry is partially de-risked, capital is reinforced by a partner, and listing risk is contained.
Base case – Progress with ongoing financing risk
- Rolling BLA is completed, but the exact timing and content of FDA acceptance and review milestones remain uncertain.
- No major Fabry partner signs near-term; funding continues through equity issuance, ATM and possibly debt.
- Nasdaq compliance is restored via a reverse split combined with modest price recovery.
The company survives and Fabry advances, but shareholder returns depend heavily on the balance between pipeline progress and dilution.
Bear case – Regulatory or financing breakdown
- The rolling BLA is delayed, rejected or requires additional large trials, pushing out timelines materially.
- Financing becomes difficult, forcing highly dilutive raises or unfavorable structured transactions.
- Nasdaq listing is lost or only preserved after an extreme reverse split without underlying improvement.
This scenario would likely result in permanent capital loss for many shareholders.
10. Risk Map
| Risk factor | Level | Comments |
|---|---|---|
| Regulatory (Fabry BLA) | Medium–High | Strong STAAR data and clear FDA dialogue on eGFR slope, but rolling submission has just begun and acceptance/approval are not guaranteed. |
| Financing / dilution | High | Runway into Q1 2026; further capital likely required, with risk of additional dilution. |
| Nasdaq listing | High | Extension only until 27 April 2026; failure to regain $1.00 could trigger delisting procedures. |
| Execution (commercial & operational) | Medium | Even with approval, Fabry commercialization will require pricing, reimbursement and manufacturing execution. |
| Pipeline technical risk (neurology) | Medium | ST-503 and ST-506 remain early-stage and may fail despite encouraging preclinical data. |
| Partner dependence | Medium | History with Pfizer shows partnerships can end abruptly, removing expected milestones. |
11. Key Source Links
- SGMO Investor Relations – news and SEC: https://investor.sangamo.com/
- Q3 2025 results and business highlights (Nasdaq copy).
- Rolling BLA submission announcement for ST-920 – 18 Dec 2025 (news wires).
- Fast Track designation for ST-503 – Dec 2025.
- Nasdaq minimum bid price extension – company 8-K.
- Analyst consensus – MarketBeat and similar services.
- Retail sentiment – Stocktwits, Reddit and X threads tagged $SGMO.
Analisi singolo titolo – SGMO
Sangamo Therapeutics (SGMO) – Fabry BLA contro rischio cassa
Dossier completo su Sangamo Therapeutics (NASDAQ: SGMO) aggiornato al 18 dicembre 2025: gene therapy ST-920 per Fabry, pivot neurologico, situazione finanziaria e diluizione, rischio di delisting da Nasdaq, sentiment di analisti e retail, con uno scenario potenzialmente rialzista nel caso in cui la BLA Fabry venga accettata in review.
Grafico e quadro tecnico
Riferimento intraday
Fonte grafico: Finviz , istantanea intraday intorno al 18 dicembre 2025. Per i dati aggiornati fare sempre riferimento alle fonti live.
1. Executive summary (IT)
Sangamo Therapeutics oggi è, di fatto, una scommessa concentrata su un driver principale: ST-920, gene therapy per la malattia di Fabry, per cui è stata avviata la procedura di rolling BLA verso la FDA. Il 18 dicembre 2025 l’azienda ha comunicato l’inizio della sottomissione a rotazione e l’obiettivo di completarla entro il secondo trimestre 2026.
Sul fronte finanziario la situazione è fragile: al 30 settembre 2025 la cassa era 29,6 milioni di dollari e il management parla esplicitamente di runway solo fino al primo trimestre 2026, includendo i 6 milioni ricevuti da Pfizer e le vendite via ATM. Nel frattempo il titolo ha ottenuto una estensione da Nasdaq fino al 27 aprile 2026 per rientrare sotto il requisito di prezzo minimo di 1 dollaro.
La parte “neurologica” della storia (ST-503 per small fiber neuropathy e ST-506 per le malattie da prioni), insieme alla piattaforma STAC-BBB con partner come Genentech, Astellas e Lilly, rappresenta un’opzione a medio-lungo termine, non una fonte di cassa nel breve.
La domanda chiave è binaria: Sangamo riuscirà a superare i prossimi 12–24 mesi senza bruciare troppo capitale e senza perdere il listing, mentre porta avanti ST-920 fino all’accettazione della BLA e alla review? Uno scenario in cui la BLA viene accettata per la revisione completa e, in parallelo, arriva un partner commerciale su Fabry renderebbe la storia sensibilmente più rialzista rispetto a oggi, ma resta un’ipotesi, non un dato di fatto.
2. Profilo azienda e modello di business
Sangamo Therapeutics (NASDAQ: SGMO) si presenta come società di genomic medicine focalizzata su terapie geniche e regolazione epigenetica per malattie rare e indicazioni neurologiche.
Pilastri principali
- Gene therapy Fabry – ST-920: terapia genica epatica di proprietà completa, pensata per aumentare in modo duraturo i livelli di α-Gal A e ridurre o eliminare la necessità di ERT cronica.
- Portafoglio neurologico – ST-503 e ST-506: regolatori epigenetici per small fiber neuropathy (ST-503) e malattie da prioni (ST-506), veicolati con capsidi STAC-BBB attraversando la barriera emato-encefalica.
- Monetizzazione piattaforma – STAC-BBB e collaborazioni: accordi di licensing e partnership su capsidi con big pharma (Genentech, Astellas, Eli Lilly) e collaborazioni legacy.
I ricavi attuali sono quasi interamente da collaborazioni e sono crollati nel 2025 per il venir meno di contributi significativi dal lato Genentech. Nel terzo trimestre 2025 i ricavi sono stati circa 0,6 milioni, contro 49,4 milioni nello stesso periodo del 2024.
4. Pipeline e programmi chiave
4.1 ST-920 (Fabry) – studio registrativo e BLA
ST-920 è la terapia genica di Sangamo per pazienti adulti con malattia di Fabry. L’obiettivo è ottenere una produzione duratura di α-Gal A dal fegato, in modo da sostituire l’ERT e migliorare il quadro multiorgano.
Lo studio STAAR (Phase 1/2, registrativo) ha prodotto nel 2025 una serie di dati chiave:
- pendenza media annualizzata dell’eGFR positiva a 52 settimane sull’intera coorte trattata;
- parametri cardiaci sostanzialmente stabili su almeno un anno di follow-up;
- elevazione duratura dell’attività di α-Gal A, con il paziente più longevo seguito per oltre 4 anni;
- sospensione dell’ERT in tutti i pazienti che la ricevevano all’ingresso, con livelli di lyso-Gb3 generalmente stabili dopo lo stop;
- miglioramenti in FOS-MSSI e in diversi parametri di qualità di vita;
- profilo di sicurezza e tollerabilità favorevole, senza bisogno di pre-conditioning.
La FDA ha accettato l’uso dell’eGFR slope a 52 settimane come endpoint primario per un percorso di accelerated approval. Il 18 dicembre 2025 Sangamo ha dichiarato di aver avviato la sottomissione “rolling” della BLA e di volerla completare entro il secondo trimestre 2026. Una rolling BLA però, da sola, non equivale all’accettazione formale della domanda per la review completa.
4.2 ST-503 – dolore neuropatico cronico (SFN)
ST-503 è un regolatore epigenetico su Nav1.7, pensato per il dolore cronico da small fiber neuropathy.
- Studio STAND (Phase 1/2): centri attivi e reclutamento in corso.
- Dati preclinici 2025 su primati non umani mostrano durata, potenza e selettività con buon profilo di sicurezza.
- Il 3 dicembre 2025 la FDA ha concesso la Fast Track per il trattamento della SFN.
La stessa azienda non si aspetta segnali di efficacia prima della fine 2026, quindi è un catalyst a medio termine.
4.3 ST-506 – malattia da prioni
ST-506 utilizza la piattaforma STAC-BBB per colpire le malattie da prioni con un approccio epigenetico.
- Lavoro di preparazione CTA in corso, con allineamento regolatorio sul CMC nel Regno Unito.
- Modelli preclinici indicano estensioni di sopravvivenza molto marcate.
- Target interno per la submission CTA: metà 2026.
4.4 Piattaforma STAC-BBB e programmi in partnership
I capsidi STAC-BBB sono al centro di varie collaborazioni con big pharma (Genentech, Astellas, Lilly). Sangamo evidenzia già incassi upfront significativi e un monte potenziale di milestone nell’ordine dei miliardi di dollari, anche se si tratta di numeri teorici vincolati al successo clinico e commerciale nel lungo periodo.
5. Timeline regolatoria ed eventi (ultimi 12 mesi e outlook)
- Ottobre 2024 – accordo con FDA su eGFR slope a 52 settimane come base per accelerated approval in Fabry.
- Dicembre 2024 – Pfizer termina la collaborazione su emofilia A, rimuovendo un’importante fonte potenziale di milestone.
- Maggio 2025 – notifica Nasdaq per mancato rispetto del prezzo minimo di 1 dollaro; prima scadenza a ottobre 2025.
- Giugno 2025 – pubblicazione dei dati registrativi STAAR su ST-920.
- Settembre 2025 – presentazione dettagliata dei dati Fabry a ICIEM 2025 (Kyoto).
- 6 novembre 2025 – risultati Q3 2025, cassa 29,6 milioni, estensione Nasdaq fino al 27 aprile 2026, pagamento Pfizer da 6 milioni.
- Novembre 2025 – conferma della volontà di presentare la BLA Fabry quanto prima e di chiudere un accordo commerciale.
- 3 dicembre 2025 – Fast Track FDA per ST-503 in SFN.
- 18 dicembre 2025 – avvio della rolling BLA per ST-920, completion mirata a Q2 2026.
- Q1–Q2 2026 (piano) – completamento BLA e possibili sviluppi lato partner Fabry.
- Metà 2026 (piano) – CTA per ST-506 in prion disease.
- Entro 27 aprile 2026 – deadline per il rientro nei requisiti di prezzo minimo Nasdaq.
6. Situazione finanziaria e diluizione
6.1 Conto economico e ricavi
Nel terzo trimestre 2025 Sangamo ha registrato una perdita netta di 34,9 milioni di dollari, contro un utile di 10,7 milioni nel Q3 2024, con ricavi scesi da 49,4 a 0,6 milioni per la fine del contributo Genentech. È una struttura tipica da biotech in fase di R&D pesante e ricavi quasi solo da collaborazioni.
6.2 Cassa e runway
Al 30 settembre 2025 la cassa era pari a 29,6 milioni. Tenendo conto del pagamento da 6 milioni ricevuto da Pfizer a ottobre e dell’uso dell’ATM, il management parla esplicitamente di runway solo fino al primo trimestre 2026. Questo implica alta probabilità di ulteriori interventi sul capitale (equity, deal, tagli o una combinazione di questi).
7. Consenso analisti
I principali aggregatori mostrano un giudizio medio di tipo Hold su SGMO, con mix di raccomandazioni Buy, Hold e Sell. I target medi a 12 mesi sono nell’area 3,8–4 dollari, cioè multipli dell’attuale prezzo di mercato, ma dipendono in modo sensibile dal successo di Fabry e dalla gestione del rischio finanziario.
9. Mappa scenari – con bull case se la BLA viene accettata
Il valore di SGMO nei prossimi 12–24 mesi dipende da tre assi: (1) percorso BLA Fabry ST-920, (2) capacità di finanziare l’azienda senza eccessiva diluizione, (3) rientro nei requisiti Nasdaq.
Scenario rialzista – BLA accettata e rischio ridotto
- La rolling BLA viene completata entro Q2 2026 e la FDA accetta formalmente la domanda per la review.
- In parallelo Sangamo firma un accordo commerciale su Fabry con upfront e milestone significativi.
- La maggior parte della nuova finanza arriva da partner e non solo da equity pura, limitando la diluizione.
- Il prezzo si riporta in modo stabile sopra 1 dollaro, risolvendo il problema Nasdaq senza split estremi.
- I programmi neurologici avanzano, aggiungendo optionalità ma senza essere costretti a “salvare” la tesi.
In questa configurazione la storia diventa chiaramente più bullish rispetto a oggi: parte del rischio regolatorio su Fabry è ridotto, la cassa viene rafforzata e il tema del listing passa in secondo piano.
Scenario intermedio – progresso con rischio cassa
- La BLA viene completata ma i tempi e i contenuti delle tappe FDA restano poco visibili.
- Nessun partner Fabry importante nel breve; il finanziamento continua tramite aumenti di capitale e strumenti similari.
- La compliance Nasdaq viene ripristinata principalmente tramite reverse split.
L’azienda va avanti e Fabry progredisce, ma il ritorno per gli azionisti è fortemente dipendente dal mix tra progresso clinico e diluizione.
Scenario ribassista – problemi regolatori o finanziari
- La rolling BLA subisce ritardi, viene respinta o richiede nuovi studi di grandi dimensioni.
- La raccolta di capitale diventa difficile, costringendo a operazioni fortemente diluitive o strutture pesanti.
- Il listing Nasdaq viene perso o mantenuto solo dopo uno split molto aggressivo senza reale miglioramento di fondo.
In questo scenario il rischio di perdita permanente di capitale per molti azionisti è concreto.
10. Mappa rischi (riassunto)
| Fattore di rischio | Livello | Commento |
|---|---|---|
| Rischio regolatorio Fabry (BLA) | Medio–alto | Dati STAAR solidi e dialogo FDA chiaro, ma il processo di rolling è appena iniziato; accettazione e approvazione non sono garantite. |
| Cassa e diluizione | Alto | Runway dichiarata fino a Q1 2026; probabile necessità di nuova finanza con rischio di ulteriore diluizione. |
| Rischio Nasdaq | Alto | Deadline 27 aprile 2026 per tornare sopra 1 dollaro; in caso contrario possibile delisting. |
| Esecuzione commerciale | Medio | Anche con eventuale approvazione Fabry, restano incognite su prezzo, rimborso e produzione. |
| Rischio tecnico pipeline neurologica | Medio | ST-503 e ST-506 sono ancora in fasi iniziali, con rischio standard da biotech early stage. |
| Dipendenza da partner | Medio | Il precedente con Pfizer dimostra che i partner possono uscire anche in presenza di dati interessanti. |
11. Fonti principali
- Investor Relations Sangamo – news e SEC: https://investor.sangamo.com/
- Risultati e comunicato Q3 2025.
- Comunicati su rolling BLA ST-920 e Fast Track ST-503 (dicembre 2025).
- Comunicazioni e 8-K relativi all’estensione Nasdaq.
- Consenso analisti da MarketBeat e altri aggregatori.
- Sentiment retail da Stocktwits, Reddit e X su ticker SGMO.
Per una visione più ampia dei catalyst in arrivo su FDA, dati clinici e operazioni corporate nel settore biotech, puoi consultare il Biotech Catalyst Calendar dedicato qui: Biotech Catalyst Calendar – Merlintrader . Viene aggiornato regolarmente e aiuta a posizionare SGMO all’interno del quadro generale dei catalyst.
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


